Brenzcatechin (1,2-Dihydroxybenzol) ist eine farblose organische Verbindung, die auch in der Natur in Spuren vorkommt. Die Molekularstruktur ist durch zwei benachbarte, sich in ortho-Position befindende Hydroxygruppen am Benzolring charakterisiert. Die englische Bezeichnung ist Catechol (Kurzform von Pyrocatechol), nach IUPAC wird es auch 1,2-Dihydroxybenzen oder Benzen-1,2-diol genannt.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Brenzcatechin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C6H6O2 | |||||||||||||||||||||
| Kurzbeschreibung |
farblose Kristalle[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 110,11 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Dichte |
1,34 g·cm−3[1] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt |
245 °C[1] | |||||||||||||||||||||
| Dampfdruck | ||||||||||||||||||||||
| Löslichkeit | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| MAK |
Schweiz: 5 ml·m−3 bzw. 23 mg·m−3[5] | |||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Außer Brenzcatechin (1,2-Dihydroxybenzol) existieren zwei weitere stellungsisomere Formen, nämlich das Resorcin (1,3-Dihydroxybenzol) und das Hydrochinon (1,4-Dihydroxybenzol).
Geschichte
Der Trivialname der chemischen Verbindung geht auf die Gerber-Akazie (Acacia catechu) zurück. Aus deren Pflanzensaft, der Catechin enthält, wurde sie erstmals 1839 vom deutschen Chemiker Hugo Reinsch durch trockene Destillation, sogenanntes Brenzen (altertümliche Bezeichnung für Pyrolyse), isoliert.[7] 1841 wurde die Substanz von den deutschen Chemikern Heinrich Wackenroder und Constantin Zwenger unabhängig voneinander beschrieben.[8][9] August Kekulé charakterisierte die Verbindung 1867 als das Diol des Benzols.[10] Außerdem waren für Brenzcatechin die Bezeichnungen Pyrocatechin und Pyrocatechol geläufig.[11]
Vorkommen

Brenzcatechin ist im Pflanzenreich verbreitet und kommt unter anderem in Zwiebeln, Anadenanthera peregrina, der Gemeinen Wegwarte, Grapefruitpflanzen, Erdbeeren (Fragaria spp), Virginischem Tabak, Olivenbäumen, Oregano, Guaraná, Avocadopflanzen, Portulak, Pterocarpus marsupium, dem Kakaobaum und Gewürzvanille vor.[12] Es kann durch Pyrolyse (Brenzreaktion) natürlicher Rohstoffe wie Holz, Kohle und Lignin erhalten werden. Es ist mehrheitlich in Baumharz und Buchenholzteer enthalten. Früher wurde es auch aus den Schwelwässern der Braunkohle gewonnen.[13]
Außerdem ist Brenzcatechin in signifikanten Mengen auch in Tabakrauch zu finden (je nach Marke 20–500 µg pro Zigarette).[14][15] Dort wird Brenzcatechin auch eine Mitwirkung an der tumorpromovierenden Wirkung des Tabakrauchs zugewiesen. Als mögliche Mechanismen wurden unter anderen die Translokation der PKC und die Bildung von 8-Hydroxydesoxyguanosin vorgeschlagen.[16][17]
Gewinnung und Darstellung
Brenzcatechin lässt sich mit Hilfe einer Alkalischmelze[18] von o-Chlorphenol oder o-Phenolsulfonsäure darstellen.


Auch durch Hydrolyse von 2-Chlorphenol mit Natronlauge bei höherer Temperatur in Gegenwart von Kupfersulfat, auch in Gegenwart von Bariumhydroxid und Kupfer(I)-chlorid[13] oder durch den oxidativen Abbau von Salicylaldehyd mit Wasserstoffperoxid und Natronlauge (Dakin-Reaktion).[19]
Eigenschaften
Physikalische Eigenschaften
Brenzcatechin bildet farblose Kristalle, die bei 105 °C schmelzen.[20] Die Schmelzenthalpie wurde mit 22,87 kJ·mol−1 bestimmt.[21] Der Siedepunkt unter Normaldruck liegt bei 245 °C.[22] Die Standardverdampfungsenthalpie beträgt 71,9 kJ·mol−1.[21] Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 5,5033, B = 2713,153 und C = −23,96 im Temperaturbereich von 391,7 bis 518,7 K.[23]
Chemische Eigenschaften
An der Luft und bei Lichteinfall wird es instabil und oxidiert zu 1,2-Benzochinon (Autoxidation).

Die wässrige Lösung ist farblos, wird aber bei pH-Werten über 7 in Gegenwart von Sauerstoff schnell durch Oxidation braun. In neutraler Lösung ergibt die Kombination mit Eisen(III)-chlorid eine Grünfärbung. Diese Reaktion kann zur Unterscheidung der Dihydroxybenzole dienen: Resorcin gibt eine violette Färbung, Hydrochinon eine Blaufärbung, die nach kurzer Zeit wieder verschwindet, da das Hydrochinon vom Eisen(III)-chlorid zum p-Benzochinon oxidiert wird, das keine Farbreaktion zeigt.[24] Mit Blei(II)-acetat bildet sich dagegen ein farbloser Niederschlag. Eine blaugrüne Färbung gibt die Reaktion von Brenzcatechin mit „Vanadinschwefelsäure“ → Mandelin-Reagenz.[25][26] Ebenfalls eine blaugrüne Färbung gibt die Reaktion mit Chlorkalk.[26]
Verwendung
Die Verwendungsmöglichkeiten von Brenzcatechin liegen in der Fototechnik als Entwickler. Zum Einsatz kommt es als Antioxidations- und Desinfektionsmittel. In der organischen Synthese spielt es eine Rolle als Ausgangsmaterial für Farbstoffe, Riechstoffe und Arzneimittel sowie als Schutzgruppe für Carbonylverbindungen. Etwa 50 % des synthetischen hergestellten Brenzcatechins wird zur Herstellung von Pestiziden verwendet, wobei der Rest als Vorstufe zu Chemikalien zur Herstellung von Parfüms und Arzneimitteln dient.[27]
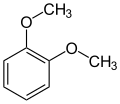
Das Hydroborierungsmittel Catecholboran ist ein Derivat von Brenzcatechin. Methylierungen ergeben Guajacol (Monomethylether) und Veratrol (Dimethylether):[28]


Nachweis
Zum qualitativ-analytischen Nachweis entsteht bei der Bromierung mit Kaliumbromid und Brom[29] das Tetrabromderivat mit einem Schmelzpunkt von 192 °C.[30]

Sicherheitshinweise
Die Dihydroxybenzole reizen Augen, Haut und Atemwege. Sie sind gesundheitsschädlich bei Berührung mit der Haut und beim Verschlucken. Brenzcatechin ist giftig für Wasserorganismen und daher als umweltgefährlich in Wassergefährdungsklasse 2 eingestuft.[1] Auf Vorschlag der französischen Chemikalienbehörde wurde 2015 und 2016 die chemikalienrechtliche Einstufung von Brenzcatechin überarbeitet. Der Ausschuss für Risikobewertung (RAC) der Europäischen Chemikalienagentur (ECHA) hat am 16. September 2016 die Einstufung für Brenzcatechin wie folgt entschieden: Brenzcatechin wird als krebserzeugend Carc 1B, Muta 2 sowie Acute Tox 3 für orale und dermale Gabe eingestuft. Die Warnhinweise wurden festgelegt auf H301 und H311 (giftig bei Verschlucken und Hautkontakt), sowie H341 (möglicherweise mutagen) und H350 (krebserregend). Die Einstufungen als hautreizend Kategorie 2 und augenreizend Kategorie 2 wurden mit den entsprechenden Warnhinweisen H315 und H319 beibehalten.[31]
Metabolismus und Toxikologie
Wie andere Dihydroxybenzene auch, wird Brenzcatechin im Gastrointestinaltrakt absorbiert und im Urin frei, als Monosulfat (Sulfatierung) oder als Monoglucuronid (Glucuronidierung) ausgeschieden.[32] Im Metabolismus entsteht als Zwischenprodukt (neben dem Sulfat und Glucuronid) hauptsächlich 1,2-Benzochinon, untergeordnet auch Hydroxyhydrochinon.[33] Außerdem kam es in Einzelfällen zu einer Kontaktdermatitis führen.[34] In bestimmten Zelllinien induzierte Brenzcatechin die Apoptose von Zellen.[35] In Erythrozyten kann es Hämolyse verursachen.[36]
Auf einer molekularen Ebene wird vermutet, dass Brenzcatechin die Chinone und Radikale bildet[37] und in Kombination mit dem Verbrauch von Antioxidanzien wie Glutathion insgesamt ein Absinken der antioxidativen Kapazität verursacht und so zu oxidativem Stress führt.[38] Dieser könnte ursächlich für die Induktion von DNA-Schäden sein.[39] Außerdem kann Catechol mit Cysteinresten interagieren und so eventuell zur Aggregation von Proteinen oder zur Bildung von Disulfidbrücken führen.[40]
Abgeleitete Verbindungen
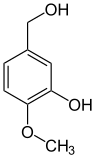
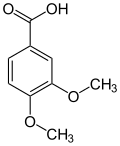
Vom Brenzcatechin und seinen Methylethern Guajacol und Veratrol leiten sich formal zahlreiche Naturstoffe ab, darunter das bekannte Vanillin.
Einzelnachweise
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.