Bortrifluorid
chemische Verbindung Aus Wikipedia, der freien Enzyklopädie
chemische Verbindung Aus Wikipedia, der freien Enzyklopädie
Bortrifluorid ist eine chemische Verbindung, bestehend aus den Elementen Bor und Fluor. Es besitzt die Summenformel BF3 und wird manchmal auch als Trifluorboran bezeichnet.
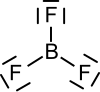
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Bortrifluorid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | BF3 | |||||||||||||||
| Kurzbeschreibung |
farbloses, stechend riechendes, an feuchter Luft rauchendes Gas[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 67,81 g·mol−1 | |||||||||||||||
| Aggregatzustand |
gasförmig[2] | |||||||||||||||
| Dichte | ||||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
−100,4 °C[2] | |||||||||||||||
| Dampfdruck |
28 bar (bei −30 °C)[4] | |||||||||||||||
| Löslichkeit |
reagiert heftig mit Wasser[2] | |||||||||||||||
| Dipolmoment |
0[5] | |||||||||||||||
| Brechungsindex |
1,316 (20 °C, Dihydrat)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK | ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−1136,0(8) kJ/mol[8] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Bortrifluorid kann gewonnen werden durch:
Bortrifluorid bildet eine trigonal-planare Molekülstruktur aus. Es ist eine sehr giftige, bei Raumtemperatur gasförmige chemische Verbindung, die eine kritische Temperatur von −12,3 °C besitzt.
Bortrifluorid ist eine sehr starke Lewis-Säure (Elektronenpaarakzeptor). Es bildet mit Elektronenpaardonatoren Additionsverbindungen (Lewis-Säure-Base-Addukte).
Mit Wasser reagiert es unter Zersetzung zu Borsäure und Flusssäure. Im Gegensatz zu den anderen Bortrihalogeniden findet keine direkte Hydrolyse statt, sondern eine Abfolge mehrerer Reaktionen. Dabei bildet sich aufgrund der starken BF3-Bindung zunächst ein Lewis-Säure-Base-Addukt.
Allerdings ist die Hydrolyse im Gegensatz zu anderen Borhalogeniden nicht vollständig, da sich auch das inerte, tetraedrische Tetrafluoroboration (BF4−) bildet.
Auch die Produkte der Hydrolyse reagieren weiter zur Tetrafluorborsäure, die als Oxoniumsalz vorliegt.
In der chemischen Industrie kann Bortrifluorid für eine Vielzahl von chemischen Reaktionen als Katalysator bzw. als Ausgangsstoff zur Herstellung verschiedener Borverbindungen eingesetzt werden. Gasförmiges Bortrifluorid und Bortrifluorid-Addukte werden hauptsächlich als Katalysatoren oder Co-Katalysatoren benutzt, zum Beispiel bei der Herstellung von Polymeren, hochwertigen Schmierölen, Pharmazeutika, Aroma- und Duftstoffen und weiteren Feinchemikalien sowie zur Synthese von Borverbindungen wie zum Beispiel Alkylboranen, Aminboranen und Reagenzien für die Suzuki-Kupplung. Weiterhin wird es in der Halbleiterindustrie als Borlieferant für die Ionenimplantation (p-Dotierung), zur Oberflächenbehandlung von Stahl und Glas und in Neutronendetektoren verwendet.
Bortrifluorid ist sehr giftig und stark ätzend.

Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.