Styren
chemická sloučenina From Wikipedia, the free encyclopedia
Styren (fenylethen, vinylbenzen) je aromatická průmyslová chemikálie. Patří k přírodním produktům . Jako bezbarvou čirou kapalinu s charakteristickým zápachem jej poprvé izoloval berlínský lékárník Johann Eduard Simon v roce 1839 z pryskyřice stromu Liquidambar orientalis. Nejnovější výzkumy dokládají použití styrenu při mumifikaci mrtvých již ve starém Egyptě. V nízkých koncentracích se nachází v tabákovém kouři, v ovoci (jahody, broskve), v oříšcích, zrnech obilí a kávy a skořici. Průmyslový výrobek je dodáván o koncentraci 99,8 %.[2]
| Styren | |
|---|---|
 | |
 | |
| Obecné | |
| Systematický název | ethenylbenzen |
| Triviální název | styren |
| Ostatní názvy | vinylbenzen, cinnamen, fenylethylen |
| Anglický název | Styrene |
| Německý název | Styrol |
| Sumární vzorec | C8H8 |
| Vzhled | bezbarvá až nažloutlá viskózní kapalina |
| Identifikace | |
| Registrační číslo CAS | 100-42-5 |
| Vlastnosti | |
| Molární hmotnost | 104,15 g/mol |
| Teplota tání | −30 °C |
| Teplota varu | 145 °C |
| Hustota | 0,909 g/cm³ |
| Rozpustnost ve vodě | < 1 % |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| H-věty | H226 H361d H332 H372 (sluchové orgány) H315 H319 |
| R-věty | R10 R20 R36/38 R40 |
| S-věty | (S2) S23 |
Některá data mohou pocházet z datové položky. | |
Výroba
Nejčastěji se vyrábí dehydrogenací ethylbenzenu za použití selektivních katalyzátorů v dehydrogenačních aparátech a účinných rektifikačních kolonách. Zatímco proces výroby ethylbenzenu je exotermní, vyžaduje proces dehydrogenace ethylbenzenu na styren značné množství energie. Proto se moderní jednotky stavějí jako paralelní na jednom místě ke vzájemnému sdílení energií s kapacitami styrenu přes 500 tis. tun za rok.[2]
Současné světové kapacity výroben styrenu se blíží 30 mil. tun/rok. Dominuje s více než 60 % podílem Asie, následuje Evropa s pětinovým podílem a Amerika s 18 % podílem. Čína je nyní díky politice soběstačnosti nezávislá na dovozu. Mezi pět největších výrobců styrenu se řadí: Ineos, Loyal, Xinga Group, Total a Trinseo s kapacitami 2,2 mil. tun/rok u první společnosti, po 1,3 mil. tun u páté. V rámci evropské asociace Plastics Europe působí skupina 8 z evropských výrobců styrenu jako Styrene Producers Association (SPA): BASF, Ineos, LyondellBasell, Repsol, Shell, Total, Trinseo, Versalis, která vydala v červenci 2022 publikaci „Styrene Monomer: Safe Handling Guide“, ve které jsou shrnuty informace o vlastnostech styrenu, včetně zdravotních a ekologických aspektů a zásad transportu, skladování a aplikací.[2]
Tuzemská výroba
Tuzemská výroba styrenu v Kaučuku Kralupy byla úspěšně zahájena 29. července 1963. Jednalo se o výrobní jednotku s roční kapacitou 28.000 tun. Ethylbenzen, který byl dodávaný produktovodem z Litvínova, se dehydrogenoval na železitém katalyzátoru v přebytku přehřáté vodní páry. Katalyzátor byl vyráběn v Litvínově dle podkladů z VUSK Kralupy nad Vltavou. Endotermní dehydrogenace ethylbenzenu na styren byla prováděna v adiabatickém reaktoru při průměrné teplotě 600 °C, přičemž se tepelná kapacita reakční směsi zvyšovala přídavkem přehřáté páry. V reaktoru se tak dosahovala konverze ethylbenzenu na styren asi 60 % hm. a kapalná reakční směs se dělila na nezreagovaný ethylbenzen a styren účinnou rektifikací.[2]
Kapacita jednotky na výrobu styrenu ve výši 28 kt spuštěná v roce 1963 záhy limitovala další rozvoj výroby styren-butadienového kaučuku a blokového polystyrenu. Byla proto vystavěna nová výrobní jednotka, tzv. Styren II, o kapacitě 40 kt. Nová jednotka disponovala výkonnějším reaktorem dehydrogenace a kloboučkovou rektifikační kolonou. Potřebnou výstavbu velkokapacitní výrobny styrenu, tzv. Styren III, se nepodařilo prosadit do státního plánu. Proto kralupský podnik v období 1982–1989 využil několik devizově návratných úvěrů pro rozvoj výroby styrenu, kdy byla zvýšena kapacita stávající jednotky z 68 kt/rok až na 112 kt/rok. Potřebné devizy ke splácení úvěru byly v tomto případě získávány exportem ze zvýšené výroby polystyrenu. Licence byla zakoupena od francouzské firmy CdF Chemie Engineering (Technip Lyon). V několika etapách byly staré reaktory přestavěny, resp. nahrazeny novými výkonnějšími a energeticky méně náročnými dvouložovými dehydrogenizačními reaktory. Tato modernizační akce představovala úsporu energií ve výši 173 TJ ročně. Výstavba rektifikační výplňové rektifikační kolony o kapacitě 60 kt/rok byla realizována podle licence firmy Sulzer.[2]
V polovině 90. let byla opět řešena zvýšená potřeba styrenu. Konkrétní přípravy na stavbu nové jednotky styrenu v předcházejícím období vrcholily v březnu roku 1996 zpracováním dokumentace pro územní rozhodnutí. Prostor pro novou jednotku byl vytvořen na místě provozů a staveb z období výstavby závodu. Byly odstřeleny výrobny kontaktní pece, kompresorová a výparníková stanice, které byly součástí někdejší výroby butadienu. Vzhledem k předchozím výrobám různými technologiemi získala tato investiční akce a posléze i jednotka název Styren III. Kontrakt o výstavbě jednotky na 130 kt/rok, což byla nejvýznamnější investice od r. 1963, byl podepsán v roce 1996 s firmou ABB Lummus s tím, že realizační harmonogram akce Styren III byl vytyčen na 24 měsíců. Koncem srpna 1997 došlo na staveništi k symbolickému výkopu.[2]
V roce 1998 byla výstavba výrobní jednotky Styren III dokončena. Společně s ní byla dokončena i výstavba jednotky výroby blokového krystalového polystyrenu. Návazně byla v červenci 2000 podepsána dohoda s firmou ABB Lummus Global na další rozšíření výroby styrenu ze 130 kt/rok na roční kapacitu 170 kt s využitím technologie SMART. Jednotka s rozšířenou kapacitou byla zprovozněna na podzim roku 2001.[2]
Vlastnosti
Za běžných podmínek jde o bezbarvou až nažloutlou kapalinu pronikavě nasládlého zápachu. Snadno těká, na vzduchu se oxiduje a vytvářejí se peroxidy, které působí jako katalyzátor polymerizace společně s dalšími parametry, jako je tlak, teplota, světlo a silné kyseliny. Proto se styren stabilizuje přídavkem inhibitorů, např. hydrochinonem. V přírodě se volně nenalézá, metabolicky však vzniká jako produkt rozkladu kyseliny skořicové. Je špatně rozpustný ve vodě, ale dobře se rozpouští v organických rozpouštědlech (alkoholy, aceton a sirouhlík aj.).
Použití
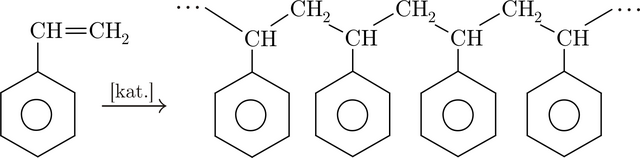
Je využíván při výrobě barviv, plastů, v gumárenském průmyslu. Jeho výskyt v atmosféře je především důsledkem antropogenní činnosti. Nejvýznamnější je jeho využití k polymeraci za účelem výroby jednoho z nejběžnějších plastů – polystyrenu. Ale využívá se i ve výrobě lepidel, fotografických filmů, inkoustů, automobilových součástek, obalových materiálů, plastového nádobí a řady dalšího spotřebního zboží.
Toxicita
Styren má narkotické a lokálně dráždivé účinky. Koncentrace 70 ppm ještě nevyvolává dráždění, koncentrace 100 ppm je snesitelná, koncentrace 200 ppm až 400 ppm vyvolává nepříjemný pocit zápachu. Nad koncentraci 400 ppm se projevuje dráždivý účinek, nad 800 ppm se projevuje narkotizační účinek a při koncentraci nad 1 300 ppm je již pobyt nesnesitelný. Nejsou vyloučeny pozdní účinky, například edém plic. Při požití je nepatrně jedovatější než benzen. Při styku s kůží dochází k jejímu vysušení a dráždění. Při styku s rohovkou dochází k dráždění až trvalému poškození. Chronická expozice se projevuje pseudoneurastenickými poruchami, změnami v jaterních funkcích a poklesem krevního tlaku. Mezi dalšími následky chronické expozice patří hepatotoxické účinky a atrofie sliznice horních cest dýchacích. Jako test expozice styrenu je možno použít analýzu kyseliny mandlové v moči. Mezinárodní agentura pro výzkum rakoviny (IARC) řadí styren mezi karcinogeny skupiny 2B .[3] Několik studií u pracovníků vystavených styrenu při výrobě plastů nalezlo zvýšený počet chromozomálních aberací v periferních lymfocytech.[4]
Americká organizace SIRC již více než 30 let komplexní výzkumný program, jehož cílem je lépe porozumět potenciálu styrenu ovlivňovat lidské zdraví, pokud vůbec tento účinek existuje. Značnou pozornost věnoval SIRC řešení karcinogenního potenciálu styrenu, dále zkoumali potenciální neurotoxicitu styrenu, reprodukční a vývojovou toxicitu a genotoxicitu.[2]
V roce 2019 bylo dokončeno aktualizované hodnocení rizik styrenu, které potvrdilo bezpečnost styrenu pro širokou populaci a doplnilo soubor znalostí o potenciálních účincích na zdraví při expozicích na pracovišti se závěry:
- Za normálních okolností jsou naměřené environmentální koncentrace styrenu ve vzduchu, vodě a půdě příliš nízké, aby účinkovaly škodlivě na organismy.
- Je nepravděpodobné, že by došlo k nepříznivým zdravotním účinkům v důsledku expozice styrenu prostřednictvím výrobků ze styrenu, včetně plastů.
- Rozsáhlý výzkum ukazuje, že styren nepřetrvává ani se nehromadí v atmosféře, v půdách či vodách, včetně pitných.
- Pracovní rizika pro většinu pracovních aktivit se styrenem jsou v přijatelných rozmezích.
- Neexistují žádné silné nebo konzistentní náznaky, že styren způsobuje u lidí jakoukoliv formu rakoviny. Důkazy o karcinogenitě styrenu z některých studií jsou neprůkazné.[2]
V životním prostředí
Po uvolnění do ovzduší se styren mění v benzaldehyd a formaldehyd. Poločas setrvání v ovzduší je kolem dvou hodin. V městském prostředí se styren vyskytuje v koncentracích okolo 0,3 μg/m³, ve znečištěném ovzduší až 20 μg/m³.[4]
V rámci procesů udržitelnosti plastů se postupně realizují procesy chemických recyklací odpadních polystyrenových polymerů na styren. Využívají se technologie depolymerizací, např. katalytická mikrovlnná depolymerizace firmy Pyrowave, nebo proces ReVital společnosti Agilyx. Takto získaný styren je nutno rektifikovat.[2]
Odkazy
Wikiwand - on
Seamless Wikipedia browsing. On steroids.



