chemická sloučenina From Wikipedia, the free encyclopedia
Dimethylamin (též DMA) je organická sloučenina se vzorcem (CH3)2NH. Tento sekundární amin je bezbarvý, hořlavý, zkapalnitelný plyn se zápachem po amoniaku. Obvykle se používá ve formě vodného roztoku o koncentraci do 40 %. V roce 2005 činila roční světová výroba 270 tisíc tun.[1]
| Dimethylamin | |
|---|---|
 Strukturní vzorec | |
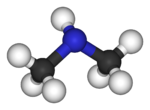 Model molekuly | |
| Obecné | |
| Systematický název | N-methylmethanamin |
| Funkční vzorec | (CH3)2NH |
| Sumární vzorec | C2H7N |
| Vzhled | bezbarvý plyn |
| Identifikace | |
| Registrační číslo CAS | 124-40-3 |
| PubChem | 674 |
| ChEBI | 17170 |
| SMILES | CNC |
| InChI | InChI=1S/C2H7N/c1-3-2/h3H,1-2H3 |
| Číslo RTECS | IP8750000 |
| Vlastnosti | |
| Molární hmotnost | 45,085 g/mol |
| Teplota tání | −93,00 °C |
| Teplota varu | 7–9 °C |
| Hustota | 0,6496 g/cm3 |
| Disociační konstanta pKb | 3,29 |
| Rozpustnost ve vodě | 1,540 kg.dm−3 |
| Tlak páry | 170,3 kPa (20 °C) |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −21 až −17 kJ/mol |
| Bezpečnost | |
| H-věty | H220 H302 H315 H318 H332 H335 |
| P-věty | P210 P261 P280 P305+351+338 |
Některá data mohou pocházet z datové položky. | |
Molekula dimethylaminu je složena z atomu dusíku se dvěma methylovými substituenty a jedním protonem. Dimethylamin je zásaditý; pKa amonné soli CH3-NH2+-CH3 je 10,73, tedy více než v případě methylaminu (10,64) a trimethylaminu (9,79).
Dimethylamin reaguje s kyselinami a tvoří soli, například dimethylamin-hydrochlorid, bezbarvou pevnou látku tající při 171,5 °C. Dimethylamin se vyrábí katalytickou reakcí methanolu a amoniaku za zvýšené teploty a vysokého tlaku:[2]
Dimethylamin je prekurzorem různých průmyslově významných sloučenin.[1][3] Reaguje se sirouhlíkem za vzniku dimethyldithiokarbamátu, prekurzoru chemikálií široce používaných při vulkanizaci gumy. Z dimethylaminu se vyrábějí také rozpouštědla dimethylformamid a dimethylacetamid. Je též surovinou pro výrobu mnoha zemědělských a farmakologických produktů, například dimefoxu nebo difenhydraminu. Od DMA je odvozena i nervově paralytická látka tabun. Tenzid lauryldimethylaminoxid získaný z dimethylaminu se používá v mýdlech a čisticích prostředcích. Nesymetrický dimethylhydrazin je raketové palivo připravované z dimethylaminu.
Rus domácí využívá dimethylamin jako feromon pro komunikaci.[4]
DMA podléhá ve slabě kyselém prostředí nitrozaci na dimethylnitrosamin. Tato látka karcinogenní pro zvířata byla detekována a kvantifikována ve vzorcích lidské moči a může být i produktem nitrozace DMA oxidy dusíku přítomnými v kyselém dešti v silně industrializovaných zemích.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.