
Cel·la electrolítica
From Wikipedia, the free encyclopedia
Cel·la electrolítica és el dispositiu utilitzat per a la descomposició mitjançant corrent elèctric de substàncies ionitzades anomenades electròlits.[1]
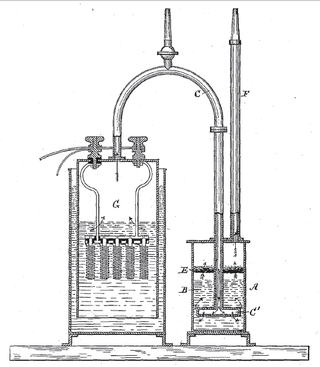

La cel·la electrolítica és una cel·la electroquímica que experimenta una reacció química redox quan se li aplica energia elèctrica. Demanera similar a una cel·la galvànica, les cel·les electrolítiques normalment consten de dues meitats de cel·la.
El procés de dissociació o descomposició realitzat en la cel·la electrolítica s'anomena electròlisi.
Exemples importants d'electròlisi són la descomposició de l'aigua en hidrogen i oxigen i la bauxita en alumini i altres productes químics.
Una cel·la electrolítica té tres parts components: un electròlit i dos elèctrodes (un càtode i un ànode). Només amb un potencial elèctric extern (és a dir, voltatge) de polaritat correcta i magnitud suficient hi pot haver descomposició. Els electròlits poden ser àcids, bases o sals.