Electròlit
From Wikipedia, the free encyclopedia
Un electròlit és una substància química que es dissocia en ions lliures quan es dissol en un dissolvent ionitzant o es fon, produint un medi conductor de l'electricitat.
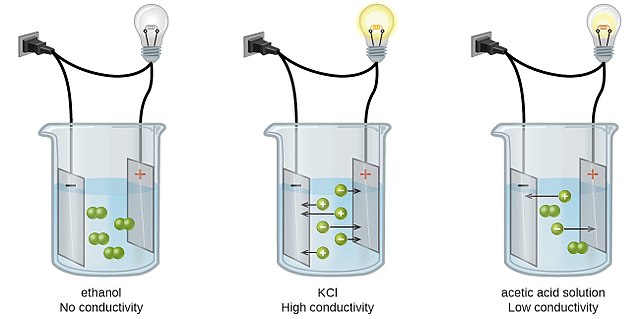
La conductivitat electrolítica és producte del moviment dels ions (positius o cations i negatius o anions), i això la diferencia de la conductivitat deguda als electrons (cas de la conducció en els metalls i en els semiconductors). Són electròlits els àcids (àcid sulfúric, àcid nítric...), les bases (hidròxid de sodi, amoníac...) i les sals (clorur de sodi, nitrat de potassi...). Són no-electròlits els metalls (ferro, coure...) i la majoria de composts covalents (diamant, acetona, benzè...).[1]
El mot «electròlit» prové de l’anglès electrolyte, mot creat el 1834 pel científic anglès Michael Faraday (1791–1867), de electro- (forma prefixada del mot elèctric) i el grec λυτός lytos ‘soluble’.[2]