
Leucinski zatvarač
From Wikipedia, the free encyclopedia
Leucinski zatvarač ili leucinske makaze, leucinske škare, leucinski ziper[1] uobičajeni je trodimenzijskii strukturni motiv u proteinima. Prvo su ih opisali Landschulz et al., 1988.[2] kada su otkrili da vezni protein pojačivača ima vrlo karakterističan segment od 30 aminokiselina i obrazac ovih aminokiselinskih sekvenci na idealiziranom alfa-heliksu ispoljavajući periodično ponavljanje leucinskih ostataka na svakom sedmom položaju, na udaljenosti koja pokriva osam spiralnih zavoja. Predloženo je da polipeptidni segmenti koji sadrže ove periodične sekvence ostataka leucina postoje u alfa-heliksnoj konformaciji, a leucinski bočni lanci iz jednog alfa-heliksa se međusobno dijele s onima iz alfa-heliksa drugog polipeptida, olakšavajući dimerizaciju.
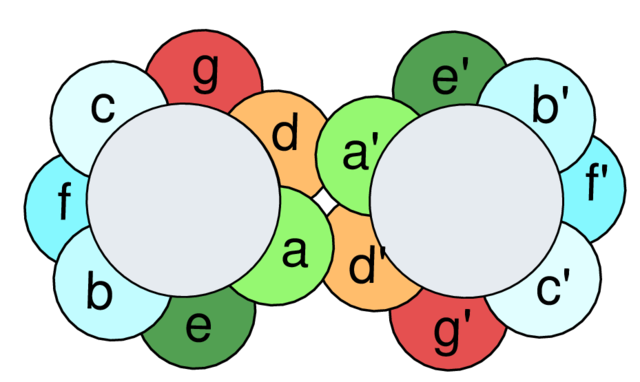
Motivi leucinskog zatvarača imaju dimerizacije klase bZIP (leucin zatvarač u baznoj regiji) eukariotski faktori transkripcije.[3] Dužina bZIP domena je 60 do 80 aminokiselina, s visoko konzerviranim DNK veznim osnovnim regionom i diverzifikovanijom regijom dimerizacije zatvarača.[4] Lokalizacija leucina je presudna za vezivanje DNK za proteine. Zatvarači s leucinom prisutni su i u eukariotskim i u prokariotskim regulatornim proteinima, ali su uglavnom svojstvo eukariota.
Oni se takođe mogu označiti jednostavno kao ZIP, a motivi slični ZIP-u pronađeni su u proteinima, osim faktora transkripcije, a smatra se da su jedan od općih proteinskih modula za interakcije protein-protein.[5]