Loading AI tools
একটি মৌলিক পদার্থ উইকিপিডিয়া থেকে, বিনামূল্যে একটি বিশ্বকোষ
অ্যান্টিমনি হল একটি মৌলিক পদার্থ, এর প্রতীক Sb, (লাতিন: স্টিবিয়াম) এবং পারমাণবিক সংখ্যা ৫১। এটি একটি চকচকে ধূসর ধাতুকল্প, এটি প্রকৃতিতে মূলত সালফাইড খনিজ স্টিবনেট হিসাবে পাওয়া যায় (Sb2S3)। অ্যান্টিমনি যৌগগুলি প্রাচীন কাল থেকেই পরিচিত ছিল এবং গুঁড়ো করে চিকিৎসাক্ষেত্রে ও প্রসাধনীতে ব্যবহার হত, এটিকে প্রায়শই আরবি কাজল নামে ডাকা হত।[1] ধাতব অ্যান্টিমনির কথাও জানা ছিল, তবে এটি আবিষ্কারের পরে এটিকে ভুল করে সীসা হিসাবে চিহ্নিত করা হয়েছিল। ১৫৪০ সালে, পশ্চিম ভূভাগে সর্বপ্রথম ধাতবটির বিবরণ পাওয়া গিয়েছিল ভ্যানোচিও বিরিঙ্গুচিওর লিখিত বিবরণীতে।
| |||||||||||||||||||||||||
| সাধারণ বৈশিষ্ট্য | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| নাম, প্রতীক, পারমাণবিক সংখ্যা | অ্যান্টিমনি, Sb, ৫১ | ||||||||||||||||||||||||
| রাসায়নিক শ্রেণী | ধাতুকল্প | ||||||||||||||||||||||||
| গ্রুপ, পর্যায়, ব্লক | ১৫, ৫, পি | ||||||||||||||||||||||||
| ভৌত রূপ | চকচকে ধূসর রুপোলি চিত্র:Sb,৫১.jpg | ||||||||||||||||||||||||
| পারমাণবিক ভর | ১২১.৭৬০(1) g/mol | ||||||||||||||||||||||||
| ইলেক্ট্রন বিন্যাস | [Kr] ৪ডি১০ ৫এস২ ৫পি৩ | ||||||||||||||||||||||||
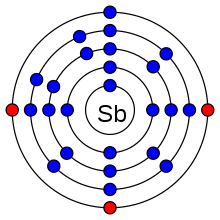
| প্রতি শক্তিস্তরে ইলেকট্রন সংখ্যা | ২, ৮, ১৮, ১৮, ৫ | ||||||||||||||||||||||||
| ভৌত বৈশিষ্ট্য | |||||||||||||||||||||||||
| দশা | কঠিন | ||||||||||||||||||||||||
| ঘনত্ব (সাধারণ তাপ ও চাপে) | ৬.৬৯৭ g/cm³ | ||||||||||||||||||||||||
| গলনাংকে তরল ঘনত্ব | ৬.৫৩ গ্রাম/সেমি³ | ||||||||||||||||||||||||
| গলনাঙ্ক | ৯০৩.৭৮ K (৬৩০.৬৩ °C, ১১৬৭.১৩ °F) | ||||||||||||||||||||||||
| স্ফুটনাঙ্ক | ১৮৬০ K (১৮৫৭ °C, ২৮৮৯ °F) | ||||||||||||||||||||||||
| গলনের লীন তাপ | ১৯.৭৯ kJ/mol | ||||||||||||||||||||||||
| বাষ্পীভবনের লীন তাপ | ১৯৩.৪৩ kJ/mol | ||||||||||||||||||||||||
| তাপধারণ ক্ষমতা | (২৫ °সে) ২৫.২৩ জুল/(মোল·কে) | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| পারমাণবিক বৈশিষ্ট্য | |||||||||||||||||||||||||
| কেলাসীয় গঠন | রম্বোহেড্রাল | ||||||||||||||||||||||||
| জারণ অবস্থা | −৩, ৩, ৫ | ||||||||||||||||||||||||
| তড়িৎ ঋণাত্মকতা | ২.০৫ (পাউলিং স্কেল) | ||||||||||||||||||||||||
| আয়নীকরণ শক্তি (বিস্তারিত) |
প্রথম: ৮৩৪ কিলোজুল/মোল | ||||||||||||||||||||||||
| দ্বিতীয়: ১৫৯৪.৯ কিলোজুল/মোল | |||||||||||||||||||||||||
| তৃতীয়: ২৪৪০ কিলোজুল/মোল | |||||||||||||||||||||||||
| পারমাণবিক ব্যাসার্ধ | ১৪৫ pm | ||||||||||||||||||||||||
| Atomic radius (calc.) | ১৩৩ pm | ||||||||||||||||||||||||
| Covalent radius | ১৩৮ pm | ||||||||||||||||||||||||
| অন্যান্য বৈশিষ্ট্য | |||||||||||||||||||||||||
| Magnetic ordering | কোন তথ্য নেই | ||||||||||||||||||||||||
| Electrical resistivity | (20 °C) ৪১৭ nΩ·m | ||||||||||||||||||||||||
| তাপ পরিবাহিতা | (300 K) ২৪.৪ W/(m·K) | ||||||||||||||||||||||||
| Thermal expansion | (25 °C) ১১.০ µm/(m·K) | ||||||||||||||||||||||||
| Speed of sound (thin rod) | (20 °C) ৩৪২০ m/s | ||||||||||||||||||||||||
| ইয়ং এর গুণাঙ্ক | ৫৫ GPa | ||||||||||||||||||||||||
| Shear modulus | ২০ GPa | ||||||||||||||||||||||||
| Bulk modulus | ৪২ GPa | ||||||||||||||||||||||||
| Mohs hardness | ৩.০ | ||||||||||||||||||||||||
| Brinell hardness | ২৯৪ MPa | ||||||||||||||||||||||||
| সি এ এস নিবন্ধন সংখ্যা | ৭৪৪০-৩৬-০ | ||||||||||||||||||||||||
| কয়েকটি উল্লেখযোগ্য সমস্থানিক | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| References | |||||||||||||||||||||||||

বেশ কিছু সময় ধরে, এন্টিমনি এবং এর যৌগগুলির বৃহত্তম উৎপাদক ছিল চীন, এর বেশি অংশটাই আসত হুনান প্রদেশের জিকুয়াংশান খনি থেকে। অ্যান্টিমনি পরিশোধন করার শিল্প পদ্ধতিগুলি হল সেটিকে ঝলসানো এবং কার্বন দিয়ে বিজারণ বা লোহার সাথে স্টিবনেটের সরাসরি বিজারণ।
ধাতব অ্যান্টিমনির বৃহত্তম উপযোগিতা হল সীসা এবং টিনের সঙ্গে মিশ্র ধাতু তৈরি এবং সীসা – অ্যাসিড ব্যাটারিতে (লেড – অ্যাসিড ব্যাটারি) সীসা অ্যান্টিমনির পাতের ব্যবহার। অ্যান্টিমনি সহ সীসা এবং টিনের মিশ্রধাতু ব্যবহার করে সোল্ডার, গুলি এবং প্লেইন বিয়ারিং এর বৈশিষ্ট্যগুলি উন্নত হয়েছে। অ্যান্টিমনি যৌগগুলি বহু বাণিজ্যিক এবং গার্হস্থ্য পণ্যগুলিতে পাওয়া ক্লোরিন এবং ব্রোমিনযুক্ত অগ্নি প্রতিরোধকারী যন্ত্রের বিশিষ্ট সংযোজন। আধুনিক কালে অণু-ইলেকট্রন বিজ্ঞানে অ্যান্টিমনির ব্যবহার ক্রমবর্ধমান।এর একটি বিশেষ বৈশিষ্ট্য হচ্ছে, এই ধাতুর উপর আঘাত করলে শব্দ হয় না।
অ্যান্টিমনি পর্যায় সারণীর গ্রুপ ১৫র সদস্য, নিকটোজেন নামে পরিচিত উপাদানগুলির মধ্যে একটি, এবং এর তড়িৎ ঋণাত্মকতা ২.০৫। পর্যায়ক্রমিক প্রবণতা অনুসারে, এটি টিন বা বিসমাথের চেয়ে বেশি তড়িৎ ঋণাত্মক, এবং টেলুরিয়াম বা আর্সেনিকের চেয়ে কম তড়িৎ ঋণাত্মক। অ্যান্টিমনি ঘরের তাপমাত্রায় বাতাসে স্থিতিশীল, তবে উত্তপ্ত করলে অক্সিজেনের সাথে বিক্রিয়া করে অ্যান্টিমনি ট্রাই অক্সাইড উৎপাদন করে, Sb২O৩।[2]:৭৫৮
অ্যান্টিমনি হল একটি রুপোলি, চকচকে ধূসর ধাতুকল্প, এর কাঠিন্য মাত্রা ৩, তাই এটি দিয়ে শক্ত বস্তু তৈরি করা যায়না; ১৯৩১ সালে চীনের কুইচৌ প্রদেশে অ্যান্টিমনির মুদ্রা চালু করা হয়েছিল কিন্তু এর স্থায়িত্ব খুব কম ছিল এবং তাই এর উৎপাদন বন্ধ করে দেওয়া হয়।[3] অ্যান্টিমনি, অ্যাসিড দ্বারা ক্ষয় প্রতিরোধী। অ্যান্টিমনি চারটি বহুরূপতা আছে: একটি স্থিতিশীল ধাতব রূপ এবং তিনটি প্রায় স্থিতিশীল রূপ (মেটাস্টেবল) (বিস্ফোরক, কালো এবং হলুদ)। অ্যান্টিমনি হল একটি ভঙ্গুর, রৌপ্য-সাদা চকচকে ধাতুকল্প। ধীরে ধীরে ঠান্ডা করলে, গলিত অ্যান্টিমনি ত্রিমাত্রিক কোষে কেলাসিত হয়, যেটি আর্সেনিকের ধূসর বহুরূপতার (অ্যালোট্রপি) সম কেলাসিত গঠনের মতই। অ্যান্টিমনি ট্রাইক্লোরাইডের তড়িৎ বিশ্লেষণ করলে অ্যান্টিমনি বিরল বিস্ফোরক রূপ পাওয়া যায়। কোন তীক্ষ্ণ বস্তু দিয়ে আঁচড়ালে, একটি তাপমোচী বিক্রিয়া হয় এবং সাদা ধোঁয়া মুক্ত করে ধাতব অ্যান্টিমনি তৈরি হয়; যখন নুড়ি দিয়ে খলে ঘষা হয়, একটি শক্তিশালী বিস্ফোরণ ঘটে। অ্যান্টিমনি বাষ্পকে দ্রুত শীতল করলে কালো অ্যান্টিমনি তৈরি হয়। এটির কেলাসের গঠন লাল ফসফরাস এবং কালো আর্সেনিকের মতো, এটি বাতাসে জারিত হয় এবং স্বতঃস্ফূর্তভাবে জ্বলে উঠতে পারে। ১০০ °সেন্টিগ্রেড তাপমাত্রায়, এটি ধীরে ধীরে স্থিতিশীল রূপে রূপান্তরিত হয়। অ্যান্টিমনির হলুদ বহুরূপ সবচেয়ে অস্থিতিশীল। এটি কেবলমাত্র স্টিবাইনের জারণে উৎপন্ন হয় (SbH৩) −৯০ °সেন্টিগ্রেড তাপমাত্রায়। এই তাপমাত্রার উপরে এবং পারিপার্শ্বিক আলোতে, এই প্রায় স্থিতিশীল বহুরূপ আরও স্থিতিশীল কালো বহুরূপে রূপান্তরিত হয়।[4][5][6]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.