chemiese verbinding From Wikipedia, the free encyclopedia
Triptofaan (afgekort as Trp of W; gekodeer deur die kodon UGG) is 'n α-aminosuur wat gebruik word in die biosintese van proteïene. Dit bevat 'n α-aminogroep, 'n α-karboksielgroep, en 'n indoolsyketting, wat dit 'n nie-polêre aromatiese aminosuur maak. Dit is noodsaaklik in die mens, want die liggaam kan dit nie sintetiseer nie: dit moet uit die dieet verkry word. Triptofaan is ook 'n voorloper van die neurotransmitter serotonien en die hormoon melatonien.[1]
|
Algemeen | |
|---|---|
| Naam | Triptofaan |
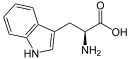
| IUSTC-naam | Triptofaan of (2S)-2-amino-3-(1H-indool-3-yl)propanoësuur |
 |
|
| Chemiese formule | C4H9O3N1 |
| Molêre massa | g/mol |
| CAS-nommer | 73-22-3 |
| Fasegedrag | |
| Smeltpunt | |
| Kookpunt | |
| Digtheid | |
| Oplosbaarheid | 0.23 g/L by 0 °C, 11.4 g/L by 25 °C, |
|
Suur-basis eienskappe | |
| pKa | |
|
Veiligheid | |
| Flitspunt | |
|
Tensy anders vermeld is alle data vir standaardtemperatuur en -druk toestande. | |
| Portaal | |
Soos ander aminosure is triptofaan 'n zwitterioon by fisiologiese pH: die aminogroep is geprotoneer (–NH3+; pKa = 9.39) en die karboksielgroep is gedeprotoneer ( –COO−; pKa = 2.38).[2]
Die isolering van triptofaan is vir die eerste keer deur Frederick Hopkins in 1901 berig.[3] Hopkins het triptofaan uit gehidroliseerde kaseïen herwin, en kon 4-8 g triptofaan uit 600 g ongeprosesseerde kaseïen verkry.[4]
As 'n noodsaaklike aminosuur, word triptofaan nie uit eenvoudiger stowwe by die mens en ander diere gesintetiseer nie, so dit moet teenwoordig wees in die dieet in die vorm van triptofaan-bevattende proteïene. Plante en mikro-organismes sintetiseer normaalweg triptofaan uit sjikimiensuur of antranilaat:[5] antranilaat kondenseer met fosforibosielpirofosfaat, met pirofosfaat as 'n neweproduk. Die ribosering word geopen en onderwerp aan reduktiewe dekarboksilering, en indool-3-gliserolfosfaat word gevorm; hierdie, op sy beurt, word in indool omgesit. In die laaste stap kataliseer triptofaansintase die vorming van triptofaan uit indool en die aminosuur serien.
Die industriële produksie van triptofaan is ook 'n biosintetiese, en is gebaseer op die fermentasie van serien en indool deur bakterieë soos B. amyloliquefaciens, B. subtilis, C. glutamicum of E. coli. Partykeer word geneties gemodifiseerde bakterië gebruik. Die bakterië wat gebruik word het almal mutasies die heropname van aromatiese aminosure verhoed, of wat veelvuldige of ooruitgedrukte trp operons het.[6][7][8]

Aminosure, insluitend triptofaan, is boustene vir proteïensintese, en proteïene is nodig om lewe te onderhou. Baie diere (insluitend die mens) kan nie triptofaan sintetiseer nie: hulle moet dit in hulle dieet kry, wat dit 'n noodsaaklike aminosuur maak. Triptofaan is een van die minder algemene aminosure in proteïene, maar dit speel 'n belangrike strukturele of funksionele rolle waar dit voorkom. Triptofaan- en tirosienresidue speel byvoorbeeld 'n spesiale rol in die "ankering" van membraanproteïene in die selmembraan. Daarbenewens funksioneer triptofaan as 'n biochemiese voorloper vir die volgende verbindings:
Fruktosewanabsorpsie veroorsaak onvoldoende absorpsie van triptofaan in die dunderm, verminderde vlakke van triptofaan in die bloed,[14] en depressie.[15]
In bakterieë wat triptofaan sintetiseer, aktiveer hoë sellulêre vlakke van die aminosuur 'n repressor proteïen, wat bind aan die trp operon.[16] Binding van hierdie repressor aan die triptofaanoperon verhoed transkripsie van die stroomaf DNA wat kodeer vir die ensieme wat betrokke is by die biosintese van triptofaan. Hoë vlakke van triptofaan voorkom dus triptofaansintese deur middel van 'n negatiewe terugvoer lus, en wanneer die sel se triptofaan vlakke weer afneem, word transkripsie van die tvp operon hervat. Hierdie meganisme laat streng gereguleerde en vinnige reaksie op veranderinge in die sel se interne en eksterne triptofaanvlakke toe.
Triptofaanmetabolisme deur menslike mikrobiota
|
In 2002 het die Amerikaanse Instituut van Medisyne 'n Aanbevole Dieettoelaag (ADT) van 5 mg/kg liggaamsmassa/dag van triptofaan vir volwassenes 19 jaar en ouer voorgestel.[21]
Triptofaan is teenwoordig in die meeste proteïen-gebaseerde voedsel. Dit is veral volop in sjokolade, hawer, gedroogde dadels, melk, jogurt, maaskaas, rooi vleis, eiers, vis, pluimvee, sesam, kekerertjies, amandels, sonneblomsade, pampoenpitte, bokwiet, spirulina, en grondboontjies. In teenstelling met die algemene opvatting[22] dat kalkoenvleis baie triptofaan bevat, is die triptofaaninhoud in kalkoen tipies van pluimvee.[23]
| voedsel | Triptofaan [g/100 g voedsel] |
Proteïen [g/100 g voedsel] |
Triptofaan/Proteïen [%] |
|---|---|---|---|
| eierwit, gedroog | |||
| spirulina, gedroog | |||
| kabeljou, atlanties, gedroog | |||
| sojabone, rou | |||
| kaas, Parmesaan | |||
| sesamsaad | |||
| kaas, cheddar | |||
| sonneblomsaad | |||
| varkvleis, tjop | |||
| Kalkoenvleis | |||
| hoendervleis | |||
| beesvleis | |||
| hawer | |||
| salm | |||
| lam, tjop | |||
| baars, Atlantiese oseaan | |||
| kekerertjies, rou | |||
| eier | |||
| koring meel, wit | |||
| bak sjokolade, onversoet | |||
| melk | |||
| rys, wit, medium-graan, gaar | |||
| quinoa, rou | |||
| quinoa, gaar | |||
| aartappels, rooibruin | |||
| tamarinde | |||
| piesang |
'n Algemene opvatting in die VSA is dat lomerigheid by inname van te veel kalkoenvleis met hoë vlakke van triptofaan in kalkoen verbind kan word.[25][26] Die hoeveelheid triptofaan in kalkoenlveis is egter vergelykbaar met dié van ander vleis. Lomerigheid na ete kan veroorsaak word deur ander voedsel wat saam met die kalkoen geëet word, veral koolhidrate.[27] Na 'n maaltyd wat ryk aan koolhidrate is, word insulien vrygestel.[28][29][30] Insulien stimuleer op sy beurt die inname van groot neutrale vertakte syketting aminosure, maar nie triptofaan nie, deur spierweefsel, wat daartoe lei dat die verhouding van triptofaan tot vertakte aminosure in die bloedstroom verhoog word. Die gevolglike verhoogde triptofaan verhouding verminder kompetisie by die groot neutrale aminosuur transportproteïen wat aminosure met vertakte en aromatiese sykettings oor membrane skuif, veral in die kapillêre bloedvate van die bloed–brein skans, sodat meer triptofaan oorgedra word in die serebrospinale vog.[31][32] Sodra dit in die serebrospinale vog is, word triptofaan in die raphe kerne deur die normale ensiematiese pad in serotonien omgesit,[33] wat verder in die pineaalklier in melatonien omgesit word. Na-ete lomerigheid kan dus die gevolg wees van 'n swaar maaltyd ryk aan koolhidrate en proteïen, wat indirek die produksie van melatonien in die brein verhoog, en daardeur slaap bevorder.
Omdat triptofaan omgeskep word in 5-hidroskitriptofaan (5-HTP) wat dan omskep word in die neurotransmitter serotonien, is daar al voorgestel dat die gebruik van triptofaan of 5-HTP depressiesimptome kan verlig deur die vlak van serotonien in die brein te verhoog. Triptofaan word oor die toonbank in die Verenigde State van Amerika verkoop, nadat dit tussen 1989 en 2005 meer of minder sterk gekontroleer is, en in die Verenigde Koninkryk as 'n dieetaanvulling met die veronderstelling dat dit as 'n antidepressant, angswerende middel, of slaapmiddel sou werk. Dit is ook in beskikbaar in sommige Europese lande as 'n voorskrifmedikasie vir die behandeling van depressie. Alhoewel bloedvlakke van triptofaan waarskynlik nie verander word deur die veranderings in die dieet nie,[34][35] maar inname van suiwer triptofaan verhoog die vlak van serotonien in die brein.[36] Dit is omdat die stelsel wat triptofaan oor die bloed-brein skans vervoer, ook ander aminosure vervoer wat in voedsel voorkom. Hoë bloedplasmavlakke van ander groot neutrale aminosure verhoed dat die plasmakonsentrasie van triptofaan bydra tot die verhoging van die triptofaankonsentrasie in die brein.[37]
In 2001 is 'n Cochrane Reviews artikel gepubliseer oor die effek van 5-HTP en triptofaan op depressie. Slegs hoë kwaliteit studies op 5-HTP en triptofaan is ingesluit. Van die 108 studies wat tussen 1966 en 2000 gepubliseer is, het net twee voldoen aan die kwaliteitstandaarde vir insluiting, met 'n totaal van 64 mense wat deelgeneem het. Die stowwe was meer effektief as plasebo, maar die skrywers se opsomming was dat die getuienis onvoldoende was op 'n sterk gevolgtrekking te maak, en dat ander antidepressante bestaan wat doeltreffend en veilig is, wat die kliniese nut van 5-HTP en triptofaan beperk.[38] Die gebruik van triptofaan as 'n bykomende terapie tot die standaardbehandeling vir gemoed- en angsversteurings word tans nie ondersteun nie.[39]
Moontlike newe-effekte van triptofaan sluit in naarheid, diarree, lomerigheid, lighoofdigheid, hoofpyn, droë mond, versteurde visie, verdowing, euforie, en nystagmus (onwillekeurige oogbewegings).[40][41]
Omdat triptofaan nog nie deeglik bestudeer is in 'n kliniese omgewing nie, is sy interaksies met ander middels nog nie goed bekend nie. Wanneer triptofaan geneem word as 'n dieet aanvulling, het dit die potensiaal om serotoniensindroom te veroorsaak wanneer dit gekombineer word met antidepressante van die MAOI of SSRI klasse of met ander sterk serotonergiese middels.
In 1912 het Felix Ehrlich getoon dat gis die natuurlike aminosure in wese aanval deur koolstofdioksied af te splyt, en die amino groep met hidroksiel te vervang. Deur hierdie reaksie word triptofaan in triptofol omgeskakel.[42]
Triptofaan beïnvloed serotoniensintese in die brein wanneer mondelings in 'n gesuiwerde vorm toegedien word, en word dus gebruik om serotonienvlakke vir navorsingsdoeleindes te verander. Lae serotonienvlakke in die brein kan veroorsaak word deur lae-triptofaan diete.[43] Studies wat hierdie metode gebruik het, het bevind dat serotonien aggressie verminder en welgevalligheid verhoog.[44]
Triptofaan is 'n belangrike intrinsieke fluoressensie-peiler, wat gebruik kan word om die aard van die mikro-omgewing rondom die triptofaanresidu te bepaal. Meeste van die intrinsieke fluoressensie van 'n gevoude proteïen is as gevolg van triptofaan residue.
Daar was 'n groot uitbraak van eosinofilie-mialgie sindroom in die VSA in 1989, met meer as 1500 gevalle wat aan die CDC gerapporteer is en ten minste 37 sterftes.[45] Na die voorlopige ondersoek aan die lig gebring het dat die uitbraak aan triptofaan gekoppel kan wees, het die Food and Drug Administration (FDA) triptofaan-dieetaanvullings in 1989 teruggeroep en meeste verkope aan die publiek in 1990 verbied:[46][47] ander lande het hierdie voorbeeld gevolg.[48][49]
Die daaropvolgende epidemiologiese studies het die sindroom gekoppel aan spesifieke lotte van L-triptofaan wat deur 'n enkele groot Japannese vervaardiger, Showa Denko, afkomstig was.[50][51][52] Dit het uiteindelik duidelik geword dat die lotte besmet is deur spoor onsuiwerhede, wat verdink is om verantwoordelik te wees vir die 1989 uitbraak.[53][54] Daar is egter ook getuienis daarvoor dat triptofaan self 'n belangrike bydraende faktor in die sindroom kan wees.[55]
Die FDA het sy beperkinge op die verkope en bemarking van triptofaan in Februarie 2001 gedeeltelik gelig, maar het voortgegaan om die invoer van triptofaan wat nie vir 'n gemagtige gebruik bestemis, tot en met 2005 te beperk.[56]
Die feit dat die Showa Denko fasiliteit geneties gemanipuleerde bakterieë gebruik het om die besmette lotte van L-triptofaan te produseer is aangehaal as stawing vir noue monitering van die chemiese suiwerheid van produkte wat van biotegnologie afkomstig is.[57] Die fokus op hierdie aspek deur teenstaanders van genetiese manipulasie is ook gekritiseer, omdat die genetiese manipulasie nie die oorsaak van die kontaminasie was nie.[58]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.