Loading AI tools
来自维基百科,自由的百科全书
立体中心是分子的立體異構焦點,該焦點可以是原子(中心)、軸或平面;也就是說,當至少三個不同的基團與立體中心結合時,交換任意兩個不同的基團會產生一個新的立體異構體。[1][2]

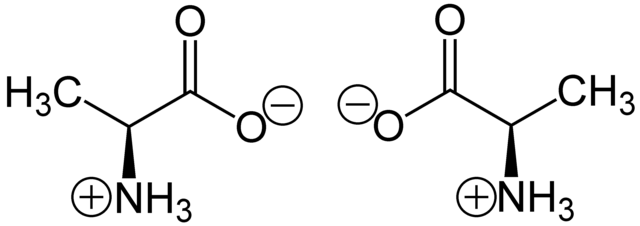
立體中心在幾何上被定義為分子中的一個點(位置);立體中心通常但不總是一個特定的原子(通常是碳)。[2][3]立體中心可以存在於手性或非手性分子上;立體中心可以包含單鍵或雙鍵。[1] 立體異構體的預設數量為 2n ,其中 n 是四面體立體中心的數量;然而,內消旋化合物等例外情況會使立體異構體的實際數量降低到 2n 以下。[4]
立体中心一词是Mislow和Siegel于1984年最早使用的。[5]
手性中心則是一種具有四個不同取代基的立體中心;手性中心是立體中心的一個特定子集,因為它們只能有 sp3 雜化,這意味著它們只能有單鍵。[6]
手性中心是立體中心的一種。手性中心定義為在其鏡像上不可疊加的空間排列中包含一組四個不同配體(原子或原子團)的原子。手性中心必須是 sp3 雜化的,這意味著手性中心只能有單鍵。[6]在有機化學中,手性中心通常指碳、磷或硫原子,但其他原子也可能是手性中心,特別是在有機金屬和無機化學領域。
按照国际纯粹与应用化学联合会的定义,手性中心是“不对称碳原子”概念的拓展。不对称碳原子指的是连有四个不同的基团的碳原子,交换连在该原子上的两个基团的位置会得到原化合物的立体异构体。手性中心的概念則將該概念由碳擴展至任何原子,具有四個不同連接基團的任何原子,若其中任何兩個連接基團的交換能產生對映異構體,則該原子為分子的手性中心。[7]
一个分子可以同时具有多个立体中心,因而具有多个立体异构体。若一个化合物的立体异构体全部由于立體中心产生,且所有的立體中心都以四面体的立体结构成键,则该化合物的立体异构体的理论数目不会超过2n,其中n是手性中心的总数。若分子有一定的对称性,则分子的立体异构体数目一定小于这个值。
两个手性中心连接的基团相同且位置上具有对称性时,会得到非手性的内消旋化合物 。由于位阻的原因,部分构型可能不能存在。环状化合物即使具有手性中心,由于二重轴的存在,也可能不显示手性。手性化合物也不一定具有手性中心,例如在平面手性和轴手性的情形。
“手性碳”或“不对称碳”指的是具有不对称型的碳原子,通常用C*表示。
一个碳原子要成为手性碳需满足两个条件:该碳原子必须是sp3-杂化,且连有四个不同的基团。
碳原子的其它成键方式都会在分子中形成对称从而不具有手性。如, sp 或 sp2杂化的碳原子会使分子该部分呈平面型,因而具有对称面。碳原子上连有两个相同基团时,两基团与碳原子所成夹角的角平分面会成为对称面。
碳原子在有机化学中的普遍性使得其成为最重要的手性中心,不过手性中心并不限于碳原子,三价氮原子和磷原子的成键也具有四面体的特点。当瓦尔登翻转引起的构型转换受限时,或在形成季铵盐和鏻盐时,手性就有可能出现。
在配合物中,具有四面体构型与八面体构型的中心金属原子也可能成为手性中心。 对于八面体构型来说,有多种可能的情况。若手性中心只與兩種配體配合,而各種配體的數量均是三個,同一種配體沿中線(meridian)排列時,就會給出mer-異構體;同一種配體形成一個面(face)時,就會給出fac-異構體。此外,有三个双齿配体时,就有一对对映异构体,用标记 Λ 和 Δ 表示。
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.