Loading AI tools
取代反應(英語:Substitution reaction)是一種重要的有機化學反應,其定義是分子中的一個原子或原子團被其他原子或原子團取代。[1][2]而取代反應主要依照反應中所使用的試劑分為親核取代反應與親電取代反應兩大類,但也有不屬於前面兩種類型的取代反應,將會在下文提及。
有機的取代反應會依以下的特點,被歸類到若干個有機取代反應類別中:
詳細了解取代反應的類別不但對預測產物很有幫助,而且還可以利用控制溫度或調整所使用的溶劑等反應條件的調控方式來增快反應速率或提升反應的產率。
鹵化反應就是取代反應的一個例子。這裡以甲烷的氯代反應為例:當部分氯氣分子(Cl-Cl)受到輻射照射即分解產生氯自由基(Cl.),此時氯自由基上的不成對電子具有高度親核性,它將攻擊甲烷上的其中一個氫質子、打斷C-H共價鍵並形成穩定的氯化氫分子,而另一個氯自由基則跟CH3.形成鍵結產生氯甲烷。[3]

親核取代反應
親核取代反應是取代反應的一種基本型式,指親核基與帶正電或部分正電的原子或原子團反應並取代它。被取代的原子或原子團稱為離去基;帶正電的原子或原子團為親電子基;帶有離去基和親電子基的整個原始分子則稱為受質。[4][5]
親核取代反應的通式如下:
- Nuc: + R-LG → R-Nuc + LG:
親核基利用電子對(:)攻擊受質(R-LG)形成一個新的鍵結,同時受質上的離去基(LG:)鍵結被打斷並離去,反應結束,得到此反應的主要產物(R-Nuc)。親核基可以是電中性或帶負電荷,受質上的親電子基則通常為電中性或帶有正電荷。
親核取代反應可以根據反應的速控步涉及到幾個分子的化學變化分為單分子親核取代反應(SN1)與雙分子親核取代反應(SN2)。以下將簡略說明。
雙分子親核取代反應(SN2反應),親核取代反應的一種。反應過程為親核基直接攻擊中心碳原子形成鍵結,幾乎同時離去基與中心碳原子鍵結斷裂並離去,其過渡態是一個碳五鍵的分子,如下圖。此反應為一步反應,所以此步驟也是這個反應的速控步,而兩種反應物-親核試劑和受質-都參與這個步驟,所以此反應為雙分子反應。

單分子親核取代反應(SN1反應),另一種親核取代反應。反應過程分為兩個步驟:首先離去基與中心碳原子之間的化學鍵斷裂,產生一個碳陽離子中間產物,第二步驟為親核基與碳陽離子形成新的鍵結,如下圖。這個反應的第一步驟「形成碳陽離子中間體」為速控步,因為只牽涉到一個分子(受質上的離去基)所以反應為單分子反應。[6]

親電取代反應
另一種取代反應的基本形式為親電取代反應,是親電試劑取代親核基上某原子或原子團的反應,被取代的原子通常是氫原子,但也可以是其他原子。親電取代反應依照親核基為芳香類化合物或脂肪類化合物分為兩類。
對芳香類化合物的親電取代反應稱為親電芳香取代反應,其中包括對芳香類化合物的硝化反應、鹵代反應、磺化反應以及傅-克反應等。

而對脂肪類化合物的親電取代反應與上述親核取代反應很類似,也分為SE1與SE反應。在SE1反應中,分為兩步驟,受質先游離形成碳陰離子與帶正電的有機殘基,碳陰離子迅速與親電試劑結合,完成取代反應。SE2的反應機構則是只有一個過渡態,舊鍵結的斷裂與形成新鍵結幾乎同時發生。[7] 脂肪族的親電取代反應有:
自由基取代反應
在有機反應的分類上,若反應中的活性中間體為自由基則稱為自由基反應。而涉及到自由基的取代反應則稱為自由基取代反應,例如以質子取代羥基的Barton–McCombie去氧反應或是像沃爾–齊格勒溴化反應對烯丙位的溴化反應等等。[8][9]
取代化合物
取代化合物[10]指的是某核心結構化合物上的氫原子被烴基、羥基或鹵素等等的取代基取代。
舉例來說,苯是最簡單的芳香環,而苯上的氫原子可以被各種原子或原子團取代後就成了各式各樣的化合物:
| 幾種簡單的苯取代化合物 | ||
| 化合物 | 分子式 | 結構式 |
| 苯 | C6H6 | 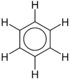 |
| 甲苯 | C6H5-CH3 | |
| 鄰二甲苯 | C6H4(-CH3)2 | 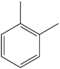 |
| 均三甲苯 | C6H3(-CH3)3 |  |
| 苯酚 | C6H5-OH | 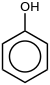 |
參見
參考資料
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.