User:Merphisto/沙盒3
維基百科,自由的 encyclopedia
酸解离常数,Ka,(也称为酸度系数,或酸电离系数)是一种衡量酸在溶液中强度的一种定量。它是酸-碱反应中解离化学反应中的平衡常数。其平衡可写为:
- HA ⇌ A− + H+,

其中HA代表酸解离出了质子或氢离子后形成A−,即酸的共轭碱。而产生的氢离子若是在水溶液中这是以水合氢离子形式存在。如图片所示,HA代表乙酸,A−代表乙酸根离子。三个化学物种HA和A−以及H+在达到化学平衡时,它们浓度保持不变。解离常数通常表示为它们各平衡浓度的商,即[HA],[A−]与[H+]的商:
由于Ka值之间都相差许个数量级,因此酸解离常数在实际使用中通常使用对数来进行衡量,也就是其对数常数:pKa,等于−log10 Ka,通常的酸解离常数为:
pKa的值越大,其解离的能力越小。通常弱酸在水中的pKa值在-2至12之间。当酸的pKa值小于-2则可称为强酸;强酸在水溶液中可几乎发生完全电离,因此其没有电离的酸分子浓度变得无法测量。因此强酸的pKa值可通过其在非水溶剂当中的电离常数通过理论推测出,因强酸在非水溶剂中的解离常数会降低,如乙腈或二甲亚砜。
理论背景
The acid dissociation constant for an acid is a direct consequence of the underlying thermodynamics of the dissociation reaction; the pKa value is directly proportional to the standard Gibbs energy change for the reaction. The value of the pKa changes with temperature and can be understood qualitatively based on Le Chatelier's principle: when the reaction is endothermic, the pKa decreases with increasing temperature; the opposite is true for exothermic reactions. The underlying structural factors that influence the magnitude of the acid dissociation constant include Pauling's rules for acidity constants, inductive effects, mesomeric effects, and hydrogen bonding.
The quantitative behaviour of acids and bases in solution can be understood only if their pKa values are known. In particular, the pH of a solution can be predicted when the analytical concentration and pKa values of all acids and bases are known; conversely, it is possible to calculate the equilibrium concentration of the acids and bases in solution when the pH is known. These calculations find application in many different areas of chemistry, biology, medicine, and geology. For example, many compounds used for medication are weak acids or bases, and a knowledge of the pKa values, together with the water–octanol partition coefficient, can be used for estimating the extent to which the compound enters the blood stream. Acid dissociation constants are also essential in aquatic chemistry and chemical oceanography, where the acidity of water plays a fundamental role. In living organisms, acid-base homeostasis and enzyme kinetics are dependent on the pKa values of the many acids and bases present in the cell and in the body. In chemistry, a knowledge of pKa values is necessary for the preparation of buffer solutions and is also a prerequisite for a quantitative understanding of the interaction between acids or bases and metal ions to form complexes. Experimentally, pKa values can be determined by potentiometric (pH) titration, but for values of pKa less than about 2 or more than about 11, spectrophotometric or NMR measurements may be required due to practical difficulties with pH measurements.
定义
按照酸-碱理论#阿伦尼乌斯的定义中的原始定义,酸是水溶液中解离反应中的底物,释放出氢离子H+(一个质子):[1]
- HA ⇌ A− + H+.
其解离反应的平衡常数就是解离常数。游离的质子与水分子结合形成水合氢离子H3O+,因此阿伦尼乌斯后期被修正为一种酸碱反应:
- HA + H2O ⇌ A− + H3O+
Brønsted and Lowry总结之后衍生出了质子交换反应:[2][3][4]
- 酸 + 碱 ⇌ 共轭碱 + 共轭酸
The acid loses a proton, leaving a conjugate base; the proton is transferred to the base, creating a conjugate acid. For aqueous solutions of an acid HA, the base is water; the conjugate base is A− and the conjugate acid is the hydronium ion. The Brønsted–Lowry definition applies to other solvents, such as dimethyl sulfoxide: the solvent S acts as a base, accepting a proton and forming the conjugate acid SH+.
In solution chemistry, it is common to use H+ as an abbreviation for the solvated hydrogen ion, regardless of the solvent. In aqueous solution H+ denotes a solvated hydronium ion rather than a proton.[5][6]
The designation of an acid or base as "conjugate" depends on the context. The conjugate acid BH+ of a base B dissociates according to
- BH+ + OH− ⇌ B + H2O
which is the reverse of the equilibrium
- H2O (acid) + B (base) ⇌ OH− (conjugate base) + BH+ (conjugate acid).
The hydroxide ion OH−, a well known base, is here acting as the conjugate base of the acid water. Acids and bases are thus regarded simply as donors and acceptors of protons respectively.
A broader definition of acid dissociation includes hydrolysis, in which protons are produced by the splitting of water molecules. For example, boric acid (B(OH)3) produces H3O+ as if it were a proton donor,[7] but it has been confirmed by Raman spectroscopy that this is due to the hydrolysis equilibrium:[8]
- B(OH)3 + 2 H2O ⇌ B(OH)4− + H3O+.
Similarly, metal ion hydrolysis causes ions such as [Al(H2O)6]3+ to behave as weak acids:[9]
- [Al(H2O)6]3+ +H2O ⇌ [Al(H2O)5(OH)]2+ + H3O+.
平衡常数
酸的解离常数是平衡常数的一种特例。即是在单质子酸,HA和其共轭碱A−,在水中的一种特殊平衡。
- HA + H2O ⇌ A− + H3O+
热力学平衡常数K![]() 可通过定义[10]
可通过定义[10]
这里{A}是化学物种A的活度。K![]()
where {A} is the activity of the chemical species A etc. K![]() is dimensionless since activity is dimensionless. Activities of the products of dissociation are placed in the numerator, activities of the reactants are placed in the denominator. See activity coefficient for a derivation of this expression.
is dimensionless since activity is dimensionless. Activities of the products of dissociation are placed in the numerator, activities of the reactants are placed in the denominator. See activity coefficient for a derivation of this expression.

Since activity is the product of concentration and activity coefficient (γ) the definition could also be written as
where [HA] represents the concentration of HA and Γ is a quotient of activity coefficients.
To avoid the complications involved in using activities, dissociation constants are determined, where possible, in a medium of high ionic strength, that is, under conditions in which Γ can be assumed to be always constant.[10] For example, the medium might be a solution of 0.1 M sodium nitrate or 3 M potassium perchlorate (1 M = 1 mol·dm−3, a unit of molar concentration). Furthermore, in all but the most concentrated solutions it can be assumed that the concentration of water, [H2O], is constant, approximately 55 mol·dm−3. On dividing K![]() by the constant terms and writing [H+] for the concentration of the hydronium ion the expression
by the constant terms and writing [H+] for the concentration of the hydronium ion the expression
is obtained. This is the definition in common use.[11] pKa is defined as −log10 Ka. Note, however, that all published dissociation constant values refer to the specific ionic medium used in their determination and that different values are obtained with different conditions, as shown for acetic acid in the illustration above. When published constants refer to an ionic strength other than the one required for a particular application, they may be adjusted by means of specific ion theory (SIT) and other theories.[12]
Although Ka appears to have the dimension of concentration it must in fact be dimensionless or it would not be possible to take its logarithm. The illusion is the result of omitting the constant term [H2O] from the defining expression. Nevertheless it is not unusual, particularly in texts relating to biochemical equilibria, to see a value quoted with a dimension as, for example, "Ka = 300 M".
单质子酸
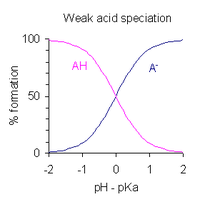
After rearranging the expression defining Ka, and putting pH = −log10[H+], one obtains
This is a form of the Henderson–Hasselbalch equation, from which the following conclusions can be drawn.
- At half-neutralization [A−]/[HA] = 1; since log(1) =0, the pH at half-neutralization is numerically equal to pKa. Conversely, when pH = pKa, the concentration of HA is equal to the concentration of A−.
- The buffer region extends over the approximate range pKa ± 2, though buffering is weak outside the range pKa ± 1. At pKa ± 1, [A−]/[HA] = 10 or 1/10.
- If the pH is known, the ratio may be calculated. This ratio is independent of the analytical concentration of the acid.
In water, measurable pKa values range from about −2 for a strong acid to about 12 for a very weak acid (or strong base). All acids with a pKa value of less than −2 are more than 99% dissociated at pH 0 (1 M acid). This is known as solvent leveling since all such acids are brought to the same level of being strong acids, regardless of their pKa values. Likewise, all bases with a pKa value larger than the upper limit are more than 99% protonated at all attainable pH values and are classified as strong bases.[3]
An example of a strong acid is hydrochloric acid, HCl, which has a pKa value, estimated from thermodynamic quantities, of −9.3 in water.[13] The concentration of undissociated acid in a 1 mol·dm−3 solution will be less than 0.01% of the concentrations of the products of dissociation. Hydrochloric acid is said to be "fully dissociated" in aqueous solution because the amount of undissociated acid is imperceptible. When the pKa and analytical concentration of the acid are known, the extent of dissociation and pH of a solution of a monoprotic acid can be easily calculated using an ICE table.
A buffer solution of a desired pH can be prepared as a mixture of a weak acid and its conjugate base. In practice the mixture can be created by dissolving the acid in water, and adding the requisite amount of strong acid or base. The pKa of the acid must be less than two units different from the target pH.
多质子酸

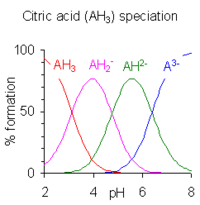
Polyprotic acids are acids that can lose more than one proton. The constant for dissociation of the first proton may be denoted as Ka1 and the constants for dissociation of successive protons as Ka2, etc. Phosphoric acid, H3PO4, is an example of a polyprotic acid as it can lose three protons.
| equilibrium | pKa value |
|---|---|
| H3PO4 ⇌ H2PO4− + H+ | pKa1 = 2.15 |
| H2PO4− ⇌ HPO42− + H+ | pKa2 = 7.20 |
| HPO42− ⇌ PO43− + H+ | pKa3 = 12.37 |
When the difference between successive pK values is about four or more, as in this example, each species may be considered as an acid in its own right;[14] In fact salts of H2PO4− may be crystallised from solution by adjustment of pH to about 5.5 and salts of HPO42− may be crystallised from solution by adjustment of pH to about 10. The species distribution diagram shows that the concentrations of the two ions are maximum at pH 5.5 and 10.
When the difference between successive pK values is less than about four there is overlap between the pH range of existence of the species in equilibrium. The smaller the difference, the more the overlap. The case of citric acid is shown at the right; solutions of citric acid are buffered over the whole range of pH 2.5 to 7.5.
In general, it is true that successive pK values increase (Pauling's first rule).[15] For example, for a diprotic acid, H2A, the two equilibria are
- H2A ⇌ HA− + H+
- HA− ⇌ A2− + H+
it can be seen that the second proton is removed from a negatively charged species. Since the proton carries a positive charge extra work is needed to remove it; that is the cause of the trend noted above. Phosphoric acid values (above) illustrate this rule, as do the values for vanadic acid, H3VO4. When an exception to the rule is found it indicates that a major change in structure is occurring. In the case of VO2+ (aq), the vanadium is octahedral, 6-coordinate, whereas vanadic acid is tetrahedral, 4-coordinate. This is the basis for an explanation of why pKa1 > pKa2 for vanadium(V) oxoacids.
| equilibrium | pKa value |
|---|---|
| [VO2(H2O)4]+ ⇌ H3VO4 + H+ + 2H2O | pKa1 = 4.2 |
| H3VO4 ⇌ H2VO4− + H+ | pKa2 = 2.60 |
| H2VO4− ⇌ HVO42− + H+ | pKa3 = 7.92 |
| HVO42− ⇌ VO43− + H+ | pKa4 = 13.27 |
Isoelectric point
For substances in solution the isoelectric point (pI) is defined as the pH at which the sum, weighted by charge value, of concentrations of positively charged species is equal to the weighted sum of concentrations of negatively charged species. In the case that there is one species of each type, the isoelectric point can be obtained directly from the pK values. Take the example of glycine, defined as AH. There are two dissociation equilibria to consider.
- AH2+ ⇌ AH + H+; [AH][H+] = K1[AH2+]
- AH ⇌ A- + H+; [A-][H+] = K2[AH]
Substitute the expression for [AH] into the first equation
- [A-][H+]2 = K1K2[AH2+]
At the isoelectric point the concentration of the positively charged species, AH2+, is equal to the concentration of the negatively charged species, A-, so
- [H+]2 = K1K2
Therefore, taking cologarithms, the pH is given by
pI values for amino acids are listed at Proteinogenic amino acid#Chemical properties. When more than two charged species are in equilibrium with each other a full speciation calculation may be needed.
水的自身电离
Water has both acidic and basic properties. The equilibrium constant for the equilibrium
- 2 H2O ⇌ OH− + H3O+
is given by
When, as is usually the case, the concentration of water can be assumed to be constant, this expression may be replaced by
The self-ionization constant of water, Kw, is thus just a special case of an acid dissociation constant.
| T/°C | 0 | 5 | 10 | 15 | 20 | 25 | 30 | 35 | 40 | 45 | 50 |
|---|---|---|---|---|---|---|---|---|---|---|---|
| pKw | 14.943 | 14.734 | 14.535 | 14.346 | 14.167 | 13.997 | 13.830 | 13.680 | 13.535 | 13.396 | 13.262 |
From these data it can be deduced that Kw = 10−14 at 24.87 °C. At that temperature both hydrogen and hydroxide ions have a concentration of 10−7 mol dm−3.
Amphoteric substances
An amphoteric substance is one that can act as an acid or as a base, depending on pH. Water (above) is amphoteric. Another example of an amphoteric molecule is the bicarbonate ion HCO3− that is the conjugate base of the carbonic acid molecule H2CO3 in the equilibrium
- H2CO3 + H2O ⇌ HCO3− + H3O+
but also the conjugate acid of the carbonate ion CO32− in (the reverse of) the equilibrium
- HCO3− + OH− ⇌ CO32− + H2O.
Carbonic acid equilibria are important for acid-base homeostasis in the human body.
An amino acid is also amphoteric with the added complication that the neutral molecule is subject to an internal acid-base equilibrium in which the basic amino group attracts and binds the proton from the acidic carboxyl group, forming a zwitterion.
- NH2CHRCO2H ⇌ NH3+CHRCO2-
At pH less than about 5 both the carboxylate group and the amino group are protonated. As pH increases the acid dissociates according to
- NH3+CHRCO2H ⇌ NH3+CHRCO2- + H+
At high pH a second dissociation may take place.
- NH3+CHRCO2- ⇌ NH2CHRCO2- + H+
Thus the zwitter ion, NH3+CHRCO2-, is amphoteric because it may either be protonated or deprotonated.
碱
Historically, the equilibrium constant Kb for a base has been defined as the association constant for protonation of the base, B, to form the conjugate acid, HB+.
- B + H2O ⇌ HB+ + OH−
Using similar reasoning to that used before
Kb is related to Ka for the conjugate acid. In water, the concentration of the hydroxide ion, [OH−], is related to the concentration of the hydrogen ion by Kw = [H+] [OH−], therefore
Substitution of the expression for [OH−] into the expression for Kb gives
When Ka, Kb and Kw are determined under the same conditions of temperature and ionic strength, it follows, taking cologarithms, that pKb = pKw − pKa. In aqueous solutions at 25 °C, pKw is 13.9965,[17] so pKb ~ 14 − pKa. In effect there is no need to define pKb separately from pKa, but it is done here because pKb values can be found in the older literature.
Temperature dependence
All equilibrium constants vary with temperature according to the van 't Hoff equation[18]
R is the gas constant and T is the absolute temperature . Thus, for exothermic reactions, (the standard enthalpy change, ΔH![]() , is negative) K decreases with temperature, but for endothermic reactions (ΔH
, is negative) K decreases with temperature, but for endothermic reactions (ΔH![]() is positive) K increases with temperature.
is positive) K increases with temperature.
在非水溶剂中的酸度
A solvent will be more likely to promote ionization of a dissolved acidic molecule in the following circumstances.[19]
- It is a protic solvent, capable of forming hydrogen bonds.
- It has a high donor number, making it a strong Lewis base.
- it has a high dielectric constant (relative permittivity), making it a good solvent for ionic species.
pKa values of organic compounds are often obtained using the aprotic solvents dimethyl sulfoxide (DMSO)[19] and acetonitrile (ACN).[20]
| Solvent | Donor number[19] | Dielectric constant[19] |
|---|---|---|
| Acetonitrile | 14 | 37 |
| Dimethylsulfoxide | 30 | 47 |
| Water | 18 | 78 |
DMSO is widely used as an alternative to water because it has a lower dielectric constant than water, and is less polar and so dissolves non-polar, hydrophobic substances more easily. It has a measurable pKa range of about 1 to 30. Acetonitrile is less basic than DMSO, and, so, in general, acids are weaker and bases are stronger in this solvent. Some pKa values at 25 °C for acetonitrile (ACN)[21][22][23] and dimethyl sulfoxide (DMSO)[24] are shown in the following tables. Values for water are included for comparison.
| HA ⇌ A− + H+ | ACN | DMSO | water |
|---|---|---|---|
| p-Toluenesulfonic acid | 8.5 | 0.9 | strong |
| 2,4-Dinitrophenol | 16.66 | 5.1 | 3.9 |
| Benzoic acid | 21.51 | 11.1 | 4.2 |
| Acetic acid | 23.51 | 12.6 | 4.756 |
| Phenol | 29.14 | 18.0 | 9.99 |
| BH+ ⇌ B + H+ | |||
| Pyrrolidine | 19.56 | 10.8 | 11.4 |
| Triethylamine | 18.82 | 9.0 | 10.72 |
| Proton sponge | 18.62 | 7.5 | 12.1 |
| Pyridine | 12.53 | 3.4 | 5.2 |
| Aniline | 10.62 | 3.6 | 4.6 |
Ionization of acids is less in an acidic solvent than in water. For example, hydrogen chloride is a weak acid when dissolved in acetic acid. This is because acetic acid is a much weaker base than water.
- HCl + CH3CO2H ⇌ Cl− + CH3C(OH)2+
- acid + base ⇌ conjugate base + conjugate acid
Compare this reaction with what happens when acetic acid is dissolved in the more acidic solvent pure sulfuric acid[25]
- H2SO4 + CH3CO2H ⇌ HSO4− + CH3C(OH)2+
The unlikely geminal diol species CH3C(OH)2+ is stable in these environments. For aqueous solutions the pH scale is the most convenient acidity function.[26] Other acidity functions have been proposed for non-aqueous media, the most notable being the Hammett acidity function, H0, for superacid media and its modified version H− for superbasic media.[27]

In aprotic solvents, oligomers, such as the well-known acetic acid dimer, may be formed by hydrogen bonding. An acid may also form hydrogen bonds to its conjugate base. This process, known as homoconjugation, has the effect of enhancing the acidity of acids, lowering their effective pKa values, by stabilizing the conjugate base. Homoconjugation enhances the proton-donating power of toluenesulfonic acid in acetonitrile solution by a factor of nearly 800.[28] In aqueous solutions, homoconjugation does not occur, because water forms stronger hydrogen bonds to the conjugate base than does the acid.
混合溶剂

When a compound has limited solubility in water it is common practice (in the pharmaceutical industry, for example) to determine pKa values in a solvent mixture such as water/dioxane or water/methanol, in which the compound is more soluble.[30] In the example shown at the right, the pKa value rises steeply with increasing percentage of dioxane as the dielectric constant of the mixture is decreasing.
A pKa value obtained in a mixed solvent cannot be used directly for aqueous solutions. The reason for this is that when the solvent is in its standard state its activity is defined as one. For example, the standard state of water:dioxane 9:1 is precisely that solvent mixture, with no added solutes. To obtain the pKa value for use with aqueous solutions it has to be extrapolated to zero co-solvent concentration from values obtained from various co-solvent mixtures.
These facts are obscured by the omission of the solvent from the expression that is normally used to define pKa, but pKa values obtained in a given mixed solvent can be compared to each other, giving relative acid strengths. The same is true of pKa values obtained in a particular non-aqueous solvent such a DMSO.
As of 2008, a universal, solvent-independent, scale for acid dissociation constants has not been developed, since there is no known way to compare the standard states of two different solvents.
影响pKa值的因素
Pauling's second rule states that the value of the first pKa for acids of the formula XOm(OH) n is approximately independent of n and X and is approximately 8 for m = 0, 2 for m = 1, −3 for m = 2 and < −10 for m = 3.[15] This correlates with the oxidation state of the central atom, X: the higher the oxidation state the stronger the oxyacid. For example, pKa for HClO is 7.2, for HClO2 is 2.0, for HClO3 is −1 and HClO4 is a strong acid.
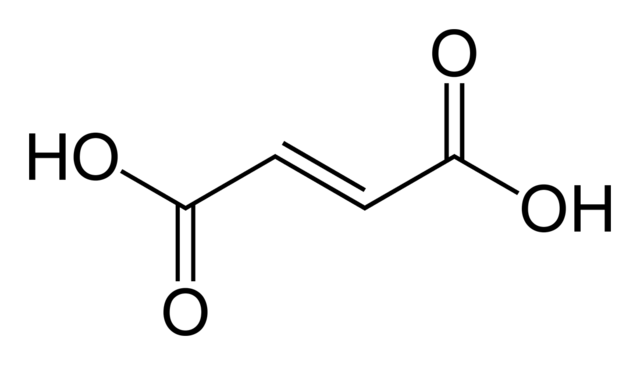
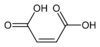

With organic acids inductive effects and mesomeric effects affect the pKa values. A simple example is provided by the effect of replacing the hydrogen atoms in acetic acid by the more electronegative chlorine atom. The electron-withdrawing effect of the substituent makes ionisation easier, so successive pKa values decrease in the series 4.7, 2.8, 1.4 and 0.7 when 0,1, 2 or 3 chlorine atoms are present.[31] The Hammett equation, provides a general expression for the effect of substituents.[32]
- log Ka = log Ka0 + ρσ.
Ka is the dissociation constant of a substituted compound, Ka0 is the dissociation constant when the substituent is hydrogen, ρ is a property of the unsubstituted compound and σ has a particular value for each substituent. A plot of log Ka against σ is a straight line with intercept log Ka0 and slope ρ. This is an example of a linear free energy relationship as log Ka is proportional to the standard fee energy change. Hammett originally[33] formulated the relationship with data from benzoic acid with different substiuents in the ortho- and para- positions: some numerical values are in Hammett equation. This and other studies allowed substituents to be ordered according to their electron-withdrawing or electron-releasing power, and to distinguish between inductive and mesomeric effects.[34][35]
Alcohols do not normally behave as acids in water, but the presence of a double bond adjacent to the OH group can substantially decrease the pKa by the mechanism of keto-enol tautomerism. Ascorbic acid is an example of this effect. The diketone 2,4-pentanedione (acetylacetone) is also a weak acid because of the keto-enol equilibrium. In aromatic compounds, such as phenol, which have an OH substituent, conjugation with the aromatic ring as a whole greatly increases the stability of the deprotonated form.
Structural effects can also be important. The difference between fumaric acid and maleic acid is a classic example. Fumaric acid is (E)-1,4-but-2-enedioic acid, a trans isomer, whereas maleic acid is the corresponding cis isomer, i.e. (Z)-1,4-but-2-enedioic acid (see cis-trans isomerism). Fumaric acid has pKa values of approximately 3.0 and 4.5. By contrast, maleic acid has pKa values of approximately 1.5 and 6.5. The reason for this large difference is that when one proton is removed from the cis- isomer (maleic acid) a strong intramolecular hydrogen bond is formed with the nearby remaining carboxyl group. This favors the formation of the maleate H+, and it opposes the removal of the second proton from that species. In the trans isomer, the two carboxyl groups are always far apart, so hydrogen bonding is not observed.[36]
Proton sponge, 1,8-bis(dimethylamino)naphthalene, has a pKa value of 12.1. It is one of the strongest amine bases known. The high basicity is attributed to the relief of strain upon protonation and strong internal hydrogen bonding.[37][38]
Effects of the solvent and solvation should be mentioned also in this section. It turns out, these influences are more subtle than that of a dielectric medium mentioned above. For example, the expected (by electronic effects of methyl substituents) and observed in gas phase order of basicity of methylamines, Me3N > Me2NH > MeNH2 > NH3, is changed by water to Me2NH > MeNH2 > Me3N > NH3. Neutral methylamine molecules are hydrogen-bonded to water molecules mailnly through one acceptor, N-HOH, interaction and only occasionally just one more donor bond, NH-OH2. Hence, methylamines are stabilized to about the same extent by hydration, regardless of the number of methyl groups. In stark contrast, corresponding methylammonium cations always utilize all the available protons for donor NH-OH2 bonding. Relative stabilization of methylammonium ions thus decreases with the number of methyl groups explaining the order of water basicity of methylamines.[39]
热力学
An equilibrium constant is related to the standard Gibbs energy change for the reaction, so for an acid dissociation constant
R is the gas constant and T is the absolute temperature. Note that pKa= −log Ka and 2.303 ≈ ln 10. At 25 °C ΔG![]() in kJ·mol−1 = 5.708 pKa (1 kJ·mol−1 = 1000 Joules per mole). Free energy is made up of an enthalpy term and an entropy term.[7]
in kJ·mol−1 = 5.708 pKa (1 kJ·mol−1 = 1000 Joules per mole). Free energy is made up of an enthalpy term and an entropy term.[7]
The standard enthalpy change can be determined by calorimetry or by using the van 't Hoff equation, though the calorimetric method is preferable. When both the standard enthalpy change and acid dissociation constant have been determined, the standard entropy change is easily calculated from the equation above. In the following table, the entropy terms are calculated from the experimental values of pKa and ΔH![]() . The data were critically selected and refer to 25 °C and zero ionic strength, in water.[7]
. The data were critically selected and refer to 25 °C and zero ionic strength, in water.[7]
| Compound | Equilibrium | pKa | ΔG |
ΔH |
—TΔS |
|---|---|---|---|---|---|
| HA = Acetic acid | HA ⇌ H+ + A− | 4.756 | 27.147† | −0.41 | 27.56‡ |
| H2A+ = GlycineH+ | H2A+ ⇌ HA + H+ | 2.351 | 13.420 | 4.00 | 9.419 |
| HA ⇌ H+ + A− | 9.78 | 55.825 | 44.20 | 11.6 | |
| H2A = Maleic acid | H2A ⇌ HA− + H+ | 1.92 | 10.76 | 1.10 | 9.85 |
| HA− ⇌ H+ + A2− | 6.27 | 35.79 | −3.60 | 39.4 | |
| H3A = Citric acid | H3A ⇌ H2A− + H+ | 3.128 | 17.855 | 4.07 | 13.78 |
| H2A− ⇌ HA2− + H+ | 4.76 | 27.176 | 2.23 | 24.9 | |
| HA2− ⇌ A3− + H+ | 6.40 | 36.509 | −3.38 | 39.9 | |
| H3A = Boric acid | H3A ⇌ H2A− + H+ | 9.237 | 52.725 | 13.80 | 38.92 |
| H3A = Phosphoric acid | H3A ⇌ H2A− + H+ | 2.148 | 12.261 | −8.00 | 20.26 |
| H2A− ⇌ HA2− + H+ | 7.20 | 41.087 | 3.60 | 37.5 | |
| HA2− ⇌ A3− + H+ | 12.35 | 80.49 | 16.00 | 54.49 | |
| HA− = Hydrogen sulfate | HA− ⇌ A2− + H+ | 1.99 | 11.36 | −22.40 | 33.74 |
| H2A = Oxalic acid | H2A ⇌ HA− + H+ | 1.27 | 7.27 | −3.90 | 11.15 |
| HA− ⇌ A2− + H+ | 4.266 | 24.351 | 7.00 | 31.35 |
- † ΔG
 = 2.303RT pKa
= 2.303RT pKa - ‡ Computed here, from ΔH and ΔG values supplied in the citation, using —TΔS
 = ΔG
= ΔG — ΔH
— ΔH
| Compound | Equilibrium | pKa | ΔH |
—TΔS |
|---|---|---|---|---|
| B = Ammonia | HB+ ⇌ B + H+ | 9.245 | 51.95 | 0.8205 |
| B = Methylamine | HB+ ⇌ B + H+ | 10.645 | 55.34 | 5.422 |
| B = Triethylamine | HB+ ⇌ B + H+ | 10.72 | 43.13 | 18.06 |
The first point to note is that, when pKa is positive, the standard free energy change for the dissociation reaction is also positive. Second, some reactions are exothermic and some are endothermic, but, when ΔH![]() is negative −TΔS
is negative −TΔS![]() is the dominant factor, which determines that ΔG
is the dominant factor, which determines that ΔG![]() is positive. Last, the entropy contribution is always unfavourable (ΔS
is positive. Last, the entropy contribution is always unfavourable (ΔS![]() < 0) in these reactions. Ions in aqueous solution tend to orient the surrounding water molecules, which orders the solution and decreases the entropy. The contribution of an ion to the entropy is the partial molar entropy which is often negative, especially for small or highly charged ions.[40] The ionization of a neutral acid involves formation of two ions so that the entropy decreases (ΔS
< 0) in these reactions. Ions in aqueous solution tend to orient the surrounding water molecules, which orders the solution and decreases the entropy. The contribution of an ion to the entropy is the partial molar entropy which is often negative, especially for small or highly charged ions.[40] The ionization of a neutral acid involves formation of two ions so that the entropy decreases (ΔS![]() < 0). On the second ionization of the same acid, there are now three ions and the anion has a charge, so the entropy again decreases.
< 0). On the second ionization of the same acid, there are now three ions and the anion has a charge, so the entropy again decreases.
Note that the standard free energy change for the reaction is for the changes from the reactants in their standard states to the products in their standard states. The free energy change at equilibrium is zero since the chemical potentials of reactants and products are equal at equilibrium.
实验测定

The experimental determination of pKa values is commonly performed by means of titrations, in a medium of high ionic strength and at constant temperature.[41] A typical procedure would be as follows. A solution of the compound in the medium is acidified with a strong acid to the point where the compound is fully protonated. The solution is then titrated with a strong base until all the protons have been removed. At each point in the titration pH is measured using a glass electrode and a pH meter. The equilibrium constants are found by fitting calculated pH values to the observed values, using the method of least squares.[42]
The total volume of added strong base should be small compared to the initial volume of titrand solution in order to keep the ionic strength nearly constant. This will ensure that pKa remains invariant during the titration.
A calculated titration curve for oxalic acid is shown at the right. Oxalic acid has pKa values of 1.27 and 4.27. Therefore the buffer regions will be centered at about pH 1.3 and pH 4.3. The buffer regions carry the information necessary to get the pKa values as the concentrations of acid and conjugate base change along a buffer region.
Between the two buffer regions there is an end-point, or equivalence point, where the pH rises by about two units. This end-point is not sharp and is typical of a diprotic acid whose buffer regions overlap by a small amount: pKa2 − pKa1 is about three in this example. (If the difference in pK values were about two or less, the end-point would not be noticeable.) The second end-point begins at about pH 6.3 and is sharp. This indicates that all the protons have been removed. When this is so, the solution is not buffered and the pH rises steeply on addition of a small amount of strong base. However, the pH does not continue to rise indefinitely. A new buffer region begins at about pH 11 (pKw − 3), which is where self-ionization of water becomes important.
It is very difficult to measure pH values of less than two in aqueous solution with a glass electrode, because the Nernst equation breaks down at such low pH values. To determine pK values of less than about 2 or more than about 11 spectrophotometric[43] or NMR[11][44] measurements may be used instead of, or combined with, pH measurements.[45]
When the glass electrode cannot be employed, as with non-aqueous solutions, spectrophotometric methods are frequently used.[22] These may involve absorbance or fluorescence measurements. In both cases the measured quantity is assumed to be proportional to the sum of contributions from each photo-active species; with absorbance measurements the Beer-Lambert law is assumed to apply.
Aqueous solutions with normal water cannot be used for 1H NMR measurements but heavy water, D2O, must be used instead. 13C NMR data, however, can be used with normal water and 1H NMR spectra can be used with non-aqueous media. The quantities measured with NMR are time-averaged chemical shifts, as proton exchange is fast on the NMR time-scale. Other chemical shifts, such as those of 31P can be measured.
Micro-constants

A base such as spermine has a few different sites where protonation can occur. In this example the first proton can go on the terminal -NH2 group, or either of the internal -NH- groups. The pKa values for dissociation of spermine protonated at one or other of the sites are examples of micro-constants. They cannot be determined directly by means of pH, absorbance, fluorescence or NMR measurements. Nevertheless, the site of protonation is very important for biological function, so mathematical methods have been developed for the determination of micro-constants.[46]
应用与影响
A knowledge of pKa values is important for the quantitative treatment of systems involving acid–base equilibria in solution. Many applications exist in biochemistry; for example, the pKa values of proteins and amino acid side chains are of major importance for the activity of enzymes and the stability of proteins.[47] Protein pKa values cannot always be measured directly, but may be calculated using theoretical methods. Buffer solutions are used extensively to provide solutions at or near the physiological pH for the study of biochemical reactions;[48] the design of these solutions depends on a knowledge of the pKa values of their components. Important buffer solutions include MOPS, which provides a solution with pH 7.2, and tricine, which is used in gel electrophoresis.[49][50] Buffering is an essential part of acid base physiology including acid-base homeostasis,[51] and is key to understanding disorders such as acid-base imbalance.[52][53][54] The isoelectric point of a given molecule is a function of its pK values, so different molecules have different isoelectric points. This permits a technique called isoelectric focusing,[55] which is used for separation of proteins by 2-D gel polyacrylamide gel electrophoresis.
Buffer solutions also play a key role in analytical chemistry. They are used whenever there is a need to fix the pH of a solution at a particular value. Compared with an aqueous solution, the pH of a buffer solution is relatively insensitive to the addition of a small amount of strong acid or strong base. The buffer capacity[56] of a simple buffer solution is largest when pH = pKa. In acid-base extraction, the efficiency of extraction of a compound into an organic phase, such as an ether, can be optimised by adjusting the pH of the aqueous phase using an appropriate buffer. At the optimum pH, the concentration of the electrically neutral species is maximised; such a species is more soluble in organic solvents having a low dielectric constant than it is in water. This technique is used for the purification of weak acids and bases.[57]
A pH indicator is a weak acid or weak base that changes colour in the transition pH range, which is approximately pKa ± 1. The design of a universal indicator requires a mixture of indicators whose adjacent pKa values differ by about two, so that their transition pH ranges just overlap.
In pharmacology ionization of a compound alters its physical behaviour and macro properties such as solubility and lipophilicity (log p). For example ionization of any compound will increase the solubility in water, but decrease the lipophilicity. This is exploited in drug development to increase the concentration of a compound in the blood by adjusting the pKa of an ionizable group.[58]
Knowledge of pKa values is important for the understanding of coordination complexes, which are formed by the interaction of a metal ion, Mm+, acting as a Lewis acid, with a ligand, L, acting as a Lewis base. However, the ligand may also undergo protonation reactions, so the formation of a complex in aqueous solution could be represented symbolically by the reaction
- [M(H2O)n]m+ +LH ⇌ [M(H2O)n−1L](m−1)+ + H3O+
To determine the equilibrium constant for this reaction, in which the ligand loses a proton, the pKa of the protonated ligand must be known. In practice, the ligand may be polyprotic; for example EDTA4− can accept four protons; in that case, all pKa values must be known. In addition, the metal ion is subject to hydrolysis, that is, it behaves as a weak acid, so the pK values for the hydrolysis reactions must also be known.[59] Assessing the hazard associated with an acid or base may require a knowledge of pKa values.[60] For example, hydrogen cyanide is a very toxic gas, because the cyanide ion inhibits the iron-containing enzyme cytochrome c oxidase. Hydrogen cyanide is a weak acid in aqueous solution with a pKa of about 9. In strongly alkaline solutions, above pH 11, say, it follows that sodium cyanide is "fully dissociated" so the hazard due to the hydrogen cyanide gas is much reduced. An acidic solution, on the other hand, is very hazardous because all the cyanide is in its acid form. Ingestion of cyanide by mouth is potentially fatal, independently of pH, because of the reaction with cytochrome c oxidase.
In environmental science acid–base equilibria are important for lakes[61] and rivers;[62][63] for example, humic acids are important components of natural waters. Another example occurs in chemical oceanography:[64] in order to quantify the solubility of iron(III) in seawater at various salinities, the pKa values for the formation of the iron(III) hydrolysis products Fe(OH)2+, Fe(OH)2+ and Fe(OH)3 were determined, along with the solubility product of iron hydroxide.[65]
常用物质的pKa值
There are multiple techniques to determine the pKa of a chemical, leading to some discrepancies between different sources. Well measured values are typically within 0.1 units of each other. Data presented here were taken at 25 °C in water.[3][66] More values can be found in thermodynamics, above.
| Chemical Name | Equilibrium | pKa |
|---|---|---|
| B = Adenine | BH22+ ⇌ BH+ + H+ | 4.17 |
| BH+ ⇌ B + H+ | 9.65 | |
| H3A = Arsenic acid | H3A ⇌ H2A− + H+ | 2.22 |
| H2A− ⇌ HA2− + H+ | 6.98 | |
| HA2− ⇌ A3− + H+ | 11.53 | |
| HA = Benzoic acid | HA ⇌ H+ + A− | 4.204 |
| HA = Butanoic acid | HA ⇌ H+ + A− | 4.82 |
| H2A = Chromic acid | H2A ⇌ HA− + H+ | 0.98 |
| HA− ⇌ A2− + H+ | 6.5 | |
| B = Codeine | BH+ ⇌ B + H+ | 8.17 |
| HA = Cresol | HA ⇌ H+ + A− | 10.29 |
| HA = Formic acid | HA ⇌ H+ + A− | 3.751 |
| HA = Hydrofluoric acid | HA ⇌ H+ + A− | 3.17 |
| HA = Hydrocyanic acid | HA ⇌ H+ + A− | 9.21 |
| HA = Hydrogen selenide | HA ⇌ H+ + A− | 3.89 |
| HA = Hydrogen peroxide (90%) | HA ⇌ H+ + A− | 11.7 |
| HA = Lactic acid | HA ⇌ H+ + A− | 3.86 |
| HA = Propionic acid | HA ⇌ H+ + A− | 4.87 |
| HA = Phenol | HA ⇌ H+ + A− | 9.99 |
| H2A = L-(+)-Ascorbic Acid | H2A ⇌ HA− + H+ | 4.17 |
| HA− ⇌ A2− + H+ | 11.57 |
参见
- Acids in wine: tartaric, malic and citric are the principal acids in wine.
- Ocean acidification: dissolution of atmospheric carbon dioxide affects seawater pH. The reaction depends on total inorganic carbon and on solubility equilibria with solid carbonates such as limestone and dolomite.
- Grotthuss mechanism: how protons are transferred between hydronium ions and water molecules, accounting for the exceptionally high ionic mobility of the proton (animation).
- Predominance diagram: relates to equilibria involving polyoxyanions. pKa values are needed to construct these diagrams.
- Proton affinity: a measure of basicity in the gas phase.
- Stability constants of complexes: formation of a complex can often be seen as a competition between proton and metal ion for a ligand, which is the product of dissociation of an acid.
- Hammett acidity function: a measure of acidity that is used for very concentrated solutions of strong acids, including superacids.
参考文献
- Miessler, G. Inorganic Chemistry 2nd. Prentice Hall. 1991. ISBN 0-13-465659-8. Chapter 6: Acid-Base and Donor-Acceptor Chemistry
- Bell, R.P. The Proton in Chemistry 2nd. London: Chapman & Hall. 1973. ISBN 0-8014-0803-2. Includes discussion of many organic Brønsted acids.
- Shriver, D.F; Atkins, P.W. Inorganic Chemistry 3rd. Oxford: Oxford University Press. 1999. ISBN 0-19-850331-8. 引文使用过时参数
coauthors(帮助) Chapter 5: Acids and Bases - Housecroft, C. E.; Sharpe, A. G. Inorganic Chemistry 3rd. Prentice Hall. 2008. ISBN 978-0131755536. Chapter 6: Acids, Bases and Ions in Aqueous Solution
- Headrick, J.M.; Diken, E.G.; Walters, R. S.; Hammer, N. I.; Christie, R.A. ; Cui, J.; Myshakin, E.M.; Duncan, M.A.; Johnson, M.A.; Jordan, K.D. Spectral Signatures of Hydrated Proton Vibrations in Water Clusters. Science. 2005, 308 (5729): 1765–69. Bibcode:2005Sci...308.1765H. PMID 15961665. doi:10.1126/science.1113094. 引文使用过时参数
coauthors(帮助) - Smiechowski, M.; Stangret, J. Proton hydration in aqueous solution: Fourier transform infrared studies of HDO spectra. J. Chem. Phys. 2006, 125 (20): 204508–204522. Bibcode:2006JChPh.125t4508S. PMID 17144716. doi:10.1063/1.2374891. 引文使用过时参数
coauthors(帮助) - Goldberg, R.; Kishore, N.; Lennen, R. Thermodynamic Quantities for the Ionization Reactions of Buffers (PDF). J. Phys. Chem. Ref. Data. 2002, 31 (2): 231–370. Bibcode:1999JPCRD..31..231G. doi:10.1063/1.1416902. 引文使用过时参数
coauthors(帮助) 引用错误:带有name属性“Goldmine”的<ref>标签用不同内容定义了多次 - Jolly, William L. Modern Inorganic Chemistry. McGraw-Hill. 1984: 198. ISBN 007027602 请检查
|isbn=值 (帮助). - Burgess, J. Metal Ions in Solution. Ellis Horwood. 1978. ISBN 0-85312-027-7. Section 9.1 "Acidity of Solvated Cations" lists many pKa values.
- Popov, K.; Ronkkomaki, H.; Lajunen, L.H.J. Guidelines for NMR Measurements for Determination of High and Low pKa Values (PDF). Pure Appl. Chem. 2006, 78 (3): 663–675. doi:10.1351/pac200678030663. 引文使用过时参数
coauthors(帮助) - Project: Ionic Strength Corrections for Stability Constants. International Union of Pure and Applied Chemistry. [2008-11-23]. (原始内容存档于29 October 2008).
- Dasent, W.E. Inorganic Energetics: An Introduction. Cambridge University Press. 1982. ISBN 0-521-28406-6. Chapter 5
- Brown, T.E.; Lemay, H.E.; Bursten,B.E.; Murphy, C.; Woodward, P. Chemistry: The Central Science 11th. New York: Prentice-Hall. 2008: 689. ISBN 0-13-600617-5. 引文使用过时参数
coauthors(帮助) - Greenwood, N.N.; Earnshaw, A. Chemistry of the Elements 2nd. Oxford: Butterworth-Heinemann. 1997: 50. ISBN 0-7506-3365-4. 引文使用过时参数
coauthor(帮助) - Harned, H.S.; Owen, B.B. The Physical Chemistry of Electrolytic Solutions. New York: Reinhold Publishing Corp. 1958: 634–649, 752–754.
- Lide, D.R. CRC Handbook of Chemistry and Physics, Student Edition 84th. CRC Press. 2004. ISBN 0-8493-0597-7. Section D–152
- Atkins, P.W.; de Paula, J. Physical Chemistry. Oxford University Press. 2006. ISBN 0-19-870072-5. 引文使用过时参数
coauthors(帮助) Section 7.4: The Response of Equilibria to Temperature - Template:Loudon p. 317–318
- March, J.; Smith, M. Advanced Organic Chemistry 6th. New York: John Wiley & Sons. 2007. ISBN 978-0-471-72091-1. 引文使用过时参数
coauthors(帮助) Chapter 8: Acids and Bases - Kütt, A.; Movchun, V.; Rodima, T,; Dansauer, T.; Rusanov, E.B. ; Leito, I.; Kaljurand, I.; Koppel, J.; Pihl, V.; Koppel, I.; Ovsjannikov, G.; Toom, L.; Mishima, M.; Medebielle, M.; Lork, E.; Röschenthaler, G-V.; Koppel, I.A.; Kolomeitsev, A.A. Pentakis(trifluoromethyl)phenyl, a Sterically Crowded and Electron-withdrawing Group: Synthesis and Acidity of Pentakis(trifluoromethyl)benzene, -toluene, -phenol, and -aniline. J. Org. Chem. 2008, 73 (7): 2607–2620. PMID 18324831. doi:10.1021/jo702513w. 引文使用过时参数
coauthors(帮助) - Kütt, A.; Leito, I.; Kaljurand, I.; Sooväli, L.; Vlasov, V.M.; Yagupolskii, L.M.; Koppel, I.A. A Comprehensive Self-Consistent Spectrophotometric Acidity Scale of Neutral Brønsted Acids in Acetonitrile. J. Org. Chem. 2006, 71 (7): 2829–2838. PMID 16555839. doi:10.1021/jo060031y. 引文使用过时参数
coauthors(帮助) - Kaljurand, I.; Kütt, A.; Sooväli, L.; Rodima, T.; Mäemets, V. Leito, I; Koppel, I.A. Extension of the Self-Consistent Spectrophotometric Basicity Scale in Acetonitrile to a Full Span of 28 pKa Units: Unification of Different Basicity Scales. J. Org. Chem. 2005, 70 (3): 1019–1028. PMID 15675863. doi:10.1021/jo048252w. 引文使用过时参数
coauthors(帮助) - Bordwell pKa Table (Acidity in DMSO). [2008-11-02]. (原始内容存档于9 October 2008).
- Housecroft, C. E.; Sharpe, A. G. Inorganic Chemistry 3rd. Prentice Hall. 2008. ISBN 978-0131755536. Chapter 8: Non-Aqueous Media
- Rochester, C.H. Acidity Functions. Academic Press. 1970. ISBN 0-12-590850-4.
- Olah, G.A; Prakash, S; Sommer, J. Superacids. New York: Wiley Interscience. 1985. ISBN 0-471-88469-3. 引文使用过时参数
coauthors(帮助) - Coetzee, J.F.; Padmanabhan, G.R. Proton Acceptor Power and Homoconjugation of Mono- and Diamines. J. Amer. Chem. Soc. 1965, 87 (22): 5005–5010. doi:10.1021/ja00950a006. 引文使用过时参数
coauthors(帮助) - Pine, S.H.; Hendrickson, J.B.; Cram, D.J.; Hammond, G.S. Organic chemistry. McGraw–Hill: 203. 1980. ISBN 0-07-050115-7. 引文使用过时参数
coauthors(帮助) - Box, K.J.; Völgyi, G. Ruiz, R. Comer, J.E. Takács-Novák, K., Bosch, E. Ràfols, C. Rosés, M. Physicochemical Properties of a New Multicomponent Cosolvent System for the pKa Determination of Poorly Soluble Pharmaceutical Compounds. Helv. Chim. Acta. 2007, 90 (8): 1538–1553. doi:10.1002/hlca.200790161. 引文使用过时参数
coauthors(帮助) - Pauling, L. The nature of the chemical bond and the structure of molecules and crystals; an introduction to modern structural chemistry 3rd. Ithaca (NY): Cornell University Press. 1960: 277. ISBN 0-8014-0333-2.
- Pine, S.H.; Hendrickson, J.B.; Cram, D.J.; Hammond, G.S. Organic Chemistry. McGraw–Hill. 1980. ISBN 0-07-050115-7. 引文使用过时参数
coauthors(帮助) Section 13-3: Quantitative Correlations of Substituent Effects (Part B) – The Hammett Equation - Hammett, L.P. The Effect of Structure upon the Reactions of Organic Compounds. Benzene Derivatives. J. Amer. Chem. Soc. 1937, 59 (1): 96–103. doi:10.1021/ja01280a022.
- Hansch, C.; Leo, A.; Taft, R. W. A Survey of Hammett Substituent Constants and Resonance and Field Parameters. Chem. Rev. 1991, 91 (2): 165–195. doi:10.1021/cr00002a004. 引文使用过时参数
coauthors(帮助) - Shorter, J. Compilation and critical evaluation of structure-reactivity parameters and equations: Part 2. Extension of the Hammett σ scale through data for the ionization of substituted benzoic acids in aqueous solvents at 25 C (Technical Report). Pure and Applied Chemistry. 1997, 69 (12): 2497–2510. doi:10.1351/pac199769122497.
- Pine, S.H.; Hendrickson, J.B.; Cram, D.J.; Hammond, G.S. Organic chemistry. McGraw–Hill. 1980. ISBN 0-07-050115-7. 引文使用过时参数
coauthors(帮助) Section 6-2: Structural Effects on Acidity and Basicity - Alder, R.W.; Bowman, P.S.; Steele, W.R.S.; Winterman, D.R. The Remarkable Basicity of 1,8-bis(dimethylamino)naphthalene. Chem. Commun. 1968, (13): 723. doi:10.1039/C19680000723. 引文使用过时参数
coauthors(帮助);|pages=和|page=只需其一 (帮助) - Alder, R.W. Strain Effects on Amine Basicities. Chem. Rev. 1989, 89 (5): 1215–1223. doi:10.1021/cr00095a015.
- Fraczkiewicz R. In Silico Prediction of Ionization. Testa B and van de Waterbeemd H (编). Comprehensive medicinal chemistry II, Vol. 5. Amsterdam: Elsevier. 2007: 603–626. ISBN 0-08-044518-7.
- P. Atkins and J. de Paula, “Atkins’ Physical Chemistry” (8th edn W.H. Freeman 2006), p.94
- Martell, A.E.; Motekaitis, R.J. Determination and Use of Stability Constants. Wiley. 1992. ISBN 0-471-18817-4. 引文使用过时参数
coauthors(帮助) Chapter 4: Experimental Procedure for Potentiometric pH Measurement of Metal Complex Equilibria - Leggett, D.J. Computational Methods for the Determination of Formation Constants. Plenum. 1985. ISBN 0-306-41957-2.
- Allen, R.I.; Box,K.J.; Comer, J.E.A.; Peake, C.; Tam, K.Y. Multiwavelength Spectrophotometric Determination of Acid Dissociation Constants of Ionizable Drugs. J. Pharm. Biomed. Anal. 1998, 17 (4–5): 699–641. doi:10.1016/S0731-7085(98)00010-7. 引文使用过时参数
coauthors(帮助) - Szakács, Z.; Hägele, G. Accurate Determination of Low pK Values by 1H NMR Titration. Talanta. 2004, 62 (4): 819–825. PMID 18969368. doi:10.1016/j.talanta.2003.10.007. 引文使用过时参数
coauthors(帮助) - Box, K.J.; Donkor, R.E. Jupp, P.A. Leader, I.P. Trew, D.F. Turner, C.H. The Chemistry of Multi-Protic Drugs Part 1: A Potentiometric, Multi-Vavelength UV and NMR pH Titrimetric Study of the Micro-Speciation of SKI-606. J. Pharm. Biomed. Anal. 2008, 47 (2): 303–311. PMID 18314291. doi:10.1016/j.jpba.2008.01.015. 引文使用过时参数
coauthors(帮助) - Frassineti, C.; Alderighi, L; Gans, P; Sabatini, A; Vacca, A; Ghelli, S. Determination of Protonation Constants of Some Fluorinated Polyamines by Means of 13C NMR Data Processed by the New Computer Program HypNMR2000. Protonation Sequence in Polyamines.. Anal. Bioanal. Chem. 2003, 376 (7): 1041–1052. PMID 12845401. doi:10.1007/s00216-003-2020-0. 引文使用过时参数
coauthors(帮助) - Onufriev, A.; Case, D.A; Ullmann G.M. A Novel View of pH Titration in Biomolecules. Biochemistry. 2001, 40 (12): 3413–3419. PMID 11297406. doi:10.1021/bi002740q. 引文使用过时参数
coauthors(帮助) - Good, N.E.; Winget, G.D.; Winter, W.; Connolly, T.N.; Izawa, S.; Singh, R.M.M. Hydrogen Ion Buffers for Biological Research. Biochemistry. 1966, 5 (2): 467–477. PMID 5942950. doi:10.1021/bi00866a011. 引文使用过时参数
coauthors(帮助) - Dunn, M.J. Gel Electrophoresis: Proteins. Bios Scientific Publishers. 1993. ISBN 1-872748-21-X.
- Martin, R. Gel Electrophoresis: Nucleic Acids. Bios Scientific Publishers. 1996. ISBN 1-872748-28-7.
- Brenner, B.M. (Editor); Stein, J.H. (Editor). Acid–Base and Potassium Homeostasis. Churchill Livingstone. 1979. ISBN 0-443-08017-8. 引文使用过时参数
coauthors(帮助) - Scorpio, R. Fundamentals of Acids, Bases, Buffers & Their Application to Biochemical Systems. Kendall/Hunt Pub. Co. 2000. ISBN 0-7872-7374-0.
- Beynon, R.J.; Easterby, J.S. Buffer Solutions: The Basics. Oxford: Oxford University Press. 1996. ISBN 0-19-963442-4. 引文使用过时参数
coauthors(帮助) - Perrin, D.D.; Dempsey, B. Buffers for pH and Metal Ion Control. London: Chapman & Hall. 1974. ISBN 0-412-11700-2. 引文使用过时参数
coauthors(帮助) - Garfin, D.(Editor); Ahuja, S. (Editor). Handbook of Isoelectric Focusing and Proteomics 7. Elsevier. 2005. ISBN 0-12-088752-5U 请检查
|isbn=值 (帮助). 引文使用过时参数coauthors(帮助) - Hulanicki, A. Reactions of Acids and Bases in Analytical Chemistry. Masson, M.R. (translation editor). Horwood. 1987. ISBN 0-85312-330-6.
- Eyal, A.M. Acid Extraction by Acid–Base-Coupled Extractants. Ion Exchange and Solvent Extraction: A Series of Advances. 1997, 13: 31–94.
- Avdeef, A. Absorption and Drug Development: Solubility, Permeability, and Charge State. New York: Wiley. 2003. ISBN 0-471-42365-3.
- Beck, M.T.; Nagypál, I. Chemistry of Complex Equilibria. Horwood. 1990. ISBN 0-85312-143-5. 引文使用过时参数
coauthors(帮助) - van Leeuwen, C.J.; Hermens, L. M. Risk Assessment of Chemicals: An Introduction. Springer. 1995: 254–255. ISBN 0-7923-3740-9. 引文使用过时参数
coauthors(帮助) - Skoog, D.A; West, D.M.; Holler, J.F.; Crouch, S.R. Fundamentals of Analytical Chemistry 8th. Thomson Brooks/Cole. 2004. ISBN 0-03-035523-0. 引文使用过时参数
coauthors(帮助) Chapter 9-6: Acid Rain and the Buffer Capacity of Lakes - Stumm, W.; Morgan, J.J. Water Chemistry. New York: Wiley. 1996. ISBN 0-471-05196-9. 引文使用过时参数
coauthors(帮助) - Snoeyink, V.L.; Jenkins, D. Aquatic Chemistry: Chemical Equilibria and Rates in Natural Waters. New York: Wiley. 1980. ISBN 0-471-51185-4. 引文使用过时参数
coauthors(帮助) - Millero, F.J. Chemical Oceanography 3rd. London: Taylor and Francis. 2006. ISBN 0-8493-2280-4.
- Millero, F.J.; Liu, X. The Solubility of Iron in Seawater. Marine chemistry. 2002, 77 (1): 43–54. doi:10.1016/S0304-4203(01)00074-3. 引文使用过时参数
coauthors(帮助) - Speight, J.G. Lange's Handbook of Chemistry 18th. McGraw–Hill. 2005. ISBN 0-07-143220-5. Chapter 8
扩展阅读
- Albert, A.; Serjeant, E.P. The Determination of Ionization Constants: A Laboratory Manual. Chapman & Hall. 1971. ISBN 0-412-10300-1. 引文使用过时参数
coauthors(帮助) (Previous edition published as Ionization constants of acids and bases. London (UK): Methuen. 1962.) - Atkins, P.W.; Jones, L. Chemical Principles: The Quest for Insight 4th. W.H. Freeman. 2008. ISBN 1-4292-0965-8. 引文使用过时参数
coauthors(帮助) - Housecroft, C. E.; Sharpe, A. G. Inorganic Chemistry 3rd. Prentice Hall. 2008. ISBN 978-0131755536. (Non-aqueous solvents)
- Hulanicki, A. Reactions of Acids and Bases in Analytical Chemistry. Horwood. 1987. ISBN 0-85312-330-6. (translation editor: Mary R. Masson)
- Perrin, D.D.; Dempsey, B.; Serjeant, E.P. pKa Prediction for Organic Acids and Bases. Chapman & Hall. 1981. ISBN 0-412-22190-X. 引文使用过时参数
coauthors(帮助) - Reichardt, C. Solvents and Solvent Effects in Organic Chemistry 3rd. Wiley-VCH. 2003. ISBN 3-527-30618-8. Chapter 4: Solvent Effects on the Position of Homogeneous Chemical Equilibria.
- Skoog, D.A.; West, D.M.; Holler, J.F.; Crouch, S.R. Fundamentals of Analytical Chemistry 8th. Thomson Brooks/Cole. 2004. ISBN 0-03-035523-0. 引文使用过时参数
coauthors(帮助)
外部链接
- Extensive bibliography of pKa values in DMSO, acetonitrile, THF, heptane, 1,2-dichloroethane, and in the gas phase.
- All-in-one freeware for pH and acid-base equilibrium calculations and for simulation and analysis of potentiometric titration curves with spreadsheets.
- Includes a database with aqueous, non-aqueous, and gaseous phase pKa values than can be searched using SMILES or CAS registry numbers.
- pKa values for various acid and bases. Includes a table of some solubility products.
- Explanations of the relevance of these properties to pharmacology.
- Free online prediction tool (Marvin) pKa, logP, logD etc. From ChemAxon
- Chemicalize.org:List of predicted structure based properties
- Evans pKa Chart http://evans.harvard.edu/pdf/evans_pka_table.pdf
![{\displaystyle K_{\mathrm {a} }=\mathrm {\frac {[A^{-}][H^{+}]}{[HA]}} }](http://wikimedia.org/api/rest_v1/media/math/render/svg/4df1424aa532585fc7ad6dd660a596705ee31a2b)


![{\displaystyle K^{\ominus }=\mathrm {{\frac {[A^{-}][H_{3}O^{+}]}{[HA][H_{2}O]}}\times {\frac {\gamma _{A^{-}}\gamma _{H_{3}O^{+}}}{\gamma _{HA}\gamma _{H_{2}O}}}=\mathrm {\frac {[A^{-}][H_{3}O^{+}]}{[HA][H_{2}O]}} \times \Gamma } }](http://wikimedia.org/api/rest_v1/media/math/render/svg/98e5acdd208e3a6eda8213278e88c22d19e4c509)
![{\displaystyle \mathrm {pH} =\mathrm {p} K_{\mathrm {a} }+\log \mathrm {\frac {[A^{-}]}{[HA]}} }](http://wikimedia.org/api/rest_v1/media/math/render/svg/1e741bfd0c07772fa2abd205e79cd865a398268e)

![{\displaystyle K_{\mathrm {a} }=\mathrm {\frac {[H_{3}O^{+}][OH^{-}]}{[H_{2}O]^{2}}} }](http://wikimedia.org/api/rest_v1/media/math/render/svg/d0fd2af6a4e208433b23af32cd7afa504c549f0e)
![{\displaystyle K_{\mathrm {w} }=[\mathrm {H_{3}O} ^{+}][\mathrm {OH} ^{-}]\,}](http://wikimedia.org/api/rest_v1/media/math/render/svg/b28e22a7001351bdc196d0c1d2e7ea94f3b2842f)
![{\displaystyle K_{\mathrm {b} }=\mathrm {\frac {[HB^{+}][OH^{-}]}{[B]}} }](http://wikimedia.org/api/rest_v1/media/math/render/svg/5e8602a5fa0751164332991a802fe0f0a9226ba2)
![{\displaystyle \mathrm {[OH^{-}]} ={\frac {K_{\mathrm {w} }}{\mathrm {[H^{+}]} }}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/ab7f583da9f8b50145990ffa4342919930edfa16)
![{\displaystyle K_{\mathrm {b} }={\frac {[\mathrm {HB^{+}} ]K_{\mathrm {w} }}{\mathrm {[B][H^{+}]} }}={\frac {K_{\mathrm {w} }}{K_{\mathrm {a} }}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/55e99b9289faff1c69f7cc5b289e461e363515a5)
