二氧化氯
来自维基百科,自由的百科全书
二氧化氯(英語:Chlorine dioxide)是一種無機化合物 ,化學式 ClO2 。它在 11 °C 以上是一種黃綠色氣體,在 −59 °C 到 11 °C 之間是一種紅棕色液體,更低溫下是橙色的固體。 它是一種氧化劑,能夠將氧轉移到各種基質上,同時通過氧化還原反應獲得一個或多個電子。 它進入水時不水解,通常作為水溶液中的溶解氣體處理。 二氧化氯的潛在危害包括健康問題,爆炸性和可燃性。 [5]它常用於漂白劑。二氧化氯是氯的最穩定的氧化物,也是唯一大量生產的鹵素氧化物[6]。
| 二氧化氯 | |||
|---|---|---|---|
| |||

| |||

| |||
| IUPAC名 Chlorine dioxide | |||
| 識別 | |||
| CAS編號 | 10049-04-4 | ||
| PubChem | 24870 | ||
| ChemSpider | 23251 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | OSVXSBDYLRYLIG-UHFFFAOYAC | ||
| Gmelin | 1265 | ||
| EINECS | 233-162-8 | ||
| ChEBI | 29415 | ||
| RTECS | FO3000000 | ||
| MeSH | Chlorine+dioxide | ||
| 性質 | |||
| 化學式 | ClO2 | ||
| 莫耳質量 | 67.45 g·mol−1 | ||
| 外觀 | 黃色氣體 | ||
| 氣味 | 辛辣 | ||
| 密度 | 2.757 (液體)[1]g·mL-1 | ||
| 密度 | 3.04 (氣體)kg·m-3 | ||
| 熔點 | -59 °C(214 K) | ||
| 沸點 | 11 °C(284 K) | ||
| 溶解性(水) | 8 g dm-3(20 °C) | ||
| 蒸氣壓 | >1 atm[2] | ||
| pKa | 3.0(5) | ||
| 熱力學 | |||
| ΔfHm⦵298K | 104.60 kJ mol-1 | ||
| S⦵298K | 257.22 J K-1 mol-1 | ||
| 危險性 | |||
| MSDS | ICSC 0127 | ||
| 歐盟編號 | 017-026-00-3 | ||
| H-術語 | H271, H314, H300+310+330, H372 | ||
| P-術語 | P210, P220, P280, P283, P260, P264, P271, P284, P301+310, P304+340, P306+360, P305+351+338, P371+380+375, P403+233 | ||
| NFPA 704 | |||
| PEL | TWA 0.1 ppm (0.3 mg/m3)[2] | ||
| 致死量或濃度: | |||
LD50(中位劑量)
|
94 mg/kg (大鼠口服) [3] | ||
LCLo(最低)
|
260 ppm (大鼠,2小時)[4] | ||
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |||
二氧化氯是在1811年首次製備,廣泛的用在造紙業以及飲用水處理中。近期也將二氧化氯應用在食品處理、住所和車輛消毒、除黴、空氣消毒及去異味、游泳池水處理、牙醫消毒以及傷口清潔上。
二氧化氯被廣泛用於消毒及殺毒。但近來有人利用二氧化氯進行詐騙,將二氧化氯宣傳為可治療多種疾病(包括兒童自閉症[7]及COVID-19[8][9][10])的食用藥物。有兒童為治療自閉症而接受二氧化氯的灌腸,以致危及性命[7]。美國食品藥品監督管理局(FDA)提出除了在牙科醫師監督下用二氧化氯清洗口部之外,其餘食用二氧化氯或在體內使用二氧化氯的作法對身體沒有好處,不應該使用[11][12]。
製備方法
| 製備型態 | 備註 | 產物特性 |
|---|---|---|
| 酸製法:
5ClO2− + 4H+ → 4ClO2 + 2H2O + Cl− 5NaClO2 + 4HCl → 4ClO2(aq) + ClO3− |
在酸性環境中反應可產生氯酸根離子,反應速率緩慢。 |
1.需要與進料幫浦連結。 2.產量限制:25~30 lb/day。 3.最大有效產率約80%。 |
| 液氯-亞氯酸鈉:
Cl2 + H2O →HOCl/ HCl HOCl/ HCl+ NaClO2 → ClO2 + H/OCl− + ClO3− + NaOH |
在酸性環境中反應可能產生氯酸根離子反應速率稍慢,須加過量氯和酸與NaOH中和。 |
1.流出液呈酸性(pH~2.8-3.5)。 2.產量限制:~1000 lb/day。 3.最大有效產率約80-92%。 |
| 液氯-亞氯酸鈉 (循環式):
2HOCl + 2NaClO2 → 2ClO2 + Cl2 + 2NaOH |
須加過量氯和酸與NaOH中和飽和液,氯在與亞氯酸鈉混合前須先經過在循環反應槽。 | |
| 液氯-亞氯酸鈉溶液 (真空式):[13]
NaClO2(aq)+ Cl2(g) → ClO2(aq)+NaCl |
在中性環境中反應反應速度快速,氯氣與25%亞氯酸鈉溶液經噴射器注入真空式反應槽,無須幫浦輔助。 |
1.產量5-120000 lb/day。 2.流出液呈中性。 3.低餘氯產生量(<2%)。 4.最大有效產率約95-99%。 5.須維持內壓至少40 psig。 |
| 氯氣-固態亞氯酸鈉:[13]
NaClO2(s) + Cl2(g) → ClO2(aq) + NaCl |
反應速度快速。
氯氣經氮氣或過濾後,空氣稀釋後再參與反應,可產生~8%二氧化氯蒸汽。 |
1.最大有效產率約>99%。 2.總產量>10000 lb/day。 |
| 電化學法:
ClO2− → ClO2 + e− [14] |
電解25%亞氯酸鈉溶液。 | |
| 氯酸根離子還原法:[15]
2NaClO3 + H2O2 + H2SO4 → 2ClO2 + Na2SO4 + 2H2O + O2 |
在酸性環境中反應。 |
二氧化氯是一種與稀釋物質分離時會劇烈分解的化合物。因此,通常優選涉及不經過氣相而製備溶液的製備方法。二氧化氯必須以安全的方式安排處理。
在實驗室, ClO2 可以由亞氯酸鈉和氯氣化合而成:[13]
- 2 NaClO2 + Cl2 → 2 ClO2 + 2 NaCl
傳統上,消毒劑應用中的二氧化氯是由亞氯酸鈉或亞氯酸鈉-次氯酸鈉方法製成的:
- 2 NaClO2 + 2 HCl + NaOCl → 2 ClO2 + 3 NaCl + H2O
或是亞氯酸鈉–鹽酸法:
- 5 NaClO2 + 4 HCl → 5 NaCl + 4 ClO2 + 2 H2O
或是亞氯酸鹽–硫酸法:
- 4 ClO−
2 + 2 H2SO4 → 2 ClO2 + HClO3 + 2 SO2−
4 + H2O + HCl
這三種方法均可以產生具有高亞氯酸鹽轉化率的二氧化氯。與其他方法不同,亞氯酸鹽-硫酸法可生產完全不含氯的二氧化氯,要生產等量的二氧化氯,其亞氯酸鹽的含量要多25%。此外,過氧化氫可有效地用於小規模的應用。[15]
- 2 KClO3 + 2 H2C2O4 → K2C2O4 + 2 ClO2 + 2 CO2 + 2 H2O
- 2 KClO3 + H2C2O4 + 2 H2SO4 → 2 KHSO4 + 2 ClO2 + 2 CO2 + 2 H2O
今天,超過 95% 的二氧化氯是由氯酸鈉還原而成, 用於木漿漂白。 它可以在強酸溶液中以合適的還原劑(例如甲醇,過氧化氫,鹽酸或二氧化硫)反應高效生產。 [15]現代技術基於甲醇或過氧化氫,因為這些化學方法可實現最佳經濟性,並且不會產生氯氣。 它的反應可以寫為:[16]
- 氯酸鹽 + 酸 + 還原劑→ 二氧化氯 + 副產物
作為一個典型示例,人們認為氯酸鈉與鹽酸在單個反應器中的反應通過以下途徑進行:
- ClO−
3 + Cl−
+ H+
→ ClO−
2 + HOCl - ClO−
3 + ClO−
2 + 2 H+
→ 2 ClO
2 + H
2O - HOCl + Cl−
+ H+
→ Cl
2 + H
2O
總反應為:
- 2 ClO−
3 + 2 Cl−
+ 4 H+
→ 2 ClO
2 + Cl
2 + 2 H
2O.
商業上更重要的生產路線使用甲醇作為還原劑,並使用硫酸進行酸度調節。 不使用基於氯化物的工藝的兩個優點是它不會形成有害的氯氣,而副產物硫酸鈉對製漿廠而言是一種有價值的化學品。 這些基於甲醇的方法可提供很高的效率,並且非常安全。 [15]
自1999年以來,由於使用氯酸鹽,過氧化氫和硫酸進行的工藝生產效率高,因此已越來越多地用於水處理和其他小規模的消毒劑應用。
高純二氧化氯可以由亞氯酸鹽的電解而成:[14]
- 2 NaClO2 + 2 H2O → 2 ClO2 + 2 NaOH + H2
氣固法可產生高純度的二氧化氯氣體(空氣或氮氣中為7.7%),該方法使稀氯氣與亞氯酸鈉固體反應: [14]
- 2 NaClO2 + Cl2 → 2 ClO2 + 2 NaCl
性質

二氧化氯是一種電中性的氯化合物。 它的結構和性質都和氯氣有很大的差別。[15]二氧化氯有著高水溶性,尤其是在冷水中。 二氧化氯不會水解,有著氯氣溶解度的10倍[15],但在光照條件下會在水中發生歧化:6ClO₂+3H₂O→HCl+5HClO₃
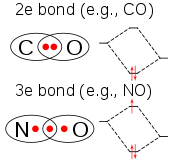
ClO2 的價電子數量是奇數,因此它是順磁性的自由基。它的電子結構一直困擾著化學家,因為沒有一種路易斯結構令人滿意。 1933年,L.O.Brockway提出了一種涉及三電子鍵的結構。 [17]化學家萊納斯·鮑林進一步發展了這個想法,並得出了兩個共振結構,它們的一面是雙鍵,另一面是單鍵加三電子鍵。 [18]在鮑林的觀點中,後一種組合應該是比雙鍵稍微弱的鍵。 在分子軌域理論中,如果將第三個電子置於反鍵軌域上,這種想法是常見的。 後來的工作證實了HOMO確實是一個不完全填充的反鍵軌域。 [19]
二氧化氯化學分子式為ClO2,分子質量為67.452。在常溫下為一種黃綠色到橙色的氣體,沸點為11°C,熔點為-59°C 。當二氧化氯含量達到 14~17 ppm時,一般人就會察覺到它的存在,而濃度達到 45 ppm時,對於嗅覺感官會產生刺激性傷害。二氧化氯具有強氧化的特性,若以其他氧化劑相比,其標準電位值約在1.50伏特之間。而二氧化氯在水中的四個主要氧化還原反應為電中性化合物。在飲用水消毒中,亞氯酸鹽 (ClO2−) 是主要反應的產物,有70%是由二氧化氯轉換,其餘則為氯酸鹽 (ClO3−) 及氯化物 (Cl−) 。而二氧化氯對於微生物的殺菌效用,不受高pH、氨水、含氮化合物及有機化合物的影響,不會引起溴化物 (次溴酸) 及提供有機溴化合物的組成。
存放性質
在壓力超過 10 kPa[15](或STP下空氣中氣相濃度大於10%的體積)下,ClO2 可能會猛烈地爆炸,分解形成氯氣 和氧氣。 分解可以通過光,熱點,化學反應或壓力衝擊來引發。因此,二氧化氯氣體絕不會以濃縮形式處理,而是幾乎總是以0.5至10克/升的濃度範圍溶解在水中作為溶解氣體。 它的溶解度在較低的溫度下會增加,因此,當以高於3克/升的濃度存儲時,通常使用冷水(5℃)。 在許多國家,例如美國,二氧化氯氣體可能不會以任何濃度輸送,並且幾乎總是使用二氧化氯發生器在現場產生。 [15]在某些國家,濃度低於3克/升的二氧化氯溶液可以通過陸路運輸,但是它們相對不穩定,並且變化的速度很快。
純度與產製之規範標準
美國國家環境保護署(Environmental Protection Agency,縮寫:EPA)對二氧化氯各種製備有明確規定純度必須大於95%,餘氯量最好小於2%,生成產量、氯殘留量及純度的計算公式,如下公式所列:
A.產量計算公式:
- Yield=[ClO2]× 100% ÷[ClO2]+[ClO2−]+ ()[ClO3−]
ClO2− ÷ ClO3−之平均分子量比值為 (),濃度單位為ppm。
B.氯的殘留量計算公式:
- Excess Cl2=[Cl2]× 100% ÷[ClO2]+[ClO2−]+ ()[ClO3−]× ( × 67.45)
Cl2 ÷ ClO2−之平均分子量比值為 × 67.45,上式在純度公式中以FAC表示。藉此可以了解反應是否完全。
C.純度計算公式:
- Purity=[ClO2]×100% ÷[ClO2]+[FAC]+[ClO2−]+[ClO3−]
二氧化氯的消毒殺菌機制
二氧化氯本身是一種高選擇性的氧化劑,其殺菌作用機制會依作用物質不同而有不同的反應路徑。由於其具有強氧化能力,幾乎百分之百以分子態存在,除了利用其特殊的單一電子轉移機制,而釋放出新生態的氧原子,利用氧原子本身的強氧化作用及滲透壓差,穿透細菌細胞膜以抑制其呼吸作用,並使磷酸轉移酶失去活性,影響其代謝,藉以殺滅細菌。也可透過將葡萄糖氧化酶 (如硫氫氧化酶) 之雙硫鍵氧化,破壞其鍵結,使蛋白質失去活性,讓細菌無法生存。
一般而言,使用化學藥劑的殺菌消毒機制,可分成下列四種 :
- 破壞細菌及病毒的細胞壁,使其不能分裂生長。
- 傷害其細胞壁的滲透性,而使之無法吸收養分,分泌物無法排出。
- 使其蛋白質變性、凝固,進而喪失其機能。
- 使產生能量的酵素受損,失去活性,進而影響其代謝。
分析方法
一般針對氧化劑這類反應速率極快之化學物質,分析方法之選擇依據常為靈敏度的高低、干擾物質的嚴重性及方法的簡易性。因此當氣態二氧化氯溶入於水中時,該二氧化氯溶液極易因操作環境等因素而使得溶液中同時存在有氯、二氧化氯、氯酸根離子及亞氯酸根離子,因此於二氧化氯之濃度與純度分析上較氯之分析來得複雜。基於二氧化氯不穩定之物化特性,於取樣分析之過程中需特別注意避免發生擾動而造成曝氣情形導致二氧化氯揮發溢散,亦需同時有妥善之遮光保存以避免因光照而發生二氧化氯光解反應。由於二氧化氯以高濃度之溶液狀態進行儲備時,亦易因環境因素而有自解並濃度下降之趨勢,因此建議應於產製過程即時量測較為準確,如無可避免需進行儲備時,因妥善避光並儲存於低溫環境,同時於取用時均需重複量測該儲備液之濃度值。以下就水中二氧化氯濃度之分析方法簡述。而國際上所採用之二氧化氯分析方式屬碘滴定法(五步碘量法)之一,係依據Aieta等人於1984年所提出同時測定水中氯、二氧化氯、氯酸根離子及亞氯酸根離子之方法。
「五步碘量法」原理:ClO2、Cl2、ClO2−和ClO3− 有自己最適合與I−反應的pH值,藉以硫代硫酸鈉標準溶液滴定游離的I2,以區分出ClO2、Cl2、ClO2−和ClO3−,如下表所示:
| 化學反應 | pH值範圍 | 添加試劑 |
|---|---|---|
| 2ClO2 + 2I− → I2 + 2ClO2− | =7.0~8.5 | 磷酸緩衝溶液 |
| Cl2 + 2I− → I2 + 2Cl− | <7.0~8.5 | 磷酸緩衝溶液 |
| 2ClO2 + 10I− + 8H+ → 5I2 + 2Cl− + 4H2O | ≦2.0 | 2.5N HCl溶液 |
| ClO2− + 4I−+4H+ → 2I2 + Cl− + 2H2O | ≦2.0 | 2.5N HCl溶液 |
| ClO3− + 6I−+6H+ → 3I2 + Cl− + 3H2O | ≦0.1~0.5 | 2.5N HCl溶液 |
從上表中可見,當pH值=7.0~8.5時,ClO2轉移1莫耳的電子被還原為ClO2−,相當於ClO2被還原為1/5 (按終產物Cl−計);當pH值<7.0~8.5條件下,Cl2會被I−還原為Cl−。在pH值≦2.0時,ClO2轉移5莫耳的電子,完全被I−還原為Cl− (包含原有的ClO2−和ClO2轉化成ClO2−的剩下4/5都被還原)。而pH值≦0.1~0.5時,I−還原全部的ClO3−轉變為Cl− (包括Cl2、ClO2和ClO2−等)。
用途
- 二氧化氯是一種人工製造出來的氣體,對細菌、病毒、黴菌的細胞壁有較強的吸附和穿透能力,能抑制蛋白質合成,達到抑菌、殺菌效果,而且是一種對環境、人體和動物比較友善的綠色消毒劑,通常用在自來水消毒,也是合法的食品用洗潔劑。[20]
- 二氧化氯的主要用途在自來水的消毒,和麵粉與木質紙漿的漂白。[21][22]:4-1[23]
- 作為消毒劑,由於其獨特的品質,二氧化氯即使在低濃度下也有效。[15][22]
- 由於它能氧化及分解蛋白質,能很有效地對抗病毒、細菌和包括梨形鞭毛蟲(學名:Giardia lamblia)與隱孢子蟲(Cryptosporidium)等原生動物所引起的囊腫與卵囊。
- 從1956年比利時的布魯塞爾把自來水消毒劑由氯氣改成二氧化氯後,二氧化氯開始被廣泛地使用。
- 台灣國立屏東科技大學研發團隊研發出超高純度99%與極高濃度3000ppm之二氧化氯相關產品,可對於大環境髒汙細菌汙染進行99%徹底殺菌。[24]。
- 2005年8月,在襲擊紐奧良的颶風卡崔娜過後,二氧化氯就被用來清除被洪水淹沒後房屋上的危險黴菌。而中華民國政府也於2006年3月6日預告二氧化氯為自來水消毒劑。[1]
- 近年也有應用於空調系統及空氣清新機的濾網,以為較多人使用的空間進行空氣消毒殺菌。
- 香港科技大學研究團隊研發出以有機微膠囊包裹二氧化氯的技術(Germagic),透過微膠囊慢慢釋放二氧化氯分子,可長效殺滅及抑制細菌病毒生長[25]。
有時將二氧化氯與氯結合用於木漿的漂白,但在ECF(無氯元素)漂白過程中單獨使用。它在中等酸性(pH3.5至6)下使用。二氧化氯的使用使所產生的有機氯化合物的量最小化。[26]目前,二氧化氯(ECF技術)是全球最重要的漂白方法。 所有漂白的牛皮紙中約有95%是使用二氧化氯按ECF漂白順序生產的。[27]
尼亞加拉瀑布城水處理廠於1944年首次使用二氧化氯進行飲用水處理,以銷毀產生味道和氣味的酚。 [22]:4-17[23]1956年,比利時的布魯塞爾-首都大區從氯氣改為二氧化氯,將二氧化氯作為飲用水消毒劑大規模使用。 [23]它在水處理中最常見的用途是作為飲用水氯化之前的氧化劑,以破壞天然水的有機雜質,否則這些雜質會在接觸游離氯氣時產生三鹵甲烷。 [29][30][31]三鹵甲烷是致癌的消毒副產物 [32],它的產生與水中自然含有的有機物的氯化反應有關。 [31]在pH 7以上操作時,二氧化氯優於氯氣, [22]:4-33 它也可以在氨和胺的存在下用於控制供水系統中的生物膜。 [31]二氧化氯在許多工業水處理應用中用作殺菌劑,包括冷卻塔,工藝用水和食品加工。 [33]
二氧化氯作為氧化劑或消毒劑時有許多用途。 [15]二氧化氯可用於空氣消毒, [34]並且是2001年美國炭疽攻擊事件後用於美國建築物淨化的主要試劑。[35]在紐奧良,路易斯安那和周圍的墨西哥灣沿岸發生2005年颶風卡特里娜災難之後,都會使用二氧化氯清除被淹沒的房屋中危險的黴菌。 [36]
在COVID-19大流行時,美國國家環境保護局已發布了許多符合其針對病原體COVID-19的環境措施標準的消毒劑清單。 [37][38]儘管每種產品使用不同的配方,但有些是基於可被轉化為二氧化氯的亞氯酸鈉。 EPA清單上的許多其他產品均包含次氯酸鈉(英語:Sodium hypochlorite),其名稱相似,但不應與亞氯酸鈉(英語:Sodium chlorite)混淆,因為它們具有非常不同的化學作用方式。
二氧化氯可以用作熏蒸劑處理,以消毒諸如發霉和發酵的藍莓,樹莓和草莓等水果。 [39]
二氧化氯可用於在屠宰家禽後通過噴霧或浸泡將其消毒。 [40]
二氧化氯可以用於內視鏡的消毒,例如商品名為Tristel的產品。 [41]它也可以三者組合使用,其中包括預先用表面活性劑進行預清洗,然後用去離子水和低濃度的抗氧化劑沖洗。 [42]
二氧化氯被用作氧化劑,以破壞廢水流中的酚,並用於控制動物副產品(提煉)工廠的空氣洗滌器中的氣味。 [22]:4-34 它也可以用作汽車和船上的除臭劑,並被水活化並在船上或汽車中過夜放置,從而產生二氧化氯。
安全性
二氧化氯是有毒的,因此需要限制其接觸以確保其安全使用。 美國環境保護署已將飲用水中的二氧化氯的最高含量定為0.8毫克/升。[44]美國勞工部的機構職業安全與健康管理局(OSHA)已將空氣中二氧化氯的8小時允許暴露極限設置為(0.3 mg/m3)[45]
2010年7月30日以及2010年10月1日,美國食品藥品監督管理局都警告不要使用產品神奇礦物溶液(MMS)。該產品必須按照說明進行配製產生二氧化氯。MMS已被推銷為多種疾病的治療方法,包括HIV,癌症,自閉症和痤瘡。FDA警告告知消費者MMS可能對健康造成嚴重傷害,並表示已收到大量關於因脫水引起的噁心、腹瀉、嚴重嘔吐和危及生命的低血壓的報道。[46][47]此警告於2019年8月12日第三次重複,於2020年4月8日第四次重複,指出攝入MMS與喝漂白劑相同,並敦促消費者不要出於任何原因使用它們或將這些產品送給孩子。[12]
該化合物已被欺詐性地用於治療多種疾病,包括兒童自閉症[7]。一些人也聲稱可飲用二氧化氯溶液以預防及治療COVID-19[48][9][10]。但需在水溶液下才能殺滅,也不能服用及接觸皮膚。一些人聲稱能殺滅COVID-19的配戴式產品含有二氧化氯,但其效能存疑[49]。[需要可靠醫學來源] 被認為是治療兒童自閉症的方法之一:用二氧化氯對兒童進行灌腸已經發現可以危及生命。 [7] 美國食品藥品監督管理局(FDA)指出,二氧化氯的攝入或其他內部使用(除了可能在牙醫監督下進行的口腔沖洗以外)對健康沒有好處,並且出於任何原因都不得在身體內部使用[11][12]。
二氧化氯的灌腸被認為可以治癒兒童時期的自閉症,導致許多人對FDA投訴稱其威脅生命,[50]甚至死亡。[51]二氧化氯被標記為多種品牌名稱,包括但不限於MMS、Miracle Mineral Solution、CD protocol。[52]二氧化氯的醫學特性沒有科學依據,且FDA已警告不要使用二氧化氯。[12][53]
參考資料
擴展閱讀
外部連結
Wikiwand - on
Seamless Wikipedia browsing. On steroids.





