玻璃轉化(glass transition)又稱玻璃化轉變,是玻璃-液體轉變(glass-liquid transition)的簡稱,是指非晶材料或在非晶區的半晶材料,隨著溫度的升高,由硬而脆且光亮透明的玻璃態逐漸轉變為黏性或橡膠態的漸進可逆轉變,亦即「玻璃態-高彈態轉變」。而具有玻璃轉化的非晶態固體,則稱為玻璃。藉由過冷使黏性液體呈玻璃態的反向轉變,稱為玻璃化。
玻璃轉化溫度(glass transition temperature, Tg)是玻璃態物質在玻璃態和高彈態之間相互可逆轉化的溫度。當溫度低於Tg時,因分子鏈無法運動,這時材料處於剛硬的「玻璃態」;當溫度高於Tg時,無定形狀態的分子鏈會開始做局部運動,材料會呈現類似橡膠般柔軟可撓的性質。
玻璃轉化表現出二級相變的表現,物質的熱容會發生連續的變化,但是玻璃轉化實際上是一個動力學轉化,因此玻璃轉化溫度的具體數值是與溫度變化的速度相關。常見的玻璃態物質有大部分的高分子材料和玻璃等等,在工業上有重要應用的玻璃態物質還有玻璃態金屬[1]。
溫度也是決定無定形高分子材料是堅硬或者是柔軟的因素:若 Tg > 室溫,則高分子材料是堅硬的;若 Tg < 室溫,則高分子材料是柔軟的。
簡介
液體向類固體狀態的玻璃化轉變可能隨著冷卻或壓縮而發生。[2] 這種轉變使得材料黏度在500 K的溫度範圍內平滑地增加高達17個數量級,而沒有明顯的材料結構變化。[3] [4] 與凍結或結晶相反,後者是Ehrenfest分類中的一級相變,體積、能量和黏度等熱力學和動力學性質會發生不連續性變化。在許多通常發生凍結轉變的材料中,如果快速冷卻,就容易在較低的溫度下導致玻璃化轉變。其他一些材料,如許多聚合物,缺乏明確定義的晶態,容易形成玻璃體,即使在非常緩慢的冷卻或壓縮下也是如此。材料在淬火時形成玻璃的傾向稱為玻璃形成能力。這種能力取決於材料的組成,並且可以通過剛度理論來預測。[5]
在轉變溫度範圍以下,玻璃態結構不會根據所用的冷卻速率而鬆弛。玻璃態的膨脹係數大致等同於晶態固體的膨脹係數。如果使用較慢的冷卻速率,結構鬆弛(或分子間重排)發生的時間增加,可能導致更高密度的玻璃產品。類似地,通過退火(從而允許緩慢的結構鬆弛),玻璃結構隨時間趨向於與該溫度下過冷液體相對應的平衡密度。Tg位於玻璃態的冷卻曲線與過冷液體之間的交點處。[3] [6][7][8][9][10]
在這個溫度範圍內,玻璃的構型隨著時間慢慢地向平衡結構變化。[11] 吉布斯自由能最小化的原理提供了最終變化所必需的熱力學驅動力。在比Tg稍高的溫度下,物質可以很容易地轉化成任何溫度下的平衡相對應的結構。相反,在比Tg低得多的溫度下,玻璃的構型很長的時間內保持相當穩定。
因此,液體-玻璃轉變不是熱力學平衡狀態之間的轉變。一般認為,真正的平衡狀態總是晶態,玻璃則是處於動力學鎖定狀態,其熵、密度等取決於熱過程。因此,玻璃轉變主要是一種動態現象。在一定程度上,時間和溫度在處理玻璃時是可互換的量,這一事實常常表現為時間-溫度疊加原理原理。在冷卻液體時,內部自由度逐漸脫離平衡。然而,是否存在一個在無限長弛豫時間的假設極限下的潛在的二級相變,這是一個長期存在的爭論。[12][13][14][15]
在一個較新的玻璃轉變模型中,當溫度降低時,液體矩陣中最大的空隙會收縮,直到小於元素或其部分的最小截面,這時的溫度就是玻璃轉變溫度。由於液體矩陣受到熱能的不斷擾動,振動的諧波會不斷改變,導致元素之間形成一些暫時的空洞(「自由體積」),它們的數量和大小與溫度有關。這樣定義的玻璃轉變溫度Tg0是一種只取決於壓力的無序(非晶)狀態的固定特性。由於分子矩陣在接近Tg0時慣性增大,達到熱平衡的時間也會逐漸延長,因此通常用來測量玻璃轉變溫度的方法往往會得到偏高的Tg值。一般來說,測量時設置的溫度變化速率越慢,測得的Tg值就越靠近Tg0。[16] 可以用動態力學分析等技術來測量玻璃轉變溫度。[17]
玻璃化轉變溫度Tg

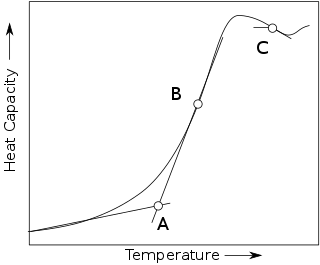
參考右下角的圖,它繪製了比熱容隨溫度的變化。在這個背景下,Tg是曲線上點A對應的溫度。[18]
玻璃化轉變溫度Tg有不同的操作定義,其中一些被認可為公認的科學標準。然而,所有的定義都有主觀性,可能會得到不同的數值結果:最好的情況是,對於給定物質的Tg值僅相差幾個開爾文。一種定義是根據黏度,將Tg固定在1013泊(或1012Pa·s)的值。實驗證明,這個值接近許多玻璃的退火點。[19]
與黏度相反,無機玻璃的熱膨脹、比熱容、剪切模量和許多其他性質在玻璃化轉變溫度處顯示出相對突然的變化。任何這樣的階躍或拐點都可以用來定義Tg。為了使這個定義可重複,必須指定冷卻或加熱速率。
最常用的Tg定義使用加熱時釋放能量的差示掃描量熱法(DSC,見圖)。通常,樣品先以10 K/min的速度冷卻,然後以相同的速度加熱。
還有一種定義Tg的方法是使用膨脹法(又稱熱膨脹)中的拐點:參考右上角的圖。這裡,常用的加熱速率是3–5 K/min。玻璃化轉變溫度以下和以上的線性部分用綠色表示。Tg是紅色回歸線交點處的溫度。[18]
下面總結了某些材料類別的特徵Tg值。
| 材料 | Tg (°C) | Tg (°F) | 商業名稱 |
|---|---|---|---|
| 輪胎橡膠 | −70 | −94[20] | |
| 聚偏二氟乙烯 (PVDF) | −35 | −31[21] | |
| 聚丙烯(無規立構) (PP atactic) | −20 | −4[22] | |
| 聚偏二氟乙烯 (PVF) | −20 | −4[21] | |
| 聚丙烯(全同立構) | 0 | 32[22] | |
| 聚3-羥基丁酸酯 (PHB) | 15 | 59[22] | |
| 聚醋酸乙烯酯 (PVAc) | 30 | 86[22] | |
| 聚三氟氯乙烯 (PCTFE) | 45 | 113[21] | |
| 尼龍 (PA) | 47—60 | 117—140 | Nylon-6,x |
| 聚乳酸 (PLA) | 60—65 | 140—149 | |
| 聚對苯二甲酸乙二酯 (PET) | 70 | 158[22] | |
| 聚氯乙烯 (PVC) | 80 | 176[22] | |
| 聚乙烯醇 (PVA) | 85 | 185[22] | |
| 聚苯乙烯 (PS) | 95 | 203[22] | |
| 聚甲基丙烯酸甲酯 (PMMA atactic) | 105 | 221[22] | Plexiglas, Perspex |
| ABS樹脂 (ABS) | 105 | 221[23] | |
| 聚四氟乙烯 (PTFE) | 115 | 239[24] | Teflon |
| 聚碳酸酯 (PC) | 145 | 293[22] | Lexan |
| 聚碸 | 185 | 365 | |
| 聚降冰片烯 | 215 | 419[22] |
乾燥的尼龍-6的玻璃化轉變溫度為47 °C(117 °F)。[25] 乾燥狀態下的尼龍-6,6的玻璃化轉變溫度約為70 °C(158 °F)。[26][27] 而聚乙烯的玻璃化轉變範圍為−130至−80 °C(−202至−112 °F)[28] 以上只是平均值,因為玻璃化轉變溫度取決於冷卻速率和分子量分布,而且可能受添加劑的影響。對於半晶態材料,如室溫下為60–80%晶態的聚乙烯,玻璃化轉變溫度是指材料冷卻時非晶部分發生轉變的溫度。
Kauzmann悖論

當液體過冷時,液相和固相之間的熵差會減小。通過將過冷液體在其玻璃化轉變溫度以下的比熱容外推,可以計算出熵差為零的溫度。這個溫度被命名為Kauzmann溫度。[3]
如果一個液體可以在其Kauzmann溫度以下過冷,並且實驗上也顯示出比晶體相更低的熵,就會引起Kauzmann悖論。[31][32]
解決Kauzmann悖論的一種方法是說,在液相的熵降低之前,必須發生一個相變。在這種情況下,轉變溫度被稱為熱測定理想玻璃轉變溫度 T0c。在這種觀點中,玻璃轉變不僅僅是一種動力學效應,不僅僅是熔體快速冷卻的結果,而且還有一個潛在的熱力學基礎。玻璃轉變溫度:
1958年的Gibbs–DiMarzio模型[33]具體預測了過冷液體的構型熵在極限時消失,此時液體的存在區域結束,其微結構與晶體的相同,它們的性質曲線在一個真正的二級相變中相交。由於實現足夠慢的冷卻速率、避免意外結晶十分困難,這一點從未得到實驗驗證。1965年的Adam–Gibbs模型[34]提出了一個解決Kauzmann悖論的方法,根據這個方法,在Kauzmann溫度處弛豫時間發散,意味著人們永遠不能在這裡平衡亞穩態過冷液體。2009年給出了一個關於Kauzmann悖論和Adam–Gibbs模型的批判性討論。[35]幾種過冷有機液體的有關數據並沒有證實Adam–Gibbs預測的在任何有限溫度下(例如Kauzmann溫度)處弛豫時間發散。[36]
至少有三種其他可能解決Kauzmann悖論的方法。一種可能是,當過冷液體接近Kauzmann溫度時,其比熱容平滑地降低到一個較小的值。另一種可能是,在Kauzmann溫度之前,物質發生一個一級相變到另一種液態,這種新狀態的比熱容小於從高溫外推得到的值。最後,Kauzmann本人通過假設所有過冷液體在達到Kauzmann溫度之前必須結晶,來解決熵悖論。
特定材料
二氧化矽(SiO2)除了石英結構外,還有許多不同的晶體形式。幾乎所有的晶體形式都涉及四面體SiO4單元,通過「共享頂點」以不同的方式排列(斯石英由連接的SiO6 八面體組成,是主要的例外)。Si-O鍵長在不同的晶體形式中有所不同。在α-石英中,鍵長為161皮米(6.3×10−9英寸),而在α-鱗石英中,它的範圍為154—171 pm(6.1×10−9—6.7×10−9英寸)。Si-O-Si鍵角也從α-鱗石英中的140°變化到α-石英中的144°,再到β-鱗石英中的180°。任何偏離這些標準參數的微觀結構差異或變化都代表了一種接近非晶、玻璃或玻璃態固體的結構。
在矽酸鹽中,玻璃轉變溫度Tg與在非晶(或隨機網絡)共價鍵晶格中斷裂和重新形成共價鍵所需的能量有關。Tg受玻璃化學成分的影響。向二氧化矽玻璃中添加硼、鈉、鉀或鈣等化合價小於4的元素,有助於打散網絡結構,從而降低Tg。另一方面,5價的磷有助於加強有序晶格,從而提高Tg。[37] Tg與鍵強度成正比,它取決於鍵的准平衡熱力學參數,例如鍵的焓Hd和熵Sd:
Tg = Hd / [Sd + R ln[(1 − fc)/ fc]
其中R是氣體常數,fc是滲透閾值。對於強熔體,如SiO2,上式中的滲透閾值是3D空間中的通用Scher–Zallen臨界密度,即fc = 0.15,但對於脆性材料,滲透閾值是材料依賴的,且fc << 1。[38]鍵的Hd和熵Sd可以從可用的黏度實驗數據中得到。
在聚合物中,玻璃轉變溫度Tg,通常表示為能令吉布斯自由能超過使得50個左右的重複單元協同運動的活化能的溫度。這使得分子鏈在受到力的作用時可以相互滑動。從這個定義中,我們可以看到引入相對剛性的化學基團(如苯環)會阻礙流動,從而提高Tg。[39] 由於這種效應,熱塑性塑料的剛度降低。當達到玻璃轉變溫度時,剛度保持不變一段時間,接近E2,直到溫度超過Tm,材料熔化。這個區域被稱為橡膠平台。

從低溫端來看,在玻璃轉變溫度Tg處,剪切模量下降了幾個數量級。Alessio Zaccone和Eugene Terentjev開發了一個分子水平的數學關係,用於描述從低溫段接近Tg時聚合物玻璃的溫度依賴的剪切模量。[40] 即使剪切模量並沒有真正降到零(它下降到了橡膠平台的較低值),在Zaccone–Terentjev公式中也將剪切模量設為零,由此得到了一個關於Tg的表達式,它恢復了弗洛里-福克斯方程,並且還表明Tg與玻璃態的熱膨脹係數成反比。這種方法提供了另一種操作來定義聚合物玻璃的Tg思路:測量剪切模量迅速下降至橡膠平台的溫度。
在熨燙中,織物被加熱,發生玻璃-橡膠轉變,使得聚合物鏈變得活動。然後來自熨斗的力施加了一個優先的排布方向。通過向聚合物基質中添加增塑劑可以顯著降低Tg。增塑劑的較小分子嵌入到聚合物鏈之間,增加了間距和自由體積,使它們即使在較低的溫度下也能相互滑動。增塑劑的添加可以有效地控制聚合物鏈的動力學,由於主要改變的是自由體積的大小,新詞聚合物末端移動性增加不明顯。[41]向聚合物中添加非反應性側鏈也可以使鏈相互遠離,降低Tg。如果一個具有一些理想性能的塑料有一個過高的Tg,有時可以與另一個在共聚物或複合材料中與具有低於預期使用溫度的Tg的塑料結合。注意,有些塑料在高溫下使用(例如在汽車發動機中),而有些在低溫下使用。[22]

在粘彈性材料中,液態行為的存在取決於材料的性質,因此隨著施加載荷的速率而變化。某些矽橡膠玩具可以根據施加力的時間速率表現出不同的行為:慢慢拉時流動,表現為高黏度的液體;用錘子敲時碎裂,表現為玻璃態。
在冷卻時,橡膠發生了「液態-玻璃轉變」,也被稱為「橡膠-玻璃轉變」。
玻璃化的力學機制
凝聚態物質中的分子運動可以用一個傅立葉級數來表示,其物理解釋由不同方向和波長的原子位移的縱波和橫波的疊加組成。在單原子系統中,這些波被稱為「密度波」。(在多原子系統中,它們也可能包括組成波。)[42]
因此,液體中的熱運動可以分解為基本的縱向振動(或聲學聲子),而橫向振動(或剪切波)最初只在表現出高度有序晶體態的彈性固體中存在。換句話說,簡單液體不能支持以剪切應力形式施加的力,並且會通過宏觀塑性變形(或粘性流動)產生機械屈服。此外,固體在保持其剛度的同時局部變形——而液體在受到剪切力作用時產生宏觀粘性流動——這是兩者之間的機械區別。[43][44]
然而,Frenkel在他對固體運動論和液體彈性理論的修正中指出了這個結論的不足。這個修正直接來源於當轉變沒有伴隨著結晶時,從液態到固態的粘彈性交叉的連續特徵——即過冷粘性液體。因此,我們看到了橫向聲子(或剪切波)和玻璃化過程中剛度密切相關,這一點Bartenev已在他對玻璃化過程的力學描述中說明。[45][46] 因此可以用低頻剪切模量的消失或顯著降低來定義玻璃轉變,這一點在Zaccone和Terentjev[40]的工作中聚合物玻璃的例子上得到了定量的展示。事實上,推動模型規定,弛豫時間的活化能與高頻平台剪切模量成正比,[3][47]這個量在冷卻時增加,從而解釋了玻璃形成液體中弛豫時間的普遍非阿倫尼烏斯溫度依賴性。
凝聚態物質中的縱向聲子的速度直接決定了熱導率,它消除了可壓縮性和熱膨脹之間的溫度差異。Kittel提出,玻璃的行為可以用晶格聲子的「平均自由程」來解釋,這個值與液體或固體的分子結構中的無序程度的數量級相當。將一些玻璃形成體的熱聲子平均自由程或弛豫長度與玻璃轉變溫度繪製在一起,表明兩者之間存在線性關係。這提示了一個基於聲子平均自由程的值的玻璃形成新準則。[48]
人們經常認為,在介電固體中,熱傳導是通過晶格的彈性振動來實現的,而這種傳導受到晶格缺陷(例如隨機分布的空位)對聲子的彈性散射的限制。[49] 這些預測被商業玻璃和玻璃陶瓷的實驗所證實,其中平均自由程顯然受到「內部邊界散射」的限制,長度尺度為10—100微米(0.00039—0.00394英寸)。[50][51] 有學者提出,這些聲子之間的相關性的出現導致了玻璃形成液體中局部剪切應力的定向有序或「凍結」,從而產生了玻璃轉變。[52]
在討論液態金屬的電阻時,熱聲子及其與電子結構的相互作用是一個重要的內容。Lindemann的熔化理論提出,[53] 從晶體態到液態的過渡中導電性下降是由於導電電子因原子振動幅度增加而增加的散射作用。這樣理論已經應用於金屬玻璃的電導率,其中電子的平均自由程非常小(與原子間距相當)。[54][55]
從熔體中用飛濺淬火法製備金矽合金的非晶態形式進一步考慮了基於金屬鍵性質對玻璃形成能力的影響。[56][57][58][59][60]
其他的工作表明,動態聲子的存在增強了局部電子的遷移率。反對這種模型的一個主張是,如果化學鍵很重要,那麼近自由電子模型就不適用。然而,如果這個模型包括了所有原子對之間的電荷分布,就像化學鍵一樣(例如,矽,當一個能帶剛好被電子填滿時),那麼它應該適用於固體。[61]
因此,如果電導率很低,那麼電子的平均自由程就很短。電子只會對玻璃中的短程有序敏感,因為它們沒有機會與距離較遠的原子發生散射。由於玻璃和晶體中的短程有序是相似的,所以電子能量應該在這兩種狀態下是相似的。對於電阻率較低和電子自由程較長的合金,電子可能開始感知到玻璃中存在無序結構,這會提高它們的能量並使玻璃相對於結晶不穩定。因此,某些合金的玻璃形成傾向的部分可能是電子的平均自由程非常短,所以只有短程有序對電子能量才重要。
還有人認為,玻璃形成與不同原子之間相互作用勢的「軟度」有關。一些作者強調玻璃和相應晶體的局部結構之間的強烈相似性,認為化學鍵有助於穩定非晶結構。[62][63]
其他人則認為,電子結構通過鍵的方向性特徵對玻璃形成產生影響。非晶態性因此在具有多種晶形和高度鍵各向異性的元素中更容易出現,暗示了周期表中的族數與不同元素固體中的玻璃形成能力之間的關係。[64]
參考文獻
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.

