氮族元素的氢化物
氮族元素與氫的化合物 来自维基百科,自由的百科全书
氮族元素的氢化物,又称磷属化氢[1](英语:hydrogen pnictides)是由氢原子与氮族元素原子(氮、磷、砷、锑、铋或镆)构成的化合物,是一种氢二元化合物。
氮族元素的三氢化物
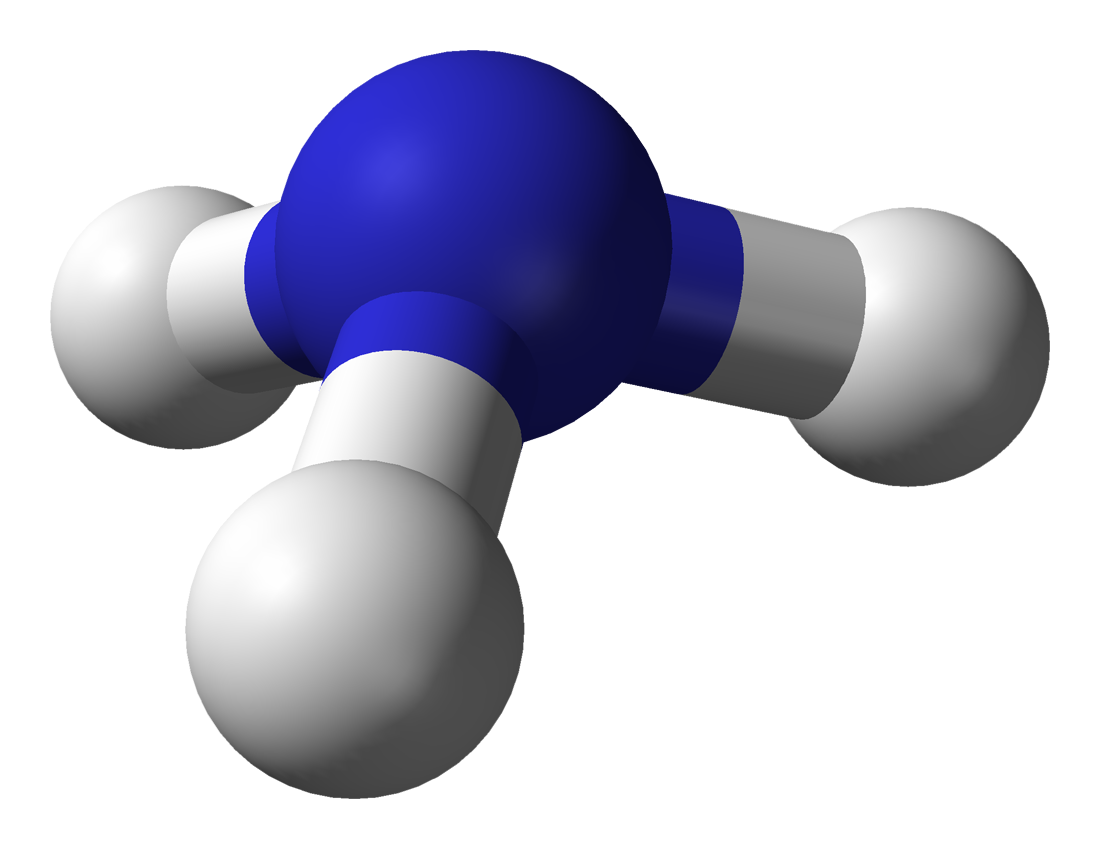
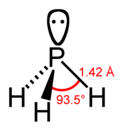
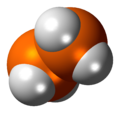
最简单的氮族元素氢化物由三个氢原子与一个氮族元素原子化合而成,其化学式通常计为XH3,少数情况下会计做H3X,其中X表示任何一种氮族元素。这些分子的结构都是三角锥形分子构型(有别于硼族元素的三氢化物的平面三角形分子构型)且皆具有极性。
这些三氢化物最稳定的是氨,而位于周期表越下方的越不稳定,且具有毒性。
氮族元素的三氢化物的性质如下[4]:
| 性质 | 氮化氢(氨) | 磷化氢(膦) | 砷化氢(胂) | 锑化氢(䏲) | 铋化氢(䏟) |
|---|---|---|---|---|---|
| 化学式 | NH3 | PH3 | AsH3 | SbH3 | BiH3 |
| 熔点 (°C) | −77.8 | −133.5 | −116.3 | −88 | ? |
| 沸点 (°C) | −34.5 | −87.5 | −62.4 | −18.4 | 16.8 (推测) |
| 液体密度 (g/cm3) | 0.683 (−34 °C) | 0.746 (−90 °C) | 1.640 (−64 °C) | 2.204 (−18 °C) | ? |
| ΔH° f/kJ mol−1 |
−46.1 | +5[5] | +66.4 | +145.1 | +277.8 |
| 键长 (X–H)/pm | 101.7 | 141.9 | 151.9 | 170.7 | 177.59 |
| 键角 H–X–H | 107.8° | 93.6° | 91.8° | 91.3° | 90.48°[6] |
氮族元素三氢化物还可以再被质子化成化学式形如XH4+的𬭩离子,且为四面体形分子:
-2价氮族元素的氢化物
参见
参考文献
Wikiwand - on
Seamless Wikipedia browsing. On steroids.