热门问题
时间线
聊天
视角
二茂铁
一种化合物 来自维基百科,自由的百科全书
Remove ads
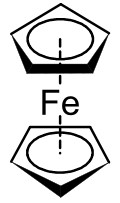
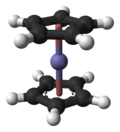
二茂铁(英文:Ferrocene,简写Fc),或称环戊二烯基铁,是分子式为Fe(C5H5)2的有机金属化合物,在室温会微量升华而带有似樟脑的特殊气味。二茂铁是最重要的金属茂基配合物,也是最早发现的夹心配合物[1],包含两颗环戊二烯负离子以π电子与铁原子成键。
Remove ads
制备
二茂铁可用很多方法制备,常用的包括令环戊二烯基钠与氯化亚铁在四氢呋喃中反应:
- FeCl2+2NaC5H5 → 2NaCl+Fe(C5H5)2
另一种方法是氯化亚铁与环戊二烯在三乙胺、二乙胺等碱溶液反应:
- FeCl2+2C5H6+2Et3N → Fe(C5H5)2+Et3NHCl
历史


二茂铁的发现纯属偶然。1951年,杜肯大学的Pauson和Kealy用环戊二烯基溴化镁处理氯化铁,试图得到二烯氧化偶联的产物富瓦烯(Fulvalene,如图),但却意外得到了很稳定的橙黄色固体。[2]当时他们认为二茂铁的结构并非夹心,而是如右图所示,并把其稳定归因于芳香的环戊二烯基负离子。与此同时,Miller、Tebboth和Tremaine在将环戊二烯与氮气混合气通过一种还原铁催化剂时也得到该橙黄色固体。[3]
罗伯特·伯恩斯·伍德沃德和杰弗里·威尔金森,[4]及恩斯特·奥托·菲舍尔[5]分别独自发现了二茂铁的夹心结构,且后者还在此基础上开始合成二茂镍和二茂钴。NMR光谱和X射线晶体学的结果也证实了二茂铁的夹心结构。[6][7]二茂铁的发现展开了环戊二烯基与过渡金属的众多π配合物的化学,也为有机金属化学掀开新帷幕。
1973年慕尼黑大学的恩斯特·奥托·菲舍尔及伦敦帝国学院的杰弗里·威尔金森爵士获授诺贝尔化学奖,以表彰他们在有机金属化学领域的杰出贡献。
Remove ads
电子结构
穆斯堡尔谱学数据显示,二茂铁中心铁原子氧化态为+2,每个茂环有一单位负电荷。每个环有6颗π电子,符合休克尔规则中4n+2电子数的要求(n为非负整数),每个环都芳香。每个环的6颗电子*2,再加上二价铁离子的6颗d电子正好等于18,符合18电子规则,非常稳定。
二茂铁两个茂环可以是重叠(D5h),也可以是错位(D5d),两者间的能垒仅有每摩8至20kJ。重叠构型可能较稳定,但在晶体中分子间作用能在数量级上与能垒差不多大或略大些,所以各种各样的构型都可存在。[8]
物理性质
二茂铁是对空气稳定的橙黄色固体,在真空和加热时迅速升华。和其他对称且不含电荷的物质类似,二茂铁可溶于苯等大多数有机溶剂,但不溶于水。
二茂铁在100°C时显著升华。下表列出一些重要的蒸气压数据及相应温度值:[9]
化学性质
二茂铁有芳香化合物的显著特征,可与亲电试剂反应生成二茂铁的取代衍生物。大多数取代的类型是1-取代物、1,1'-二取代物及1,2-二取代物(带“'”表示在A环上,不带则表示在B环上)。如二茂铁与三氯化铝和Me2NPCl2在热庚烷中反应生成二氯二茂铁膦(Dichloroferrocenyl phosphine),[10]当与苯基二氯化膦在类似条件下反应得到P,P-二氯双(二茂铁)-P-苯基膦。[11]与苯甲醚类似,二茂铁与P4S10反应生成Dithiadiphosphetane disulfide。[12]二茂铁不可以直接硝化和卤化,因为会先氧化(参见#氧化还原反应)。
二茂铁可起傅-克反应,如有磷酸催化时,二茂铁与乙酸酐或乙酰氯反应生成乙酰基二茂铁。

虽然一方面二茂铁许多反应类似于芳香烃的相应反应,但另一方面有些反应明显是铁原子在起主要作用,[8]如在亲电取代反应中,亲电试剂看上去是先进攻铁原子:

Remove ads
用丁基锂可很快夺取二茂铁的质子,产物为1,1'-二锂代二茂铁,是很强的亲核试剂。它与二乙基二硫代氨基甲酸硒反应,生成的产物有位阻,两颗环戊二烯基配体靠硒原子连接。[13]该产物可藉加热开环聚合反应(ROP)生成聚硒化二茂铁(Poly(ferrocenyl selenide)),硅和磷的类似反应也可合成相应聚合物Poly(ferrocenylsilane)和Poly(ferrocenylphosphine)。[14][15]

二茂铁在酸性溶液很易氧化为蓝色顺磁性的二茂铁𬭩离子[(η5-C5H5)2FeIII]+,其电势以饱和甘汞电极为标准大约为0.5V。产物二茂铁不太活泼且易于分离,该离子有时用作氧化剂,以六氟磷酸盐[PF6]−或氟硼酸盐[BF4]−的形式存在。[16]环上不同的取代基会改变该电势值:吸电子基(如羧基)提升电极电势值;而给电子基(如甲基)则降低该值,氧化变易。全甲基二茂铁氧化后生成的盐[Fe(η5-C5Me5)2][tcne](tcne为四氰乙烯)有不寻常的磁性,[17]为深绿色晶体,有阳离子与阴离子交替出现的长链。
二茂钌和锇的类似阳离子[MIII(η5-C5H5)2]+却不稳定,易继续氧化为[MIV(η-C5H5)2]2+阳离子或二聚成为[(η5-C5H5)2MIII-MIII(η5-C5H5)2]2+。[18]
二茂铁及衍生物的应用
二茂铁自身的应用并不多,但用已知的方法可以合成出种类繁多的衍生物,大大延伸了二茂铁的应用范围。
二茂铁及其衍生物是汽油中的抗震剂,它们比曾经使用过的四乙基铅安全得多。[19]在英国的哈尔福斯Halfords可以买到含二茂铁的汽油添加剂,它尤其适用于以前专为四乙基铅抗震剂设计的车辆。[20]二茂铁分解出的铁沉积在火花塞表面,使其更导热。
添加二茂铁同样也可以减少柴油车冒出的煤烟。
某些二茂铁的盐类有抗癌活性,如他莫昔芬的二茂铁同类物,[21]其机理为,他莫昔芬可以与雌激素结合,其细胞毒性可以杀死癌细胞。[22][23][24]
衍生物

五羰基铁与环戊二烯在高压釜中于135°C反应得到深红紫色晶体的双核络合物环戊二烯基羰基铁[Fe(η5-C5H5)(CO)2]2,它对空气和水都稳定。结构测定表明该化合物中两组成桥羰基及两块铁原子共平面,且有铁-铁键。环戊二烯基羰基铁很易制备,且在有机合成中有广泛应用。[8]
参考资料及注释
延伸阅读
外部链接
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads