二硫化碳
化合物 来自维基百科,自由的百科全书
二硫化碳是一种分子式为CS2的无色有毒液体。纯的二硫化碳有类似氯仿的芳香甜味,但是通常不纯的工业品因为混有其他硫化物(如羰基硫等)而变为微黄色,并且有令人不愉快的烂萝卜味。CS2可溶解硫单质或白磷。
| 二硫化碳 | |
|---|---|

| |
| |
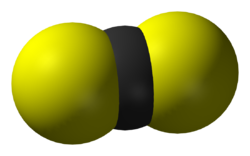
| IUPAC名 Carbon disulfide | |
| 识别 | |
| CAS号 | 75-15-0 |
| PubChem | 6348 |
| ChemSpider | 6108 |
| SMILES |
|
| InChI |
|
| InChIKey | QGJOPFRUJISHPQ-UHFFFAOYAS |
| UN编号 | 1131 |
| EINECS | 200-843-6 |
| ChEBI | 23012 |
| RTECS | FF6650000 |
| KEGG | C19033 |
| 性质 | |
| 化学式 | CS2 |
| 摩尔质量 | 76.1 g·mol⁻¹ |
| 外观 | 无色液体 不纯时带黄色 |
| 密度 | 1.26 g/cm³ |
| 熔点 | -111.6 °C (161.6 K) |
| 沸点 | 46 °C (319 K) |
| 溶解性(水) | 0.2 g/100 ml (20 °C) |
| 危险性 | |
| 欧盟危险性符号 | |
| 警示术语 | R:R11-R23/24/25-R48 |
| 安全术语 | S:S16-S33-Template:S44-S53 |
| NFPA 704 | |
| 闪点 | -30 °C |
| 自燃温度 | 90 °C |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
由于二硫化碳结构简单,虽然它的分子中含有碳原子,但是被认为是无机物。
二硫化碳通过以下反应制备:
- 2CH4 + S8 → 2CS2 + 4H2S
化学性质
二硫化碳易燃,加热至一定温度甚至可以自燃:
- CS2 + 3 O2 → CO2 + 2 SO2
二硫化碳可以和硫化钠溶液反应,形成三硫代碳酸钠:
- CS2 + Na2S → Na2CS3
用途
二硫化碳可以用来制备四氯化碳,这也是四氯化碳生产的重要方法:[1]
这个反应经过中间体硫光气(CSCl2)。
参考资料
Wikiwand - on
Seamless Wikipedia browsing. On steroids.




