四氧化三錳
化合物 来自维基百科,自由的百科全书
| 四氧化三錳[1] | |
|---|---|
| |
| IUPAC名 Manganese(II) dimanganese(III) oxide | |
| 別名 | 氧化錳(II,III) 黑錳礦 |
| 識別 | |
| CAS號 | 1317-35-7 |
| PubChem | 14825 |
| SMILES |
|
| RTECS | OP0895000 |
| 性質 | |
| 化學式 | Mn3O4 MnO·Mn2O3 |
| 摩爾質量 | 228.8118 g·mol⁻¹ |
| 外觀 | 暗紅色、褐色至黑色無臭粉末 |
| 密度 | 4.86 g/cm3 |
| 熔點 | 1567 °C |
| 沸點 | 2847 °C[2] |
| 溶解性(水) | 不溶於水 |
| 溶解性(其他) | 溶於鹽酸 |
| 危險性 | |
| 歐盟分類 | 有害 (Xn) |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
性質
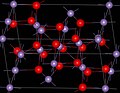
四氧化三錳是一種黑色四方結晶,經灼燒成結晶,屬於尖晶石類,離子結構為 ,其中二價和三價錳離子分佈在兩種不同的晶格位置上。氧離子為立方緊密堆積,二價錳離子佔四面體空隙,三價錳離子佔八面體空隙。溫度1443K以下時四氧化三錳為變形的四方晶系尖晶石結構,變形原因為姜-泰勒效應;1443K以上則為立方尖晶石結構。[3]
製備
1、由金屬錳或錳氧化物(如二氧化錳)、氫氧化物、碳酸鹽、亞硫酸鹽、硫酸鹽、硝酸鹽及高錳酸鹽在空氣或氧氣中於1000°C灼燒,經冷卻、粉碎製得。[3]
2、二氧化錳或水錳礦先焙燒成三氧化二錳,再在甲烷存在下,於250~500°C進一步被還原為四氧化三錳。[3]
用途
四氧化三錳主要用於電子工業,用作軟磁鐵氧體的生產原料、電子計算機中存儲信息的磁芯、磁盤和磁帶、電話用變壓器和高品質電感器、電視回掃變壓器、磁記錄用磁頭、電感器、磁放大器、飽和電感器、天線棒等。此外也用作塗料和油漆的色料。[3]
四氧化三錳可用作很多反應的催化劑,例如甲烷和一氧化碳的氧化反應[8][9]、一氧化氮的分解反應[10]、硝基苯的還原反應[11]以及有機物的催化燃燒[12]等。
參考資料
Wikiwand - on
Seamless Wikipedia browsing. On steroids.




