碳酸鋇
化合物 来自维基百科,自由的百科全书
碳酸鋇(化學式:BaCO3),由於其較容易從自然礦物中獲取,且有毒性,故有被稱作毒重石。碳酸鋇是一種不溶於水的白色沉澱,是一種常見的無機鹽。
此條目需要補充更多來源。 (2022年1月12日) |
| 碳酸鋇 | |
|---|---|
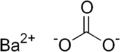
| |
| 別名 | 毒重石 |
| 識別 | |
| CAS號 | 513-77-9 |
| PubChem | 10563 |
| ChemSpider | 10121 |
| SMILES |
|
| InChI |
|
| InChIKey | AYJRCSIUFZENHW-NUQVWONBAT |
| UN編號 | 1564 |
| EINECS | 208-167-3 |
| RTECS | CQ8600000 |
| 性質 | |
| 化學式 | BaCO3 |
| 摩爾質量 | 197.336 g·mol⁻¹ |
| 外觀 | 白色粉末 |
| 密度 | 4.2865 g/cm3 (固) |
| 熔點 | 811 °C |
| 沸點 | 1450 °C |
| 溶解性(水) | 0.002 g/100 ml (20 °C) |
| 相關物質 | |
| 其他陰離子 | 硫酸鋇、氯化鋇 |
| 其他陽離子 | 碳酸鍶、碳酸鈣 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
形態
通常,碳酸鋇有α、β、γ三種結晶形態,而其工業品則為白色粉末。
γ型在811°C時會轉化為β型,β型在982°C時轉換為α型,在9.09MPa時,α型的熔點為1740°C,而在常壓加熱到1450°C時,碳酸鋇就會分解而成氧化鋇和二氧化碳。
溶解性
化學反應
- 分解反應:碳酸鋇會在高溫下分解,反應式:
- BaCO3 → BaO + CO2↑
- 與酸反應:
- 在遇到酸時的一般反應式:
- BaCO3 + 2H+ → Ba2+ + H2O + CO2↑
- 與稀硫酸反應時會生成不可溶於酸的硫酸鋇白色沉澱:
- BaCO3 + H2SO4 → BaSO4 + H2O + CO2↑
毒性
碳酸鋇是一種劇毒品,會引起急性和慢性中毒。因為鋇是重金屬,碳酸鋇能與胃液中的鹽酸反應,釋放出鋇離子,引起中毒反應。
當發生嚴重的急性中毒時,會出現急性胃腸病變、肌肉腱反射消失、痙攣、肌肉麻痹等症狀。
毒性:
- 口服
- 大鼠 LD50:418mg/kg
- 小鼠 LD50:200mg/kg
對於碳酸鋇急性中毒的患者,通常採取洗胃、灌腸、服用催吐劑等措施使碳酸鋇排出體外。
同時也可以通過服用硫酸鉀與碳酸鋇反應,能使有毒的鋇變為不溶性硫酸鋇沉澱,減輕毒性。之所以使用硫酸鉀,是因為碳酸鋇中毒可能會導致低血鉀症。參見鋇
- TLV-TWA 0.5mg/m3
- STEL 0.5mg/m3
用途
參考資料
外部連結
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
