热门问题
时间线
聊天
视角
有機鋅化合物
来自维基百科,自由的百科全书
Remove ads
有機鋅化合物是指含有碳-鋅化學鍵的一類有機化合物。有機鋅化學是一門研究有機鋅化合物理化性質、合成和反應的學科。[1][2][3][4]

第一個被發現和製備的有機鋅化合物是二乙基鋅(Diethylzinc)(由愛德華·弗蘭克蘭於1849年發現)。它還是第一個被發現具有金屬-碳σ鍵的化合物。許多有機鋅化合物都是易燃的而難以操作的(大多數有機溶劑同樣可燃而存在安全隱患)。有機鋅化合物大多易於氧化,且溶於質子性溶劑時會發生分解。在許多反應中,有機鋅試劑都需要現制現用而不能被分離純化或存放太久。所有使用有機鋅試劑的反應都需要在惰性氣體保護下進行,如氮氣或氬氣。
有機鋅化合物最常見的氧化態為+2價。它可以被分為三種類型:有機鋅鹵化合物(R-Zn-X,其中X代表鹵素原子);二烴基鋅化合物(R-Zn-R,其中R代表烷基或芳基);鋅酸鋰鹽或鋅酸鎂鹽(M+R3Zn-,其中M代表鋰或鎂)。
由於碳和鋅元素的電負性不同:(碳為2.55;鋅為1.65),碳-鋅化學鍵的極性指向碳原子。二烴基鋅化合物通常以單體形態存在,而有機鋅鹵化合物則可通過鹵素鍵橋形成聚合形態,該形態類似於格氏試劑和格氏試劑的的Schlenk平衡(Schlenk equilibrium)。
Remove ads
合成
下列為一些合成有機鋅化合物的方法:
- 氧化加成。最早由Frankland發現的二乙基鋅即是用該法製備:在氫氣的「保護」下,將碘乙烷和單質鋅進行加成反應(該反應還稱為:Frankland synthesis)。金屬鋅的活性可以通過Rieke鋅(Rieke zinc)試劑得到增強,而該試劑是金屬鉀和氯化鋅發生還原反應得到的。
- 2RI + 2Zn → ZnR2 + ZnI2
- 鹵鋅交換。該法主要分為兩種:為碘鋅交換和硼鋅交換。第二個反應(右向左)的第一步為烯烴的硼氫化。
Remove ads
反應
在下列許多反應中,有機鋅化合物都作為中間體參與反應:
- 於1863年發現的Frankland-Duppa反應中,草酸酯(ROCOCOOR)和鹵代烷烴R'X、鋅和鹽酸反應,生成α-羥基羧酸酯RR'COHCOOR[8]
- 雷福爾馬茨基反應通過鋅鹵中間體轉化α-鹵代酯和醛得到β-羥基酯。
- 西蒙斯–史密斯反應中,卡賓(碘甲基)碘化鋅和烯烴反應得到環丙烷。
- 乙炔負離子(Acetylides)鋅鹽的反應。
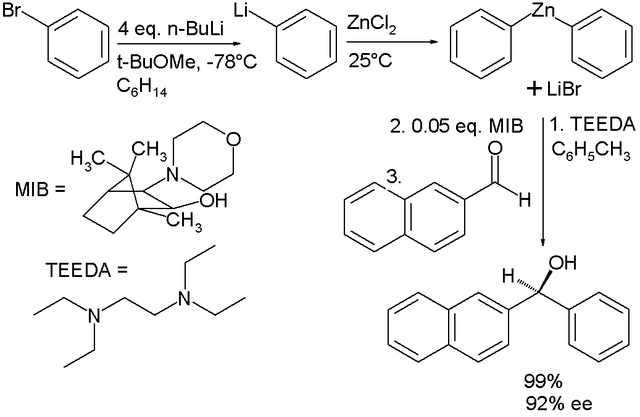
- 有機鋅試劑對於羰基的加成反應。1899年發現的Barbier反應使用鋅代替鎂進行格氏加成反應,而該反應更溫和;反應條件更簡單。有機鹵鎂試劑進行加成反應時,任何水的存在將導致反應無法進行;然而Babier反應甚至能夠在水存在下進行反應。有機鋅試劑的劣勢在於親核性弱于格氏試劑。在所有12族元素中,鋅是最具活性的。商業可售的二烴基鋅化合物包括:二甲基鋅、二乙基鋅和二苯基鋅。這些試劑價格都昂貴且難於操作和控制。在一項研究中,[9][10] 活性有機鋅化合物可通過更廉價的有機溴化合物(Organobromine)前體獲得:
Remove ads
有機鋅酸鹽
史上第一個酸根型配位化合物(Ate complex)('有機鋅酸鹽)由James Alfred Wanklyn於1858發現,[11] 金屬鈉和二乙基鋅有助於反應進行。
- 2Na + 3 Et2Zn -> 2Et3Zn-Na+ + Zn
2007年報道了通過調整反應條件,鋅酸鹽可反應為氫化絡合乙基鋅酸鈉鹽(氫原子作為橋聯配體),最終得到其中一個乙基發生β-氫消除(β-hydride elimination)的產物:[12]
一價有機鋅化合物
具有鋅-鋅鍵的低價有機鋅化合物也已被發現,第一個該類化合物為2004年報道的二(五甲基環戊二烯)基鋅(Zn2(η5–C5Me5)2)。[13]
參見
- 鋅化合物
- 含碳並有其他元素的化合物,見元素周期表:
參考文獻
外部連結
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads