氯金酸
化合物 来自维基百科,自由的百科全书
氯金酸也稱為四氯合金酸,是分子式為H[AuCl4]的無機化合物。
| 氯金酸 | |
|---|---|
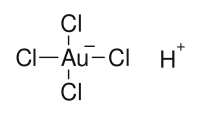
| |

| |
| 別名 | 四氯合金酸 |
| 識別 | |
| CAS號 | 16903-35-8 |
| ChemSpider | 26171 |
| SMILES |
|
| InChI |
|
| InChIKey | IXPWAPCEBHEFOV-ACHCXQQJAP |
| 性質 | |
| 化學式 | HAuCl4 |
| 摩爾質量 | 339.785 g/mol (無水) 393.833 g/mol (三水) 411.85 g/mol (四水) g·mol⁻¹ |
| 外觀 | 金黃色晶體 潮解 |
| 密度 | 3.9 g/cm3 (四水) |
| 熔點 | 254°C |
| 溶解性(水) | 可溶 |
| 溶解性 | 可溶於乙醇、乙醚 |
| 危險性 | |
| 歐盟危險性符號 [1] | |
| 警示術語 | R:R22, R36, R37, R38[1] |
| MSDS | JT Baker |
| 歐盟分類 | 未列出 |
| NFPA 704 | |
| 相關物質 | |
| 其他陰離子 | 溴金酸 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
製備及結構
- Au + HNO3 + 4 HCl → H[AuCl4] + NO↑ + 2 H2O
加熱時,氯金酸會分解為氯化氫及三氯化金,此反應是可逆反應,因此將三氯化金溶解在鹽酸中也可產生氯金酸。
- AuCl3 + HCl⇌H[AuCl4]
化學性質
氯金酸會被大部分的金屬所還原,還原反應的速度很快,還原後的產物是元素態的金。
氯金酸能夠表現出較強的氧化性。
氯金酸被二甲硫醚還原後會生成二甲硫醚氯化亞金,也常用來生成其他的含金配合物[4]。
氯金酸和氨或銨鹽反應,可以得到灰色且具有強爆炸性的「雷金」,它被認為是Au2O3·3NH3和HNAuCl·NH3的混合物。過量氨和這種混合物反應,產生Au(OH)3·3NH3,用熱水處理得到Au2O3·2NH3。[5]
應用
在利用沃爾威爾法精煉金時,會使用氯金酸為電解質。
膠體金及金的納米顆粒一般可由檸檬酸鈉還原氯金酸溶液來製備,也可用其他的程序來製備奈米金,例如燙金過程使用的Norrish反應及乙醛還原反應[6]。
參考資料
拓展閱讀
Wikiwand - on
Seamless Wikipedia browsing. On steroids.


