多碘離子(英文:Polyiodide)指的是由多個碘原子組成的多原子陰離子,是多聚鹵素陰離子的一類。多碘化物指含有多碘離子的化合物。
製備
將單質碘溶解於碘化物溶液中,就能得到多碘化物的溶液,其中多數是 I3−(三碘陰離子):
室溫下,I3− 和 I5− 在水溶液中的穩定常數為:
- ,
- ,
過量的碘與碘化鉀長時間加熱攪拌反應時,可以得到組成近似為 KI4 的多碘化物,其中的碘都是一樣的,可以與 KI 中的碘發生同位素交換反應。
將比計量稍微過量的碘加入碘化四甲基銨的乙醇溶液中,加熱攪拌使其溶解,然後緩慢冷卻,可以析出深紅色的三碘四甲基銨針狀晶體 NMe4I3。如果用過量數倍的碘,則得到深綠色單斜晶系的五碘四甲基銨針狀晶體 NMe4I5。將少量的上述晶體溶於大量水中,用有機溶劑如二氯甲烷萃取,然後用硫代硫酸鈉滴定產生的碘(不斷振盪溶液,終點無色),便可得知晶體中的多碘離子種類。(第41屆IChO實驗預備試題第1題)
性質
多碘離子的通式為 Imn−,一般m為奇數,n為1,形成諸如 I3−、I5−、I7− 之類的單陰離子。但是也有少數例外,例如 Cs2I8 中,就含有 I82− 離子。最簡單的多碘離子是三碘離子(I3−)。目前合成的最複雜的多碘離子是 I164− 離子,存在於深藍色針狀晶體 R2H2I8 中(R+ 為質子化的可可鹼),於1869年由S. M. Jorgensen首先製備出來。X射線衍射顯示該離子為中心對稱的平面結構,形狀類似於「己」字,不過上下兩橫只有中間一橫的一半長。[1]
多碘離子在非水溶劑中的穩定性要比在水中的穩定性高。例如25°C時,I3− 在水溶液中的生成穩定常數為710,而在丙酮中為108.3,在硝基乙烷中為106.7,在1,2-二氯乙烷中為107。對於相同陽離子的三鹵化物,總體上講,陰離子中心原子半徑越大,形成的陰離子對稱性越高,則該三鹵離子穩定性也越高。然而,多鹵化物在溶劑中的行為是複雜的,以乙腈、丙酮和硝基甲烷作溶劑時,三鹵離子的穩定性為:,與在水中的恰好相反。
對於含有同一多碘離子的化合物,陽離子體積越大,該多碘化物也越穩定。一般常用的陽離子有:Cs+、NR4+(R=烷基,如NMe4+)和AsPh4+,它們與多碘離子可以形成穩定的化合物,有一定的晶形,可以從溶劑中析出。
結構
這些多碘離子都看作是由 I−、I2 和 I3− 單位形成的,其結構中,I-I-I 鍵角一般接近90°或180°,I-I 距離也一般都比碘分子中的 I-I 鍵長。根據成鹽環境的不同,多碘離子的對稱性會有不同,從而使同一離子的鍵長和鍵角產生差異,這是由於鹵素原子本身性質不同,而且陽離子對多碘離子在空間上存在影響,使其產生程度不同的偏離。
一些多碘離子的結構如下:

- I3− 離子:近似直線型結構。在晶體 [NEt4]I7 和 [AsPh4]+I3− 中,I3− 離子是直線型的;但在 CsI3、Cs2I8 和 NH4I3 中,I3− 離子卻是不對稱的。
- I5− 離子:一般為平面V型結構,可看成是兩個 I2 向一個 I− 配位。[2]該離子中存在碘原子p軌道的相互作用。[3]
- I7− 離子:由中心對稱的 I3− 離子和 I2 分子組成的三維骨架結構,其中每個 I3− 離子緊連4個 I2 分子,而每個 I2 分子緊連2個 I3− 離子,I3− 和 I2 之間有強烈的相互作用。
- I9− 離子:為扭曲的h型,非平面結構。
- I42− 離子:直線型([I-I-I-I]2− 或 [I…I-I…I]2−)。[4]兩種模型中,I-I鍵總鍵長大致相等。
- I82− 離子:
 |
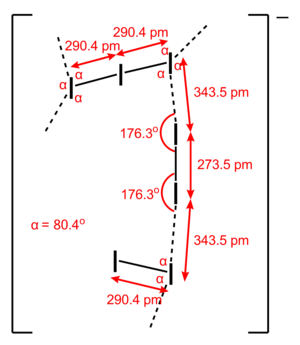 |
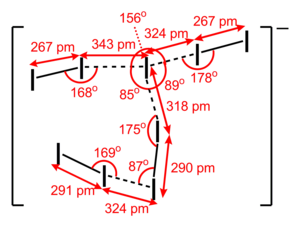 |
 |
參見
參考資料
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.




