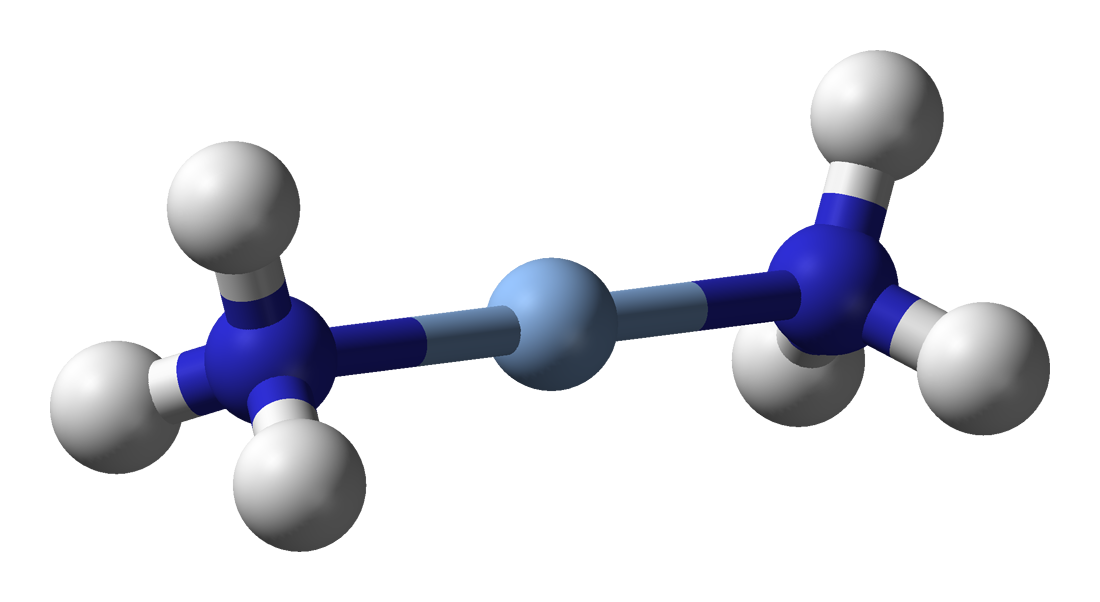
銀氨溶液,又稱氫氧化二氨合銀,俗稱苛性銀,是含有二氨合銀(I)錯離子([Ag(NH3)2]+)的水溶液,一般由硝酸銀或其他銀化合物與氨水反應製取,溶於水中能夠完全解離出氫氧根離子,故屬於強鹼,具腐蝕性。

([Ag(NH3)2]+)的球棍模型。

19世紀德國化學家伯恩哈德·多侖發現銀氨溶液遇醛反應一段時間後,會形成「漂亮且閃亮的銀鏡」(ein sehr schön glänzender Silberspiegel),也就是金屬銀,可作為檢驗醛的試劑[1],因此銀氨溶液也常被稱為多侖試劑(英語:Tollens' reagent,又譯多倫試劑、吐倫試劑或土倫試劑),而其和醛反應而析出銀的過程後來則被稱為銀鏡反應。
製備
銀氨溶液不可能在市面上買到,因為它的保質期太短了,只能在實驗室現用現配。
- 向大概0.1mol的硝酸銀溶液中加入幾滴氫氧化鈉稀溶液,此時氫氧化鈉中的氫氧根離子會把銀水配合物變成棕色的氧化銀沉澱。
- 向溶液中滴加飽和的氨水,直至棕色沉澱剛好溶解。此時產生了銀氨絡合物,所得的溶液即為銀氨溶液,含[Ag(NH3)2]NO3(aq)。而氫氧化鈉就被恢復回來了。
反應方程式為:
- 2 AgNO3 + 2 NaOH → Ag2O (s) + 2 NaNO3 + H2O
- Ag2O (s) + 4 NH3 + 2 NaNO3 + H2O → 2 [Ag(NH3)2]NO3 + 2 NaOH
也可以直接向硝酸銀溶液中滴加氨水,至沉澱恰好完全溶解。[2]
滴加氫氧化鈉時首先產生白色的氫氧化銀沉澱,非常不穩定,立即分解為棕色的氧化銀和水。硝酸銀也可由一些不溶的銀鹽代替,但製備時不需加入氫氧化鈉,直接加入氨水將不溶物溶解即可。
用途
銀氨溶液與斐林試劑類似,具有微弱的氧化性,在自身被還原後,會在容器內壁附着上一層光亮的銀層,即是所謂的銀鏡反應。一般用銀鏡反應來鑑定醛的存在,相應的氧化產物是羧酸根離子,酸化得到羧酸。甲醛或甲酸可被徹底氧化為二氧化碳。

銀氨溶液與2,4-二硝基苯肼(Brady試劑)連用可以檢出樣品中醛基官能團的存在。若樣品與2,4-二硝基苯肼作用呈陽性,產生黃色或紅色的二硝基苯腙沉澱,則可證明樣品為羰基化合物,可能是醛或酮。由於醛具還原性,而酮不具有還原性,此時再用銀氨溶液測試,便可區分這二者官能團,醛將銀氨溶液還原而產生銀鏡。此方法對醛糖和酮糖也基本有效。
銀氨溶液在組織病理解剖的豐塔納-馬森法(英語:Fontana-Masson Stain)中被用來檢測組織切片裡的脂褐素、黑色素和嗜銀細胞。黑色素和嗜鉻細胞會把硝酸銀還原成金屬銀。[2]
銀氨溶液也被用作在玻璃器具上鍍銀,如在真空保溫瓶的內膽上塗銀層。所用還原劑是帶醛基的葡萄糖,要想鍍銀效果良好,需先清潔玻璃器具。為加快金屬銀的沉澱速度,沉澱對象玻璃需要先在穩定的氯化亞錫的鹽酸溶液中預處理。[3]
在要儘可能高質量的鏡面上——如望遠鏡的主鏡,用氯化亞錫鍍銀就會產生納米級的凹凸,並降低鏡面的反射效果。[4][5]給主鏡鍍銀需要加添加劑,如使用馬丁法(英語:Martin's Method),添加含酒石酸和酒精的添加劑。[5]
安全
銀氨溶液應現配現用,並且使用後立即加鹽酸銷毀,還可利用銀離子的氧化性與一些強還原劑如羥胺等反應以回收銀單質(這也是分析化學中鹽酸羥胺的應用範圍)。它在儲存時會轉化為強爆炸性的黑色含銀不溶物(成分是氮化銀 Ag3N[6][7]),通常時間為一至三天,但天氣炎熱時數小時便會生成[8]
參考來源
外部連結
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.