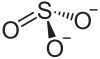
亞硫酸鋇是鋇的亞硫酸鹽,分子式為BaSO3。它是白色粉狀物,可以用於造紙。像其他的鋇化合物一樣,它是有毒的。[2]它是通過碳熱反應把硫酸鋇還原成硫化鋇的中間體。[3]
- BaSO4 + CO → BaSO3 + CO2
Quick Facts 亞硫酸鋇, 識別 ...
Close
亞硫酸鋇可以由亞硫酸鈉和氯化鋇[4]或氫氧化鋇[5]而成。


亞硫酸鋇是一種白色無臭固體,不可燃,難溶於水,[6]易溶於酸。[7]它是單斜晶系的,[8]不過三斜晶系的亞硫酸鋇也是已知的。[9]
亞硫酸鋇可以被過氧化氫氧化成硫酸鋇。[10]

在沒有空氣的情況下退火時,亞硫酸鋇會分解成硫酸鋇和硫化鋇。[7]
亞硫酸鋇的LD50為375mg/kg。它對皮膚和眼睛有刺激性。雖然亞硫酸鋇不可燃,但它加熱分解會產生有害的硫氧化物氣體。它與酸反應,放出二氧化硫[11]。
CRC Handbook of Chemistry and Physics 97th Edition. 2016-06-24: 4–50. ISBN 1-4987-5428-7 (英語). Kresse, Robert; Baudis, Ulrich; Jäger, Paul; Riechers, H. Hermann; Wagner, Heinz; Winkler, Jochen; Wolf, Hans Uwe, Ullmann's Encyclopedia of Industrial Chemistry, Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, 2005, doi:10.1002/14356007.a03_325.pub2 D. Van Nonstrant Company. Elementary General Chemistry.
C. Saint-Pierre: "Sur la décomposition spontanée de divers bisulfites" in Compt. Rend. Hebd. 1872, 74, S. 52–53. Volltext R. Abegg, F. Auerbach: Handbuch der anorganischen Chemie, Verlag S. Hirzel, Bd. 2, 1908. S. 270; Volltext Jean D'Ans, Ellen Lax: Taschenbuch für Chemiker und Physiker. 3. Elemente, anorganische Verbindungen und Materialien, Minerale, Band 3. 4. Auflage, Springer, 1997, ISBN 978-3-540-60035-0, S. 330. . R. S. W. Braithwaite, A. R. Kampf, R. G. Pritchard, R. P. H. Lamb: "The occurrence of thiosulfates and other unstable sulfur species as natural weathering products of old smelting slags" in Mineralogy and Petrology 1993, 47(2-4), S. 255–261. doi:10.1007/BF01161570 A. Classen, O. Bauer: "Ueber die Anwendbarkeit des Wasserstoffsuperoxyds in der analytischen Chemie" in Berichte der deutschen chemischen Gesellschaft 1883, S. 1061–1074. Volltext