缬氨酸
来自维基百科,自由的百科全书
来自维基百科,自由的百科全书
缬氨酸(英语:Valine)是二十种蛋白胺基酸中的其中一种。其英文名称源自于缬草(Valerian),而中文名称也因此称为缬氨酸。
| 缬氨酸 | |
|---|---|

| |
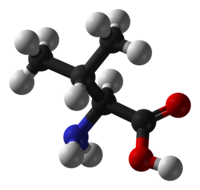
| |
| IUPAC名 2-氨基-3-甲基丁酸 | |
| 缩写 | Val, V |
| 识别 | |
| CAS号 | 72-18-4(L-异构物) 516-06-3 640-68-6(D-异构物) |
| PubChem | 1182 |
| ChemSpider | 6050 |
| SMILES |
|
| InChI |
|
| InChIKey | KZSNJWFQEVHDMF-BYPYZUCNBW |
| ChEBI | 57762 |
| DrugBank | DB00161 |
| KEGG | D00039 |
| IUPHAR配体 | 4794 |
| 性质 | |
| 化学式 | C5H11NO2 |
| 摩尔质量 | 117.15 g·mol−1 |
| 密度 | 1.316 g/cm3 |
| 熔点 | 298 °C(571 K) |
| 溶解性(水) | 易溶 |
| pKa | pKa1 = 2.29 (-COOH) pKa2 = 9.74 (-NH3+)[1] |
| 磁化率 | -74.3·10−6 cm3/mol |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
从营养学的观点来看,缬氨酸是一种必需胺基酸。它的密码子是GUU、GUA、GUC和GUG。它是一种非极性氨基酸,因此缬氨酸是疏水性的。
缬氨酸是完全地电中性,当其侧链也是中性,而且由其氨基和羧基所产生的电荷刚好平衡,这种分子称为两性离子。
在镰刀型红血球疾病里,血红蛋白内的缬氨酸替代了亲水性胺基酸-谷氨酸(Glutamate):因为缬氨酸是疏水性的,血红蛋白因此而无法正确折叠。
缬氨酸最早由赫尔曼·埃米尔·费歇尔于1901年从酪蛋白中分离出来[2]。
缬氨酸对于动物是一种必需氨基酸。故动物须通过摄食来补充生理活动所需缬氨酸(通常是以蛋白质的形式)[3]。成人每天需摄入约4毫克/千克体重的缬氨酸[4] 。植物可以丙酮酸为原料经若干步骤合成缬氨酸。该合成路径与亮氨酸的合成路径的头几步是相同的。合成路径的最后一步则为中间产物α-酮异己酸与谷氨酸的转氨作用。与上述合成路径相关的酶有:[5]
以下代谢性疾病会影响缬氨酸的降解:
消旋缬氨酸可通过异戊酸的溴化和α-溴代产物的氨基化合成
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.