Loading AI tools
来自维基百科,自由的百科全书
乙硼烷一种是无机化合物,化学式为B2H6,是目前能分离出的最简单的硼烷。乙硼烷在室温下为无色气体,可以与空气形成爆炸性混合物,并且在潮湿空气中自燃。有剧毒。
| 乙硼烷 | |
|---|---|
| |

| |
| IUPAC名 Diborane(6) | |
| 识别 | |
| CAS号 | 19287-45-7 |
| ChemSpider | 17215804 |
| SMILES |
|
| InChI |
|
| InChIKey | KLDBIFITUCWVCC-UHFFFAOYAF |
| EINECS | 242-940-6 |
| ChEBI | 33590 |
| RTECS | HQ9275000 |
| 性质 | |
| 化学式 | B2H6 |
| 摩尔质量 | 27.67 g·mol⁻¹ |
| 外观 | 无色气体 |
| 密度 | 1.18 g/L (15 °C,气态) |
| 熔点 | −165.5 °C [1] (108.15 K) |
| 沸点 | −92.5 °C (180.65 K) |
| 溶解性(水) | 反应 |
| 结构 | |
| 配位几何 | 四面体 (硼) |
| 分子构型 | 见内文 |
| 偶极矩 | 0 D |
| 危险性 | |
| NFPA 704 | |
| 闪点 | 可燃气体 |
| 自燃温度 | 38 °C |
| 相关物质 | |
| 相关硼化合物 | 癸硼烷(14) 三氟化硼 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
乙硼烷具有较高的化学活性,容易与各种无机分子和有机分子起反应。这不仅是因为乙硼烷生成热为正值(即所谓吸热化合物),还由于硼对氟、氧、氮、磷等电负性强的元素有很大的亲合力[2]。
乙硼烷为无色气体,其蒸汽压为(3.00×104±133)Pa(-111.6℃),相对密度为0.477(-122℃)及0.577(-183℃)。
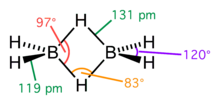
乙硼烷分子具有D2h点群。两个硼原子各用两个 sp2 混成轨域与两个氢原子的 1s 轨道重叠形成 B-H σ键的同时,每个硼原子又用第三个 sp2 混成轨域和余下的一个 p 轨道组合成两个轨道 Φ,分别位于平面上下。两个轨道分别与两个氢原子的 1s 轨道成两个垂直于平面的三中心两电子 BHB 键,正好用上余下的4个价电子[3]。因此乙硼烷分子不能自由旋转。
乙硼烷是缺电子化合物,可以与许多配体形成单桥加合物,如C5H5N·B2H6等。这类加合物的通式为:
乙硼烷分子中的端梢氢原子,可被一些有机基团取代形成各种各样的有机衍生物:
形成五、六取代物的同时往往伴随桥键的断裂而发生歧化反应。
卤代乙硼烷(氟除外)可通过B2H6与BX3的平衡反应制取,溴代物也可通过乙硼烷直接溴代获得。 乙硼烷在低温就可以和醇、醚、酮及酯类发生反应[1] :
乙硼烷可以和苯在100℃下反应。
乙硼烷和溴、碘反应分别产生B2H5Br和B2H5I. B2H5Cl极不稳定。 [1]
乙硼烷也可以和一氧化碳反应:
乙硼烷是亲电试剂,并且可将很多官能团还原,如将醛和酮还原为醇,腈还原成胺,肟还原成N-烷基羟胺,施夫碱还原为仲胺等。
乙硼烷极易水解,与水反应生成硼酸和氢:
而相对分子质量较大的戊硼烷和癸硼烷只有加热才能水解。 [1]
极纯的硼烷在干燥空气或氧气中并不自燃,但如果有微量杂质存在,就立刻发生自燃现象。[1]
此反应放热很大,故硼烷可在火箭和导弹中用作高能喷射燃料。
二硼烷可以和卤素反应。和氯气的反应很剧烈。[1]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.