氨三乙腈(NTAN)是一种有机化合物,化学式为C6H6N4,它是氨三乙酸、三(氨乙基)胺和氨乙基哌嗪的前驱体。
| 氨三乙腈 | |
|---|---|

| |
| IUPAC名 2,2′,2′′-Nitrilotriacetonitrile | |
| 别名 | 三(氰甲基)胺 2,2',2''-氮川三乙腈 |
| 识别 | |
| CAS号 | 7327-60-8 |
| PubChem | 81762 |
| ChemSpider | 73778 |
| SMILES |
|
| InChI |
|
| InChIKey | LJAIDEYQVIJERM-UHFFFAOYSA-N |
| 性质 | |
| 化学式 | C6H6N4 |
| 摩尔质量 | 134.14 g·mol−1 |
| 熔点 | 125 °C(398 K)[1] |
| 结构 | |
| 空间群 | Pnma |
| 晶格常数 | a = 7.1085, b = 9.9320, c = 9.3869 |
| 危险性 | |
GHS危险性符号  
| |
| GHS提示词 | 危险 |
| H-术语 | H301, H302, H312, H315, H319, H335, H373 |
| P-术语 | P260, P261, P264, P270, P271, P280, P301+310, P301+312, P302+352, P304+340, P305+351+338, P312, P314, P321 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
合成
氨三乙腈可由甲醛、氨和氰化氢在酸性水溶液中通过氨的氰甲基化反应得到。[2][3]
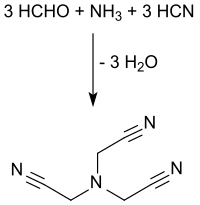
氨气进入反应体系,以六亚甲基四胺[4]或硫酸铵的形式和甲醛水溶液(通常为37wt%)在pH<2的调节下与氰化氢在100 °C反应得到。[5]在生产过程中,尤其是连续反应的情况下,低于90 °C时,氨三乙腈会沉淀出来,堵塞反应器管路,导致热失控。 [6]
应用
在碱性催化剂(如甲醇钠)存在下,氨三乙腈可与亚氨基二乙腈在熔体中均聚或共聚,形成深色的固体聚合物,它在1000°C以上可碳化形成含氮导电聚合物。[7]
氨三乙腈在氢化时,其中一个氰基会转化为亚氨基,相比于亚氨基的进一步氢化,它倾向于进攻另一个相邻的氰基以形成稳定的六元环。催化氢化的最终产物是氨乙基哌嗪。

在雷尼镍等催化剂存在下、氨过量时进行氢化,氨三乙腈会转化为三(氨乙基)胺[8]。

得到的这种化合物(简写tren)可用作四齿配体和过渡金属离子形成稳定的螯合物。[9]
氨三乙腈和甲醛在pH 9.5下反应,得到2,2-二羟甲基氨三乙腈,它在氢氧化钠溶液中于100 °C水解,得到2,2-二羟甲基氨三乙酸三钠,酸化后得到2,2-二羟甲基氨三乙酸。[10]

该化合物可作为重金属离子或碱土金属离子的络合剂,如作为漂白剂(过硼酸钠等)的稳定剂和作为洗涤助洗剂,用于抑制纺织品在洗涤过程中产生水垢。
氨三乙腈在硫酸中水解,可以定量产生氨三乙酰胺,它可用作金属配位的中性四齿配体。[11]升高温度,通过闭环反应可以得到3,5-二氧代哌嗪-1-乙酰胺,中和后在过量氨水中加热,也可以定量转化为氨三乙酰胺。[12][13]

氨三乙腈在酸性或碱性条件下水解,可以得到氨三乙酸及其钠盐。[14][2]反应中可能产生的CN−可以通过氧化后处理(如在pH 8下使用次氯酸钠氧化)去除。[15]

参考文献
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.
