
Потрійна точка
З Вікіпедії, безкоштовно encyclopedia
Потрі́йна то́чка — макроскопічний стан речовини, за якого його газоподібна, рідка та тверда форми знаходяться у рівновазі[1]. На фазовій діаграмі такому стану відповідає точка, в якій сходяться криві розділу фаз.
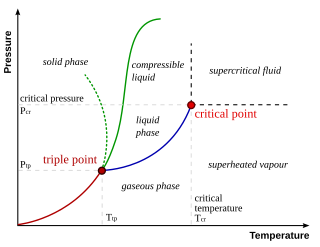
Існує єдине сполучення значень температури та тиску, за яких всі три фази речовини перебувають в стані термодинамічної рівноваги. Ця властивість робить потрійну точку зручним та легко відтворюваним еталоном температури. Зокрема, для води потрійна точка реалізується за температури 0,01 °C і тиску 611.657 Па.
Потрійна точка води використовується для визначення кельвіна — основної одиниці вимірювання термодинамічної температури в Міжнародній системі одиниць (SI). Значення потрійної точки води фіксується за визначенням, а не вимірюється. Потрійні точки кількох речовин використовуються для визначення точок міжнародної температурної шкали ITS-90, починаючи від потрійної точки водню (13.8033 К) і до потрійної точки води (273.16 К, 0.01 °С або 32.018 °F) .
За правилом фаз для однокомпонентної термодинамічної системи потрійна точка єдина.