
Оксиран
хімічна сполука / З Вікіпедії, безкоштовно encyclopedia
Шановний Wikiwand AI, Давайте зробимо це простіше, відповівши на ключові запитання:
Чи можете ви надати найпопулярніші факти та статистику про Оксиран?
Підсумуйте цю статтю для 10-річної дитини
Оксира́н (етиле́нокси́́д) — насичена гетероциклічна сполука з хімічною формулою C2H4O. Це найпростіший циклічний етер. За звичайних умов перебуває у газоподібному стані. Температура кипіння становить 10,7 °C. Добре розчинний у спиртах, ефірі, хлороформі, чотирихлористому вуглеці, ацетоні та інших розчинниках.
| Оксиран[1] | |
|---|---|
 Оксиран |
 |
 |
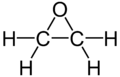 |
| Назва за IUPAC | Оксиран |
| Інші назви | Оксид етилену, етиленоксид |
| Ідентифікатори | |
| Номер CAS | 75-21-8 |
| PubChem | 6354 |
| Номер EINECS | 200-849-9 |
| Номер EC | 200-849-9 |
| KEGG | D03474 |
| Назва MeSH | Ethylene+Oxide |
| ChEBI | CHEBI:27561 |
| RTECS | KX2450000 |
| SMILES | C1CO1 |
| InChI | 1/C2H4O/c1-2-3-1/h1-2H2 |
| Номер Бельштейна | 102378 |
| Номер Гмеліна | 676 |
| Властивості | |
| Молекулярна формула | C2H4O |
| Молярна маса | 44,05 г/моль |
| Молекулярна маса | 44 а. о. м. |
| Зовнішній вигляд | безбарвний газ |
| Густина | 0,882 кг/м³ |
| Тпл | −111,4 °C[2] |
| Ткип | 10,7 °C |
| Тиск насиченої пари | 145,8 кПа (при 20 °C) |
| Діелектрична проникність (ε) | 13,9[3] |
| Показник заломлення (nD) | 1,360 (при 8,4 °C)[4] |
| Дипольний момент | 1,88—1,91[5] |
| Термохімія | |
| Ст. ентальпія утворення ΔfH 298 |
-52,6 кДж/моль |
| Ст. ентальпія згоряння ΔcH 298 |
308,4—332,5 ккал/моль[6] |
| Ст. ентропія S 298 |
243 Дж/(моль·К) |
| Теплоємність, c p |
48,19 Дж/(моль·К) |
| Небезпеки | |
| ГДК (Україна) | 1 мг/м³ |
| ЛД50 | 72 мг/кг |
| Головні небезпеки | канцероген |
| NFPA 704 | |
| Температура спалаху | -18 °C |
| Вибухові границі | 3—100 % |
| Пов'язані речовини | |
| Пов'язані речовини | азірідин, тіїран, боріран |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Найпоширенішим промисловим методом добування є каталітичне окиснення етилену, коли виробництво оксирану здійснюють у нерухомому шарі каталізатора з рециркуляцією продуктів реакції.
Оксиран різко відрізняється своїми властивостями від етерів: на відміну від них, він має велику схильність до реакцій приєднання і полімеризації, тобто поводиться як ненасичена сполука.
Токсична речовина. Звичайні симптоми системного отруєння оксираном — головний біль, задишка, нудота і блювання. Поріг сприйняття людиною запаху оксирану — 1,26 мг/л. Гранично допустима концентрація оксирану в повітрі прийнята рівною 1 мг/л[7].
Застосовується в органічному синтезі, зокрема для добування етиленгліколю, який застосовується у виробництві антифризу, як розчинник, пластифікатор, у виробництві мономерів для синтетичних волокон. Оксиран є важливою сировиною для виробництва неіоногенних поверхнево-активних речовин.
