
Софосбувір
хімічна сполука / З Вікіпедії, безкоштовно encyclopedia
Шановний Wikiwand AI, Давайте зробимо це простіше, відповівши на ключові запитання:
Чи можете ви надати найпопулярніші факти та статистику про Софосбувір?
Підсумуйте цю статтю для 10-річної дитини
Софосбувір (лат. Sofosbuvirum) — синтетичний противірусний препарат з групи нуклеозидних аналогів для перорального застосування.[2] Софосбувір був розроблений американською компанією «Pharmasset», під назвою «Совалді». А з 2012 року, після викуплення акцій «Pharmasset» компанією «Gilead Sciences»[3], подальша розробка і маркетинг препарату проводяться «Gilead Sciences».[4] У 2013 році Управління з продовольства і медикаментів США (FDA) схвалило використання софобусвіра, в комбінації з рибавірином, для лікування гепатиту C, спричиненого вірусом гепатиту С 2 і 3 генотипів; а також для потрійної терапії разом із пегільованим інтерфероном і рибавірином, для лікування гепатиту С, спричиненого вірусом гепатиту С 1 і 4 генотипів[5], — на основі 4 клінічних досліджень ІІІ фази, які проводились на території США.[6] У 2014 році FDA також схвалило застосування софобусвіра у комбінації з іншим противірусним препаратом — ледіпасвіром[7] — на основі клінічних досліджень, проведених на території США, та опублікованих на сайті британського журналу «The Lancet» у листопаді 2013 року.[8] Згідно із попередніми результатами досліджень, ця комбінація має високу ефективність у лікуванні хворих, які інфіковані вірусом гепатиту С 1-го генотипу, який є найбільш поширеним у США, Європі та Японії.[9] У 2014 році «Gilead Sciences» уклала угоду про надання ліцензії сімом індійським фармацевтичним компаніям на виробництво генеричних препаратів софобусвіра та ледіпасвіра на території Індії, та їх продаж на території 91 країни світу. Ця угода була розкритикована міжнародними організаціями, які займаються питаннями лікування і захисту хворих на гепатит С та СНІД, як така, що не дає можливості пацієнтам з гепатитом С у тих країнах, які не увійшли до списку країн із дозволом на продаж генеричного софобусвіру, лікуватись дешевшим аналогом препарату.[10] Україна також не входила в перелік країн, в яких дозволено продаж генеричного софосбувіру. Але вже у 2015 році генеричний препарат софосбувіру був зареєстрований в Україні та включений до переліку лікарських препаратів, що закуповуються за бюджетні кошти.[11][12]
 | |
|---|---|
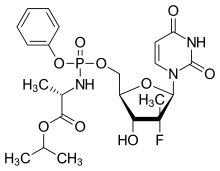
Софосбувір | |
| Систематизована назва за IUPAC | |
| Isopropyl (2S)-2-[[[(2R,3R,4R,5R)-5-(2,4-dioxopyrimidin-1-yl)-4-fluoro-3-hydroxy-4-methyl-tetrahydrofuran-2-yl]methoxy-phenoxy-phosphoryl]amino]propanoate | |
| Класифікація | |
| ATC-код | J05AX15 |
| PubChem | 45375808 |
| CAS | 1190307-88-0 |
| DrugBank | DB08934 |
| KEGG | D10366 |
| Хімічна структура | |
| Формула | C22H29FN3O9P |
| Мол. маса | 529,453 г/моль |
| Фармакокінетика | |
| Біодоступність | 92% |
| Метаболізм | Печінка |
| Період напіввиведення | 24 хв. (софосбувір), 27 год.(метаболіт) |
| Екскреція | Нирки, фекалії |
| Реєстрація лікарського засобу в Україні | |
| Назва, фірма-виробник, країна, номер реєстрації, дата | СОВАЛДІ, «Гілеад Сайєнсиз, Інк.», США UA/14706/01/01 09.10.2015-09.10.2020 ГРАТЕЦІАНО, «ЮРОПІЕН ІДЖІПШЕН ФАРМАС’ЮТІКАЛ ІНДАСТРІЗ»,Єгипет UA/14761/01/01 18.11.2015-18/11/2020 [1] |
Всесвітня організація охорони здоров'я включила софосбувір до списку необхідних лікарських засобів.[13]