
Ацетилхлорид
хімічна сполука / З Вікіпедії, безкоштовно encyclopedia
Шановний Wikiwand AI, Давайте зробимо це простіше, відповівши на ключові запитання:
Чи можете ви надати найпопулярніші факти та статистику про Ацетилхлорид?
Підсумуйте цю статтю для 10-річної дитини
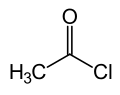
Ацети́лхлори́д — органічна сполука складу CH3COCl, хлороангідрид оцтової кислоти (етанової).
| Ацетилхлорид | |
|---|---|
 |
 |
| Назва за IUPAC | ацетилхлорид[1] |
| Систематична назва | етаноїлхлорид |
| Ідентифікатори | |
| Номер CAS | 75-36-5 |
| Номер EINECS | 200-865-6 |
| DrugBank | DB14623 |
| ChEBI | 37580 |
| RTECS | AO6390000 |
| SMILES | CC(=O)Cl[2] |
| InChI | InChI=1S/C2H3ClO/c1-2(3)4/h1H3 |
| Номер Бельштейна | 605303 |
| Номер Гмеліна | 1611 |
| Властивості | |
| Молярна маса | 78,497 г/моль |
| Зовнішній вигляд | безбарвна рідина |
| Густина | 1,0982 г/см³ |
| Тпл | -112,0 °C |
| Ткип | 51,8 °C |
| Діелектрична проникність (ε) | 16,9 (2 °C) 15,8 (22 °C) |
| Показник заломлення (nD) | 1,3897 (20 °C) |
| В'язкість | 0,368 мПа·с (25 °C) 0,294 мПа·с (50 °C) |
| Структура | |
| Дипольний момент | 2,72±0,14 Д |
| Термохімія | |
| Ст. ентальпія утворення ΔfH 298 |
-272,9 кДж/моль (рід.) -242,8 кДж/моль (газ) |
| Ст. ентропія S 298 |
200,8 Дж/(моль·K) (рід.) 295,1 Дж/(моль·K) (газ) |
| Теплоємність, c p |
117,0 Дж/(моль·K) (рід.) 67,8 Дж/(моль·K) (газ) |
| Небезпеки | |
| Температура спалаху | 4 °C |
| Температура самозаймання | 390 °C |
| Пов'язані речовини | |
| Інші (ацильні сполуки) | ацетилбромід, ацетилфлуорид |
| Пов'язані речовини | оцтова кислота |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
За звичайних умов є безбарвною рідиною, що димить на повітрі. Його присутність у повітрі при концентрації понад 0,5 мільйонних часток спричинює сльозотечу, поразнення дихальних шляхів. Вдихання випарів може спричинювати значні отруєння. Оскільки ацетилхлорид є надзвичайно реакційноздатним, він ацилює гідроксильні та аміногрупи ферментів, порушуючи їхнє нормальне функціонування. Також він є легкозаймистою речовиною (спалахує при 4 °C), що вимагає особливої обережності у його використанні та зберіганні.
Важливість ацетилхлориду вперше була описана у 1850 році. Він є ефективним агентом для ацетилювання спиртів та амінів для отримання естерів, амідів. Зокрема, його застосовують у реакції Фріделя—Крафтса при отриманні ацетофенону ацилюванням бензену. Ацетилхлорид є важливим реагентом у синтезі барвників, фармацевтичних препаратів (аспірину, парацетамолу, ацетаніліду), ацильованих полімерів.