Loading AI tools
Vikipedi'den, özgür ansiklopediden
İnsan solunum sinsityal virüsü (hRSV) ve insan ortopnömovirüsü de denilen Solunum sinsityal virüsü (RSV), solunum yolu enfeksiyonlarına neden olan yaygın, bulaşıcı bir virüs’tür. RSV, negatif anlamlı, tek sarmallı bir RNA virüsüdür.[1] Virüsün adı, enfekte olmuş hücreler birleştiğinde oluşan sinsitya denilen büyük hücrelerden gelir.[1][2]
| Solunum sinsityal virüsü (RSV) | |
|---|---|
 İpliksi RSV parçacıklarının elektron mikrografı | |
| Genel özellikler | |
| Sınıflandırma | |
| Baltimore sınıflandırması | |
| Grup Ortopnömovirüs | Ortopnömovirüs |
| UVTK sınıflandırması | |
| Takım | Henüz atanmamış |
| Familya | Ortopnömovirüs |
| Alt familya | Ortopnömovirüs hominis |
eş anlamlılar
| |
RSV, bebeklerde solunum yolu nedeniyle hastaneye kaldırılmanın yaygın bir nedenidir ve yeniden enfeksiyon, genellikle daha az şiddette olsa da, yaşamın ilerleyen dönemlerinde görülür. Tüm yaş gruplarında RSV dikkate değer bir patojen'dir. Enfeksiyon oranları genellikle soğuk kış aylarında daha yüksektir; bebeklerde bronşiyolit’e, yetişkinlerde soğuk algınlığı’na ve yaşlılarda ve bağışıklık sistemi zayıf kişilerde zatürre gibi daha ciddi solunum hastalıklarına neden olur.[3]
RSV hem toplumda hem de hastane ortamlarında salgınlara neden olabilir. Gözler veya burun yoluyla ilk enfeksiyonun ardından virüs, üst ve alt solunum yolunun epitel hücrelerini enfekte ederek iltihaplanmaya, hücre hasarına ve solunum yol tıkanıklığına neden olur.[1] RSV'nin viral tespiti ve tanısı için antijen testi, moleküler testler ve viral kültür dahil olmak üzere çeşitli yöntemler mevcuttur.[2]
Başlıca hastalık önleyici tedbirler elleri yıkamak ve hastalık bulaşmış kişilerle yakın temastan kaçınmaktır.[4] Mayıs 2023'te ABD Gıda ve İlaç Dairesi (FDA), ilk RSV aşıları olan Arexvy (GSK plc tarafından geliştirildi) ve Abrysvo'yu (Pfizer) onayladı.[5][6] Palivizumab veya nirsevimabın (her ikisi de monoklonal antikor tedavileridir) koruyucu sağlık kullanımı, yüksek riskli bebeklerde RSV enfeksiyonunu önleyebilir.[4][7]
Şiddetli hastalığın tedavisi, oksijen tedavisi ve gerektiğinde sürekli pozitif hava yolu basıncı (CPAP) veya nazal yüksek akışlı oksijen ile daha gelişmiş solunum desteği dahil olmak üzere öncelikle destekleyicidir. Şiddetli solunum yetmezliği vakalarında, entübasyon ve mekanik havalandırma gerekebilir. Ribavirin çocuklarda RSV tedavisi için lisanslı antiviral bir ilaçtır.[8] RSV enfeksiyonu genellikle ciddi değildir ancak bebeklerde ve yetişkinlerde, özellikle yaşlılarda ve kalp veya akciğer hastalığı olanlarda ölüme neden olabilir.
RSV, 1956'da araştırmacıların solunum yolu hastalığı olan şempanze nüfusundan bir virüsü izole etmesiyle keşfedildi. Virüse şempanze coryza ajanı (CCA) adını verdiler.[9] 1957'de aynı virüs Robert M. Chanock tarafından solunum yolu hastalığı olan çocuklarda tespit edildi.[10] Bebeklerde ve çocuklarda insan antikorları üzerinde yapılan çalışmalar, enfeksiyonun yaşamın erken dönemlerinde yaygın olduğunu ortaya çıkardı.[11] Virüs daha sonra insan ortopnömovirüsü veya insan solunum sinsityal virüsü (hRSV) olarak yeniden adlandırıldı.[12][13]
Diğer tüm pnömovirüsler hRSV'ye büyük benzerlik gösterir. Sığır RSV'si (bRSV), genomunun yaklaşık %80'ini hRSV ile paylaşır. Aynı zamanda hRSV'nin gençleri tercih etmesini de paylaşır ve altı aylıktan küçük buzağılarda daha ciddi hastalıklara neden olur. bRSV bulaşmış buzağılar, hRSV bulaşmış çocuklarla hemen hemen aynı semptomlara sahip olduğundan RSV araştırmalarında önemli bir hayvan modeli oldukları kanıtlanmıştır.[14]
RSV enfeksiyonu, hafif üst solunum yolu enfeksiyonlarından (ÜSYE), hastaneye kaldırılmayı ve mekanik havalandırma’yı gerektiren ciddi ve olası yaşamı tehdit eden alt solunum yolu enfeksiyonlara (ASYE) kadar çok çeşitli belirti ve semptomlarla ortaya çıkabilir.[14] RSV her yaştan insanda solunum yolu enfeksiyonlarına neden olabilse ve yaygın çocukluk çağı enfeksiyonları arasında yer alsa da sunumu genellikle yaş grupları ve bağışıklık durumu arasında farklıdır.[3] Yeniden enfeksiyon yaşam boyunca yaygındır ancak bebekler ve yaşlılar semptomatik enfeksiyon riski altındadır.[14]
Çocuklar iki yaşına kadar en az bir kere RSV enfeksiyonu geçirir.[15] Çocukluk çağı RSV enfeksiyonları, burun tıkanıklığı, burun akıntısı, öksürük ve hafifi ateş gibi tipik üst solunum yolu belirti ve semptomlarıyla sınırlıdır.[3][15] Muayenede burun mukozasında (rinit) ve boğazda (farenjit) iltihaplanma ve ayrıca gözlerde kızarıklık (konjonktival enfeksiyon) görülebilir.[2]
Çocukların yaklaşık %15-50'sinde bronşiyolit, viral pnömoni veya krup gibi daha ciddi alt solunum yolu enfeksiyonları gelişir.[14][16] Bebekler hastalığın ilerlemesi açısından en yüksek risk altındadır.[2]
Bronşiyolit akciğerlerdeki dar hava yollarının iltihaplanması ve tıkanmasıyla karakterize, yaygın bir alt solunum yolu enfeksiyonudur.[17] Çeşitli virüsler bronşiyolite neden olabilirken, vakaların yaklaşık %70'inden RSV sorumludur.[3] Genellikle 2 ila 4 gün süren burun akıntısı ve tıkanıklığı, ardından kötüleşen öksürük, gürültülü nefes alma, takipne (hızlı nefes alma) ve hırıltılı solunum ile kendini gösterir.[15]
Bebekler nefes almak için daha fazla çabaladıkça, subkostal çekilmeler (göbek göğüs kafesinin altına çekildiğinde), interkostal çekilmeler (kaburgalar arasındaki kaslar içe doğru çekildiğinde), homurdanma ve burun genişlemesi gibi solunum sıkıntısı belirtileri de gösterebilirler.[14] Çocuk yeterince beslenememişse dehidrasyon belirtileri de mevcut olabilir.[15] Ateş olabilir ancak yüksek ateş nadirdir.[14]
Oskültasyon sırasında sıklıkla çıtırtı ve hırıltı duyulabilir ve oksijen doygunluk seviyeleri azalabilir.[17]
Altı haftanın altındaki çok küçük bebeklerde ve özellikle prematüre bebeklerde enfeksiyon belirtileri daha az belirgin olabilir. Minimal solunum tutulumu olabilir. Bunun yerine, aktivitede azalma, sinirlilik, yetersiz beslenme veya zorlukla nefes alma gibi belirtiler gösterebilirler. Buna aynı zamanda apne nöbetleri veya nefes almada kısa duraklamalar da eşlik edebilir.[3][18]
RSV ile yeniden enfeksiyon yaşam boyunca yaygın olarak kalır. Yetişkinlikte yeniden enfeksiyon sıklıkla yalnızca soğuk algınlığı veya sinüs enfeksiyonu'ndan ayırt edilemeyen hafif ila orta şiddette semptomlara neden olur.[3] Enfeksiyon ayrıca asemptomatik de olabilir. Mevcutsa, burun akıntısı, boğaz ağrısı, ateş ve halsizlik gibi semptomlar genellikle üst solunum yollarına özgüdür: Vakaların büyük çoğunluğunda burun tıkanıklığı öksürük gelişiminden önce gelir.[2] Diğer üst solunum yolu enfeksiyonlarının aksine, RSV'nin yetişkinlerde yeni başlayan hırıltıya neden olma olasılığı daha fazladır.[2]
Enfekte yetişkinlerin yaklaşık %25'inde bronşit veya trakeobronşit gibi önemli alt solunum yolu enfeksiyonları olur.[14]
RSV, sağlıklı yetişkinlerde çok nadiren ciddi hastalığa neden olurken, yaşlılarda ve bağışıklık yetersizliği veya kardiyopulmoner hastalığı olanlarda hastalık ve ölüme neden olabilir. Yaşlı yetişkinler genç yetişkinlere benzer durumdadır ancak alt solunum yolu tutulumu riskinin artmasıyla birlikte semptom şiddeti daha fazla olma eğilimindedir. Özellikle yaşlıların zatürre, solunum güçlüğü ve yaşama olasılıkları daha fazladır.[2]
Hem yetişkinlerde hem de çocuklarda, bağışıklık sistemi baskılanmış olanlar, RSV ile ciddi enfeksiyona yakalanma riski altındadır. Bu gruptaki enfekte bireylerin üst solunum yolu tutulumundan alt solunum yolu tutulumuna doğru ilerleme olasılığı daha yüksektir ve virüs yayılımı uzun sürelidir.[19] Semptomun şiddeti, immün baskılanmanın boyutuyla yakından ilişkili gibi görünmektedir.
Hematopoietik kök hücre nakli]] (HSCT), yoğun kemoterapi ve akciğer nakli geçirmiş olanlar özellikle RSV’ye duyarlıdır.[2][20]
Kemik iliği nakli yapılan hastalar, özellikle ilik nakli öncesinde yüksek risk altındadır. Bu grupta RSV enfeksiyonu, hem zatürre hem de ölüm açısından yaklaşık %80 risk taşır.[2][21]
| Nüfus | RSV enfeksiyonunun rahatsızlıkları | |
|---|---|---|
| Çocuklar | Kısa süreli hastanede yatan çocuklarda aşağıdaki rahatsızlıkların gelişme riski vardır:[3]
Uzun vadede çocuklar, yetişkinliğe kadar sürebilecek aşağıdaki kronik durumları yaşama riski altındadır: | |
| Yetişkinler | Aşağıdakiler yaşlı yetişkinlerde veya altta yatan bağışıklık sistemi baskılanmış veya kardiyopulmoner rahatsızlıkları olanlarda daha çok görülür: | |
| Bağışıklık sistemi zayıflar | Bağışıklık sistemi baskılanmış bazı gruplar aşağıda yazılanlar gibi özel rahatsızlıklar açısından daha yüksek risk altındadır: |
RSV ile şiddetli alt solunum yolu enfeksiyonunun gelişmesi için risk faktörleri nüfusa göre değişir.
| Nüfus | RSV ile alt solunum yolu enfeksiyonuna ilerleme için risk faktörleri |
|---|---|
| Çocuklar[25] |
|
| Yetişkinler ve yaşlılar[3] |
|
| Bağışıklık sistemi zayıf olanlar[19][26] |
|

RSV negatif anlamlı, tek sarmallı bir RNA virüsüdür.[1] Bu viral türün bilimsel adı insan ortopnömovirüsüdür. Bu, genellikle sadece RSV olarak kısaltılan insan solunum sinsityal virüsü (hRSV) ile eşanlamlıdır.[27] Mononegavirales takımının Pneumoviridae familyası Orthopneumovirus cinsine aittir.[1] Adı, virüsün yüzeyindeki F proteinlerinin komşu hücre zarlarının birleşmesine neden olarak büyük çok çekirdekli sinsitya oluşturmasından kaynaklanır.[2]
RSV, F ve G yüzey proteinlerinin monoklonal antikorlara karşı reaktivitesine bağlı olarak A ve B olmak üzere iki antijenik alt tipe ayrılır.[1][2] Alt tipler yerel salgınlarda eş zamanlı dolaşıma girme eğiliminde olsa da A alt tipi daha yaygındır.[21] Genellikle RSV A alt tipinin (RSVA), daha yüksek viral yükleri ve daha hızlı iletim süresiyle RSV B alt tipinden (RSVB) daha öldürücü olduğu düşünülür.[1][2]
Bugüne kadar 16 RSVA ve 22 RSVB klad tanımlanmıştır.[1] RSVA arasında GA1, GA2, GA5 ve GA7 dalları baskındır.
GA7 yalnızca Amerika Birleşik Devletleri'ndedir.[1] RSVB'ler arasında BA sınıfı tüm dünyada yaygındır.[1]

RSV’nin negatif anlamlı, tek sarmallı bir RNA genom’u vardır.[1] Genom doğrusaldır ve yaklaşık 15.000 nükleotit uzunluğundadır.[2] Parçalı değildir; bu ise grip'den farklı olarak RSV'nin, büyük pandemi'lerden sorumlu olan genetik yeniden sınıflandırma ve antijenik sapma türlerine katılamayacağı anlamına gelir.[3]
11 proteini kodlayan 10 gen'i vardır.[1][3] Gen sırası NS1-NS2-N-P-M-SH-G-F-M2-L'dir ve NS1 ve NS2 geni yapısal olmayan promoter genler olarak görev yapar.[28]
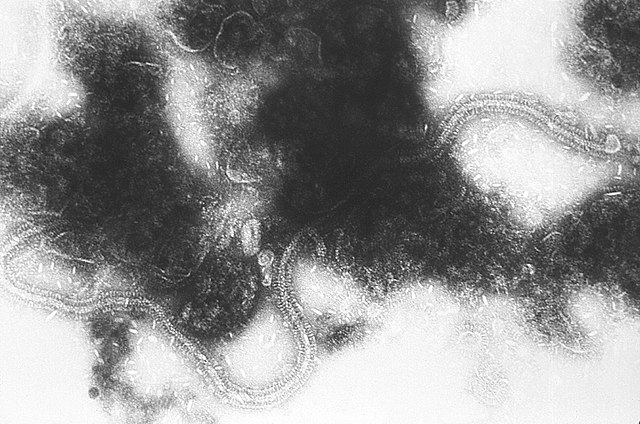

RSV orta büyüklükte (~150 nm) zarflı bir virüs'tür. Pek çok parçacık küresel olmakla birlikte filamentli türler de tanımlanmıştır.[1][2]
Genom sarmal bir nükleokapsid içindedir ve matris proteini ve viral glikoproteinleri içeren bir zarfla çevrilidir.[29] Aşağıdaki tabloda 11 protein daha ayrıntılı olarak açıklanmıştır.
| Virion'daki konum | Protein | Alternatif isim | İşlev | Ek Bilgiler |
|---|---|---|---|---|
| Lipid zarf (zar ötesi yüzey proteinleri) | G | Glikoprotein | Konak hava yolunun siliyer hücrelerine viral bağlanma | F ve G glikoproteinleri viral bağlanmayı ve enfeksiyonun başlangıç aşamalarını kontrol eden iki ana yüzey proteinidir. F ve G proteinleri aynı zamanda doğal enfeksiyon sırasında nötrleştirici antikorlar için birincil hedeflerdir. |
| F | Füzyon proteini | Viral ve konakçı hücre zarlarının füzyonu; sinsityum oluşumu | ||
| SH | Küçük hidrofobik protein | Viroporin; iyon kanalı | Hücre füzyonuna katılır, ancak bilinen nötrleştirici epitop yoktur | |
| Zarfın iç yüzü | M | Matris proteini | Montaj | |
| Ribonükleokapsid | N | Nüseloprotein | RNA bağlama | Genomda transkripsiyon, RNA replikasyonunda ve parçacık tomurcuklanmasında rol oynar |
| P | Fosfoprotein | Fosforilasyon | ||
| L | "Büyük" protein | RNA'ya bağımlı RNA polimeraz | ||
| M2-1 | - | Transkripsiyon işlenebilirlik faktörü | ||
| Düzenleyici | M2-2 | - | transkripsiyon / RNA kopyalanmasının düzenlenmesi | |
| Yapısal olmayan | NS-1 | - | doğuştan gelen bağışıklık sistemi’nin kaçırılmasına dahil oldu | apoptoz'u engelleyerek ve Tip I IFN sinyalini engelleyerek etki eder |
| NS-2 | - |


Yüzey proteini G (glikoprotein), virüsün konakçı hücrelere bağlanmasından birincil olarak sorumludur.[30] Bu protein suşlar arasında oldukça değişkendir.[21] G proteini hem membrana bağlı hem de salgılanmış formda bulunur.[2][30] Membranda bulunan form, konakçı hücrelerin yüzeyinde heparan sülfat gibi glikozaminoglikanlara (GAG'ler) bağlanarak bağlanmadan sorumludur.[1][2][3] Salgılanan form, antikor aracılı nötralizasyonu engellemek için antijen sunan hücrelerle etkileşime girerek tuzak görevi yapar.[2][30] G proteini ayrıca siliyer bronşiyal konakçı hücrelerin yüzeyindeki CX3C kemokin reseptörü 1'e (CX3CR1) bağlanan bir CX3C fraktalkin benzeri motif içerir.[1][3] Bu bağlanma hücresel kemotaksiyi değiştirebilir ve bağışıklık hücrelerinin enfekte bireylerin akciğerlerine göçünü azaltabilir.[30] G proteini aynı zamanda TLR4 dahil olmak üzere çeşitli toll benzeri reseptörlerden gelen sinyalleri engelleyerek konakçının bağışıklık tepkisini de değiştirir.[3][30]
Yüzey proteini F (füzyon proteini), viral ve konakçı hücre zarlarının füzyonunun yanı sıra viral partiküller arasında sinsityum oluşumundan sorumludur.[21] Viral bağlanma hem F hem de G proteinlerini içeriyor gibi görünse de, F füzyonu G'den bağımsız olarak gerçekleşir.[30] F proteini çoklu konformasyonel formlarda bulunur.[1][3] Prefüzyon durumunda (PreF), protein trimerik formda bulunur ve majör antijenic bölgesi Ø'yi içerir.[1] Ø vücuttaki antikorları nötralize etmenin birincil hedefi olarak hizmet eder.[3] Konakçı hücre yüzeyindeki hedefine bağlandıktan sonra (tam ligandı belirsizliğini korumaktadır), PreF, Ø'nin kaybolduğu bir konformasyonel değişime uğrar.[1][3] Bu değişiklik, proteinin kendisini konakçıya hücre zarı yerleştirmesini sağlar ve viral ve konakçı hücre zarlarının füzyonuna yol açar.[1] Son konformasyonel değişim, proteinin daha kararlı ve uzun bir formuyla sonuçlanır (postfüzyon, PostF).[3] RSV G proteininin karşısında, RSV F proteini aynı zamanda toll benzeri reseptör 4'e (TLR4) bağlanıp onu aktive ederek doğuştan gelen bağışıklık tepkisini ve sinyal iletimini başlatır.[1][30]

Viral ve konakçı hücre zarlarının füzyonunun ardından, viral nükleokapsid (viral genomu içerir) ve ilişkili viral polimeraz, konakçı hücreye sitoplazma’ya iletilir. Transkripsiyon ve translasyon her ikisi de sitoplazmada meydana gelir. RNA'ya bağımlı RNA polimeraz, genomu, konakçı hücre makinesi tarafından yapısal proteinlere çevrilen haberci RNA'nın (mRNA) 10 segmentine kopyalar. Negatif anlamlı viral genomun kopyalanması sırasında, RNA'ya bağımlı RNA polimeraz, antijenom adı verilen pozitif yönlü bir tamamlayıcıyı sentezler. Bu tamamlayıcı iplik, nükleokapsidler halinde paketlenen ve birleşme ve parçacık tomurcuklanması için plazma zarına taşınan genomik negatif anlamlı RNA'yı oluşturmak için şablon olarak kullanılır.[29]
RSV son derece bulaşıcıdır ve hem toplumdan hem de hastaneden bulaşarak salgınlara neden olabilir.[2] RSV ile enfekte olan her kişi, ortalama 5 ila 25 enfekte olmayan kişiye virüsü bulaştıracağı tahmin edilir.[31] RSV, enfekte bir kişi öksürdüğünde veya hapşırdığında ve kirli damlacıklarla havaya yayılabilir. Bulaşma genellikle bu damlacıkların başka bir kişinin göz, burun veya ağzıyla temasında olur.[32] RSV ayrıca bulaşmış ciltte (örn. ellerde) 25 dakikaya kadar, tezgah üstü ve kapı kolları gibi diğer yüzeylerde ise birkaç saate kadar yaşayabilir.[2][31]
Virüsün 2 ila 8 günlük bir kuluçka dönemi vardır.[2]
İnsanlara hastalık bulaştıktan sonra genellikle 3 ila 8 gün boyunca hastalık bulaşıcıdır. Ancak bebeklerde ve bağışıklık sistemi zayıf olan kişilerde virüs 4 haftaya kadar yayılmaya devam edebilir (artık semptom göstermedikten sonra bile).[32]

Burun veya göz yoluyla bulaşmanın ardından RSV, üst ve alt hava yollarının siliyer sütunlu epitel hücrelerini enfekte eder.[2] RSV, yaklaşık 8 gün boyunca bu bronş hücreleri içinde çoğaltılmaya devam eder.[1] İlk birkaç günden sonra, RSV ile enfekte olmuş hücreler daha yuvarlak hale gelecek ve sonuçta alt solunum yolunun daha küçük bronşiyollerine doğru dökülecektir.[1] Bu dökülme mekanizmasının aynı zamanda virüsün üst solunum yollarından alt solunum yollarına yayılmasından da sorumlu olduğu düşünülmektedir.[1] Enfeksiyon, akciğerlerde inflamatuar hücrelerin (monositler ve T hücreleri gibi) göçü ve infiltrasyonu, epitelyal hücre duvarının nekrozu, ödem ve artan mukoza üretimi dahil olmak üzere genel iltihaplanmaya neden olur.[2] İltihaplanma ve hücre hasarı yaygın olmak yerine düzensiz olma eğilimindedir.[2] Dökülen epitel hücreleri, mukus tıkaçları ve birikmiş bağışıklık hücreleri birlikte alt solunum yolunun tıkanmasına neden olur.[1][2]
RSV enfeksiyonunun tanısı için çeşitli laboratuvar testleri vardır. Amerikan Pediatri Akademisi (AAP), RSV bronşiyolitinin (tedavinin büyük ölçüde destekleyici olduğu) teşhisi için laboratuvar testinin kullanılmasını rutin olarak tavsiye etmese de,[4] yüksek riskli gruplarda, sonucun olumlu olması durumunda RSV enfeksiyonunun doğrulanması garanti edilebilir. Test, klinik kararlara rehberlik eder.
Yaygın tanımlama teknikleri, antijen testi, moleküler test ve viral kültürdür.[2]
Antijen testi, genellikle bir nazofarengeal çubukla veya aspirattan RSV antijen fragmanlarının (veya moleküler viral yapı parçalarının) tespitini içerir. Bu, floresan etiketli antijenlerin mikroskop altında görüntülenmesiyle (doğrudan floresans tahlili veya DFA) veya piyasada satılan hızlı antijen saptama testinin (RADT) kullanılmasıyla gerçekleştirilebilir.[2]
Genellikle, antijen testi küçük çocuklarda oldukça hassastır (%80-90), ancak viral yayılımın daha az olduğu daha büyük çocuklarda ve yetişkinlerde önemli ölçüde daha az güvenilirdir.[2]
Antijen testleri, yaz ayları gibi RSV'nin yoğun olduğu sezonların dışında da daha yüksek hatalı pozitiflik oranlarına maruz kalır. Bu senaryolarda viral kültürün veya nükleik asit amplifikasyon testinin (NAAT) kullanılması doğru RSV tanısına yardımcı olabilir.
Nükleik asit amplifikasyon testleri (NAAT'ler) gibi moleküler analizler, nazofaringeal sürüntülerde ve aspiratlarda çok küçük miktarlarda virüsün hassas bir şekilde tespit edilmesini sağlar. Polimeraz zincir reaksiyonu (PCR) gibi NAAT analizleri, viral antijenlerden ziyade virüse özgü genetik malzemeyi belirler.
Moleküler testler %100'e yaklaşan duyarlılık ve özgüllüğe sahiptirler.[34] Ancak, diğer test yöntemlerine göre daha pahalıdır ve daha karmaşık ekipman gerektirirler. Bu yüzden moleküler testler kaynakların sınırlı olduğu alanlarda daha az yapılır.
RSV için moleküler test solunum semptomları olan tüm hastalar için rutin olarak önerilmez. Ancak bebekler, yaşlı yetişkinler ve kronik tıbbi rahatsızlıkları olan hastalar gibi RSV komplikasyonları açısından yüksek risk taşıyan hastalara önerilebilir.
Moleküler testler ayrıca RSV salgınlarının teşhisine de yardımcı olabilir. RSV için moleküler testler çok doğrudur. RT-PCR'nin duyarlılığı %90-95, özgüllüğü ise %98-99'dur. LAMP'ın duyarlılığı %95-100, özgüllüğü ise %99-100'dür.
Geleneksel viral kültürde, virüsün bir örneği farklı hücre dizilerine sunulur ve üzerinde çalışılabilmesi için çoğalmasına izin verilir. Bu tekniğin faydaları arasında genetik karakterizasyon, suş tiplemesi ve antiviral duyarlılık testi yapabilme yeteneği yer alır. Ancak, 3-7 günlük uzun geri dönüş süresi nedeniyle sınırlıdır, bu da hasta bakımında daha az, araştırma ortamlarında ise daha yaygın olmasını sağlar.[2]
Seroloji (serumdaki virüse özgü antikorların ölçümü) RSV tanısında sıklıkla kullanılmaz. Vücudun önemli bir serolojik yanıt oluşturması (ve serumda tespit edilebilecek antikorlarda önemli bir artış göstermesi) için gereken süre genellikle hasta bakımını yönlendirmede yararlı değildir.[1] %30'a kadar RSV enfeksiyonu olduğu belgelenmiş hastalarda seroloji sonuçları negatif olacaktır.[34] Bu nedenle bu yöntem genellikle araştırma ve gözetim çalışmaları için ayrılmıştır.[1]

RSV bronşiyolitli çocuklarda göğüs röntgeni bulguları genellikle belirgin değildir ve perihiler işaretler, yamalı hiperinflasyon ve atelektazi içerir.[15] Ancak Amerikan Pediatri Akademisi (AAP), klinik sonuçları değiştirmediği ve antibiyotik kullanımının artmasıyla ilişkili olduğu için RSV bronşiyoliti olduğu varsayılan çocuklar için rutin görüntülemeyi önermemektedir.[4][15]
Bronşiyolit tanısının belirsiz olduğu veya beklenmeyen bir kötüleşmenin olduğu durumlarda bazen göğüs röntgeni çekilmesi düşünülür.[4] RSV enfeksiyonu olan yetişkinlerde göğüs filmleri genellikle normaldir veya viral zatürre ile uyumlu, yama şeklinde iki taraflı sızıntılar gibi belirgin olmayan değişiklikler gösterir.[35]
Üst ve alt solunum yolu enfeksiyonu belirti ve semptomlarıyla başvuran bireylerde ayırıcı tanı, diğer viral enfeksiyonları (rinovirüs, metapneumovirüs ve grip gibi) ve birincil bakteriyel zatürreyi içerir. Çocuklarda, solunan yabancı cisimler ve kistik fibrozis veya astım gibi konjenital durumlar da dikkate alınmalıdır.[2]
Temel önleme tedbiri, hastalık bulaşmış kişilerle yakın temastan kaçınmaktır.[4]
Virüsün hastalık yükü ve hastalığa özgü tedavilerin eksikliği göz önüne alındığında, RSV aşısının keşfine ilgi ve araştırma vardır. Aşı geliştirme, ilerlemesini engelleyen engellerle karşılaştı. Bunların arasında, olgunlaşmamış bebek bağışıklık sistemi ve bebek bağışıklama‘sını zorlaştıran anne antikorlarının varlığı gibi bebeğe özgü faktörler vardır.[2]
RSV enfeksiyonu erken çocukluk döneminde yaygındır ve küresel hastalık yüküne önemli ölçüde katkıda bulunur. Şiddetli çocukluk çağı enfeksiyonları ile bunu takip eden solunum sorunları arasındaki ilişki, özellikle de bronşiyolit, tekrarlayan çocukluk çağı hırıltısı ve çocukluk çağı astımı arasındaki önerilen bağlantı tam olarak anlaşılamamıştır.
Aşıyla önlenebilir diğer solunum yolu patojenlerinden farklı olarak RSV'nin aşı geliştirme açısından zorlu olduğu kanıtlanmıştır. Süren çabalar, saha denemelerinin heyecanla beklendiği, dayanıklı koruma sağlayan aşılar oluşturmaya odaklanmaktadır.
Halen, etkili aşılar ve antiviral ilaçlar beklendiğinden, RSV hastalığının tedavisinde temel dayanak noktası destekleyici bakımdır. Antivirallerin ve aşıların ileri teşhis teknikleriyle bir araya getirilmesi, önümüzdeki yıllarda RSV'nin küresel etkisinin azaltılması konusunda umut vadetmektedir. Bu müdahaleler enfeksiyon dinamiklerini değiştirebilir ve RSV'nin dünya çapındaki topluluklar üzerindeki etkisini zayıflatabilir.[2]
Araştırılan muhtemel aşılar beş geniş kategoridir: canlı zayıflatılmış, protein alt birimi, vektör bazlı, virüs parçacık alt birimi ve haberci RNA. Her biri farklı bağışıklık tepkilerini hedefler ve dolayısıyla farklı risk altındaki gruplarda hastalıkları önlemek için daha uygun olabilir.
Canlı zayıflatılmış aşılar, RSV almamış bebeklerde bir miktar başarılı olmuştur. Diğer aşı adayları, hamile kadınlar ve yaşlılar da dahil olmak üzere yaşamları boyunca savunmasız nüfusları hedef almıştır.[2][36]

Başlıca ilaç geliştiricileri GSK ve Pfizer, 60 yaş ve üzeri yetişkinleri hedef alan RSV aşıları için Gıda ve İlaç Dairesinin onayını aldı. GSK'nın Arexvy'si bu yaş grubunda şiddetli semptomlara karşı %94 ve semptomatik RSV'ye karşı %83 etkiliyken, Pfizer'in Abrysvo'su 60 yaş ve üzeri yetişkinlerde şiddetli semptomlara karşı %86 ve semptomatik hastalıklara karşı %67 etkilidir.[39]
CDC paneli, sağlık hizmeti sağlayıcılarına danışılarak 60 yaş üstü yetişkinler için RSV aşısını önerdi. Aşıların 2023 veya 2024'te hazır olması beklenmektedir.[39]
Araştırmacılar, daha zorlu olan yeni doğan aşısına duyulan ihtiyacı ele alarak, RSV duyarlılığı için kritik bir dönem olan ilk altı ay boyunca bebekleri korumak için hamilelikle uygulanan bir yöntemi kullandılar.
FDA'nın danışma komitesi Pfizer'in ebeveyn RSV aşısını onayladı ve aşının yenidoğanlarda üç aya kadar şiddetli RSV'ye karşı %82 etkili olduğunu ve altı aya kadar %69 etkili olduğunu kabul etti. Oybirliğiyle etkinlik lehinde olsa da komite, aşılanan grupta biraz daha yüksek erken doğum oranına ilişkin endişeler nedeniyle güvenlik için 10'a 4 oy kullandı. GSK, aşı grubunda erken doğum olasılığının %38 daha yüksek olması nedeniyle kendi denemesini durdurdu.[39]

Mayıs 2023'te ABD Gıda ve İlaç İdaresi (FDA), ilk RSV aşıları, Arexvy (GSK plc tarafından geliştirilmiştir) ve Abrysvo'yu (Pfizer) onayladı.[5][6] 2023 yılında çok sayıda RSV aşı çalışması tamamlandı.[39]
Pasif aşılama, yüksek riskli bebeklerde RSV enfeksiyonunu ve hastaneye kaldırılmayı önlemek için vardır.
Tarihsel olarak, pasif bağışıklık sağlamak için RSV'ye özgü intravenöz immünglobin (IVIG) kullanıldı. Bu, hastalıktan iyileşen insan donörlerden RSV nötralize edici antikorlar (veya immünoglobinlerin) aylık olarak uygulanmasını içeriyordu. Bu antikor transferi, risk altındaki bebeklere kısa süreli aşılama sağlamada oldukça etkili olsa da, hem intravenöz uygulama ve maliyet nedeniyle sınırlıydı.[40]
O zamandan beri RSV-IVIG'nin yerini, kas enjeksiyonu yoluyla uygulanabilen bir monoklonal antikor (MAb) kullanımı almıştır. Palivizumab (Synagis), RSV virüsünün yüzey füzyon (F) proteinine karşı yönlendirilen monoklonal bir antikordur. 1998 yılında ruhsatlandırılmıştır ve hem RSV A hem de B'ye karşı geçici profilaksi sağlamada etkilidir. RSV mevsiminden hemen önce başlatılan ve genellikle beş ay boyunca devam eden aylık enjeksiyonlarla yapılır. Palivizumab'ın belirli yüksek riskli çocuk gruplarında (kronik akciğer hastalığı, doğuştan kalp hastalığı olanlar ve erken doğanlar gibi) hem hastaneye yatış oranlarını hem de tüm nedenlere bağlı ölüm oranlarını azalttığı gösterilmiştir.[31][41] Ancak maliyeti dünyanın birçok yerinde kullanımını sınırlamaktadır. O zamandan bu yana bu antikorun daha güçlü türevleri geliştirildi (motavizumab dahil) ancak önemli olumsuz olaylarla ilişkilendirildi.[42]
Amerikan Pediatri Akademisi (AAP 2014), aşağıdaki durumlar için RSV sezonunda palivizumab ile RSV profilaksisini önermektedir:[4]
AAP yönergelerine göre palivizumab profilaksisi aşağıdaki özelliklere sahip bebeklerde de düşünülebilir:[4]
Nirsevimab (Beyfortus), yenidoğanlarda ve bebeklerde ilk RSV sezonunda RSV alt solunum yolu hastalığının önlenmesi için onaylanmış başka bir antiviral monoklonal antikordur.[43] Nirsevimab'ın, etkili kalabilmesi için ayda bir kez dört defaya kadar enjekte edilmesi gereken palivizumab'ın aksine, tüm RSV sezonu boyunca süren yalnızca bir doza ihtiyacı var.[7] Nirsevimab, Avrupa Birliği'nde[44][45] ve Birleşik Krallık'ta[46] Kasım 2022'de ve Kanada'da Nisan 2023'te tıbbi kullanım için onaylandı.[7]
RSV enfeksiyonunun tedavisi öncelikle destekleyici bakıma odaklanır. Bu, hastanın nefesinin izlenmesini veya üst solunum yolundan salgıların uzaklaştırılması için aspirasyonun kullanılmasını içerebilir. Hava akışını iyileştirmek için takviye oksijen ayrıca bir burun kanülü veya yüz maskesi yoluyla da verilebilir. Ciddi solunum yetmezliği vakalarında, solunumu desteklemek için entübasyon ve mekanik havalandırma gerekebilir. Dehidrasyon belirtileri mevcutsa ağızdan veya IV yoluyla da sıvı verilebilir.[40]
RSV bronşiyoliti nedeniyle hastaneye yatırılan bebeklerde ek destekleyici tedaviler araştırılmıştır. Ek destekleyici tedaviler şunlardır:
Astımı tedavi etmede yaygın kullanılan ilaçlardan olan Bronkodilatörler, bazen RSV enfeksiyonuyla ilişkili hırıltıyı tedavi etmek için kullanılır. Bu ilaçlar (albuterol veya salbutamol gibi) hava akışının iyileştirilmesini sağlamak için hava yollarındaki kasları gevşeten beta-agonistlerdir. Ancak bronkodilatörlerin RSV enfeksiyonu olanlarda enfeksiyonun klinik şiddetini veya hastaneye kaldırılma oranını iyileştirdiği bulunmamıştır. Sınırlı yararları ve yan etki profilleri göz önüne alındığında, RSV bronşiyolitinde kullanımları rutin olarak önerilmemektedir.[40][55]
Antibiyotik tedavisi RSV ile ilişkili bronşiyolit veya viral pnömoninin tedavisi için uygun değildir.[57] Antibiyotikler RSV gibi viral patojenleri değil, bakteriyel patojenleri hedefler. Bununla birlikte, ikincil bir bakteriyel enfeksiyonun geliştiğine dair açık kanıtlar varsa antibiyotikler düşünülebilir.
Kulak enfeksiyonları RSV bronşiolitli az sayıda bebekte de gelişebilir, bu durumda bazen ağızdan antibiyotikler kullanılabilir.[40]
Aşıların ötesinde, AstraZeneca ve Sanofi, bir yaşın altındaki bebeklerde RSV vakalarına karşı %75 etkinliğe sahip profilaktik bir monoklonal antikor olan nirsevimab'ı tanıttı. Avrupa, nirsevimab'ı Kasım 2022'de onayladı ve FDA, Temmuz 2023'te aynı şeyi yaptı. Benzer bir monoklonal antikor olan Merck'in klesrovimab'ı, ileri aşamadaki denemelerde bulunur.[39]
Dünya çapında RSV, bebeklerde ve 5 yaşın altındaki çocuklarda bronşiyolit ve zatürrenin önde gelen nedenidir. Ciddi enfeksiyon riski yaşamın ilk 6 ayında en yüksektir. RSV ile enfekte olanların %2-3'ünde bronşiyolit gelişir ve hastaneye kaldırılmayı gerektirir.[58]
Dünyada her yıl yaklaşık 30 milyon akut solunum yolu hastalığı ve 60.000'den fazla çocuk ölümü RSV'den kaynaklanmaktadır.
Bebeklerin tahminen %87'si 18 aylık olduklarında RSV enfeksiyonu geçirmiş olur ve neredeyse tüm çocuklar 3 yaşına gelindiğinde enfekte olur.
Amerika Birleşik Devletleri'nde, 5 yaşın altındaki çocuklarda akut solunum yolu enfeksiyonu nedeniyle hastaneye kaldırılanların %20'sinden RSV sorumludur. Bununla birlikte, RSV'ye bağlı ölümlerin büyük çoğunluğu, temel destekleyici bakıma erişimi olmayan az gelirli ülkelerde meydana gelmektedir.[2]
Sağlıklı genç yetişkinlerin RSV nedeniyle hastaneye kaldırılmayı gerektiren ciddi hastalık geliştirmesi nadirdir. Ancak artık yaşlılar ve altta yatan kalp veya akciğer hastalıkları olanlar da dahil olmak üzere belirli yetişkin nüfusta önemli bir hastalık ve ölüm nedeni olduğu kabul edilmektedir. Yaşlı yetişkinler arasındaki klinik etkisinin gribe benzer olduğu tahmin edilmektedir.[21]
Her yıl huzurevinde kalanların yaklaşık %5-10'u, önemli oranda zatürre ve ölümle birlikte RSV enfeksiyonu yaşar. RSV ayrıca yetişkin toplum kökenli zatürre vakalarının %2-5'inden sorumludur.[21]
Hem yetişkinlerde hem de çocuklarda bağışıklık baskılanması, RSV enfeksiyonuna duyarlılığı artırır. HIV ile yaşayan çocukların akut hastalığa yakalanma olasılığı daha yüksektir ve HIV olmayan çocuklara kıyasla hastaneye kaldırılma gerektirme olasılıkları 3,5 kat daha fazladır.[2]
Kemik iliği nakli öncesinde kemik iliği nakli yapılan hastalar özellikle yüksek risk altındadır; RSV, bu nüfusdaki viral enfeksiyonların neredeyse yarısını oluşturur. Bu grup aynı zamanda RSV zatürresi olanlar arasında %80'e varan ölüm oranları göstermiştir.[21]
Enfeksiyon toplum içinde meydana gelse de, hastane kaynaklı enfeksiyonun bağışıklık sistemi baskılanmış kişiler arasındaki vakaların %30-50'sinden sorumlu olduğu düşünülmektedir.[21]
RSV mevsimselliği dünya çapında değişiklik gösterir. Ilıman iklim’lerde enfeksiyon oranları soğuk kış aylarında en yüksek olma eğilimindedir. Bu genellikle artan iç mekan kalabalığına ve düşük sıcaklıklarda artan viral stabiliteye atfedilir. Ancak tropik ve kuzey kutbuna yakın iklimlerde, yıllık değişim daha az tanımlanmıştır ve yağışlı mevsimde daha yaygın olduğu görülmektedir.[1][2]
Yıllık salgınlara genellikle birkaç farklı viral suşun varlığı neden olur. A grubu virüsler daha yaygın olmasına rağmen, A ve B alt tipi virüsler genellikle belirli bir coğrafi bölgede aynı anda dolaşır.[21]
COVID-19'dan sorumlu virüs olan SARS-CoV-2 enfeksiyonları, RSV enfeksiyonu riskinin daha yüksek olmasına neden olabilir.[59] Kasım 2022'de yenidoğanlarda RSV nedeniyle hastaneye kaldırılma oranı, 2018'deki oranın yedi katıydı. Bu, artan grip dolaşımıyla birleştiğinde ABD'nin Oregon eyaletinin olağanüstü hal ilan etmesine neden oldu. Çocuk Hastaneleri Birliği ve Amerikan Pediatri Akademisi, ABD Başkanı Joe Biden'dan olağanüstü hal ilan etmesini istedi.[60]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.