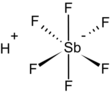
Floroantimonik asit
From Wikipedia, the free encyclopedia
Floroantimonik asit (HSbF6) hidrojen florür ve antimon pentaflorürün farklı oranlardaki karışımıdır.[1] Bu karışımlardan 1:1 kombinasyonu, bilinen en güçlü süperasit formunu oluşturur. Öyle ki, bu form, hidrokarbonları iyonize ederek karbokatyonlar ve H2 oluşturabilmektedir.[2]
| |||
| Adlandırmalar | |||
|---|---|---|---|
Fluoroantimonic acid | |||
| Tanımlayıcılar | |||
3D model (JSmol) |
|||
| ECHA InfoCard | 100.037.279 | ||
PubChem CID |
|||
CompTox Bilgi Panosu (EPA) |
|||
| |||
| Özellikler | |||
| Molekül formülü | HSbF6 | ||
| Molekül kütlesi | 236.76 g mol-1 | ||
| Görünüm | Renksiz sıvı | ||
| Tehlikeler | |||
| İş sağlığı ve güvenliği (OHS/OSH): | |||
| Ana tehlikeler | Aşındırıcı | ||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |||
| Bilgi kutusu kaynakları | |||
Hidrojen florür (HF) ve SbF5 arasında gerçekleşen tepkime ekzotermiktir. Çok iyi bir oksitleyici olan HF, SbF5 moleküllerine saldırarak addüksiyon oluşumuna neden olur. Flooroantimonik molekülde, anyon, her ne kadar resmi olarak "koordinasyon bağı kurmayan" olarak tanımlansa da, hidrojene koordinasyon bağıyla bağlanır. Bunun sebebi, bu anyonun hem çok güçsüz bir nükleofil, hem de güçsüz bir baz olmasıdır.
Proton her ne kadar etkili bir şekilde "çıplak" olarak adlandırılsa da, gerçekte hidronyum katyonunda olan duruma benzer bir şekilde, florüre çok zayıf bir koordine kovalent bağ ile bağlanır.[3] Ancak bu bağın aşırı zayıflığı, sistemin aşırı asiditesine katkıda bulunur. Floroantimonik asit, %100'lük bir sülfürik asit çözeltisinden 2×1019 (20 kentilyon) kat daha güçlüdür.[4]