Loading AI tools
โปรตีนของสัตว์เลี้ยงลูกด้วยนม พบใน Homo sapiens จากวิกิพีเดีย สารานุกรมเสรี
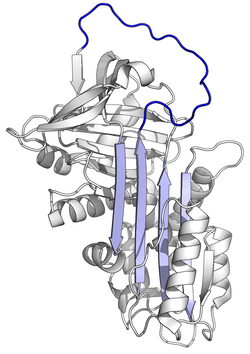
แอลฟาวัน-แอนติทริปซิน (อังกฤษ: Alpha-1 antitrypsin หรือ α1-antitrypsin; สัญลักษณ์: A1AT, α1AT, A1A , AAT) เป็นโปรตีนในกลุ่มเซอร์ปิน ถูกถอดรหัสได้จากยีน SERPINA1 บนโครโมโซมคู่ที่ 14 ออกฤทธิ์เป็นสารต้านโปรตีเอส จึงเป็นที่รู้จักกันในอีกชื่อ คือ alpha1–proteinase inhibitor (A1PI) หรือ alpha1-antiproteinase (A1AP) เนื่องจากสามารถออกฤทธิ์ต้านโปรตีเอสได้หลายชนิด ไม่เฉพาะแค่ทริปซิน[3] ในเอกสารชีวการแพทย์สมัยก่อน บางครั้งอาจเรียกโปรตีนชนิดนี้ว่า serum trypsin inhibitor (STI, สารต้านทริปซินในเลือด) เนื่องจากในการศึกษาช่วงแรกนั้น โปรตีนชนิดนี้มีความคุณสมบัติเด่นในการเป็นตัวยับยั้งทริปซิน[4] ด้วยการที่ออกฤทธิ์เป็นสารต้านเอนไซม์ A1AT จึงช่วยปกป้องเนื้อเยื่อต่างๆ จากเอนไซม์หลายชนิดที่ถูกหลั่งออกมาจากเซลล์ที่เกี่ยวเนื่องกับการอักเสบ โดยเฉพาะอย่างยิ่ง นิวโตรฟิลอีลาสเตส[4] ซึ่งเป็นเอนไซม์ที่ถูกหลั่งออกมาเพื่อทำลายแบคทีเรียแปลกปลอม และอาจทำให้เนื้อเยื่อปกติของร่างกายได้รับความเสียดายได้[5] นอกจากนี้ A1AT ยังสามารถจับกับอีลาสเตสบนผิวเซลล์ที่ทำหน้าที่ถ่ายโอนสัญญาณในการกระตุ้นการเคลื่อนที่ของเซลล์ภูมิคุ้มกันอื่นได้ด้วย[6]
| Serpin family A member 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifiers | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Aliases | protease inhibitor 1 (anti-elastase)alpha-1-antitrypsinepididymis secretory sperm binding proteinalpha-1 antitrypsinalpha-1 protease inhibitoralpha-1-antiproteinaseserine (or cysteine) proteinase inhibitorclade Amember 1serpin peptidase inhibitor clade A (alpha-1antiproteinaseantitrypsin) member 1serpin peptidase inhibitorclade A (alpha-1 antiproteinaseantitrypsin)member 1serpin peptidase inhibitor clade A member 1alpha-1-antitrypsin short transcript variant 1C5alpha-1-antitrypsin nullalpha-1-antitrypsinalpha-1-antitrypsin short transcript variant 1C4serpin A1SERPINA1alfa-1-antitrypsin | ||||||||||||||||||||||||||||||||||||||||||||||||||
| External IDs | GeneCards: | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Wikidata | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
 | |
| ข้อมูลทางคลินิก | |
|---|---|
| ชื่อทางการค้า | Aralast, Zemaira, Glassia, others[1] |
| AHFS/Drugs.com | โมโนกราฟ |
| ข้อมูลทะเบียนยา |
|
| ช่องทางการรับยา | ฉีดเข้าหลอดเลือดดำ |
| รหัส ATC | |
| กฏหมาย | |
| สถานะตามกฏหมาย |
|
| ตัวบ่งชี้ | |
| |
| เลขทะเบียน CAS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| ChEMBL | |
| ECHA InfoCard | 100.029.919 |
| ข้อมูลทางกายภาพและเคมี | |
| สูตร | C2001H3130N514O601S10 |
| มวลต่อโมล | 44324.5 g·mol−1 |
| (verify) | |
A1AT มีค่าอ้างอิงในกระแสเลือดระหว่าง 0.9–2.3 กรัม/ลิตร (ในสหรัฐ ค่านี้จะแสดงในหน่วย มิลลิกรัม/เดซิลิตร หรือไมโครโมล) แต่ค่าความเข้มข้นนี้อาจเพิ่มขึ้นในภาวะที่มีการอักเสบเฉียบพลัน[4] กรณีที่มีปริมาณหรือการทำหน้าที่ของ A1AT ผิดปกติ เช่น ในภาวะพร่องแอลฟาวัน-แอนติทริปซิน จะทำให้มีนิวโตรฟิลอีลาสเตสในรูปอิสระมากเกินไปจนก่อให้เกิดความเสียหายแก่อีลาสติน เป็นผลให้เนื้อเยื่อปอดมีความยืดหยุ่นลดน้อยลง และเกิดความผิดปกติของระบบทางเดินหายใจได้ในที่สุด อาทิ โรคปอดอุดกั้นเรื้อรัง[7] โดยปกติแล้ว A1AT ซึ่งถูกสร้างที่ตับจะเข้าสู่กระแสเลือดเพื่อเข้าจับกับเอนไซม์เป้าหมาย แต่ในกรณีภาวะพร่องแอลฟาวัน-แอนติทริปซินนั้น A1AT จะไม่สามารถเข้าสู่กระแสเลือดได้ และทำให้เกิดโรคตับแข็งได้ในที่สุด โดยหากเกิดอาจจำเป็นต้องมีการปลูกถ่ายตับเพื่อรักษาความผิดปกติดังกล่าว[8] นอกเหนือจากตับแล้ว A1AT ยังถูกสร้างได้โดยเซลล์ในไขกระดูก, เซลล์ลิมโฟไซต์และโมโนไซต์ในระบบน้ำเหลือง รวมไปถึงพาเนทเซลล์ในลำไส้เล็กด้วย[9]
การยับยั้งการทำงานของ A1AT โดยเอนไซม์อื่นที่ไม่ใช่อีลาสเตสที่ถูกหลั่งออกมาในระหว่างที่มีการอักเสบหรือการติดเชื้อจะทำให้เกิดการเคลื่อนที่ของทีเซลล์ไปยังตำแหน่งที่เกิดความผิดปกติได้อย่างแม่นยำ (T cell)by ด้วยเหตุนี้ จึงพออนุมานได้ว่า นอกจาก A1AT จะมีบทบาทในการเคลื่อนที่ของลิมโฟไซต์ไปยังเนื้อเยื่อเป้าหมาย ซึ่งเป็นกระบวนการตอบสนองขั้นต้นของระบบภูมิคุ้มกัน ยังมีส่วนสำคัญต่อการกระตุ้นระบบภูมิคุ้มกันในระยะหลังด้วย[10]
A1AT จัดเป็นทั้งสารยับยั้งโปรตีเอสที่สร้างได้ภายในร่างกายและยาที่จัดเป็นสารยับยั้งโปรตีเอสที่รับจากภายนอก โดย A1AT ในรูปแบบยาจะได้จากการสกัดจากเลือดที่ได้จากการบริจาคโลหิต และจำหน่ายในตลาดยา ทั้งภายใต้ชื่อที่ไม่เป็นกรรมสิทธิ์คือ alpha1–proteinase inhibitor และชื่อการค้าต่างๆ (ได้แก่ Aralast NP, Glassia, Prolastin, Prolastin-C และ Zemaira) นอกจากนี้ ในปัจจุบันยังมีการใช้ A1AT ที่ได้จากการสร้างดีเอ็นเอสายผสมแต่จำกัดแค่การใช้ในงานวิจัยทางการแพทย์เท่านั้น
แอลฟาวัน-แอนติทริปซินถูกค้นพบครั้งแรกโดย Fermi และ Pernossi เมื่อ ค.ศ. 1894[11] และสามารถสกัดแยกตัวอย่างออกมาได้สำเร็จในปี ค.ศ. 1955 โดย Schultze และได้มีการกำหนดให้เรียกสารนี้ว่า แอลฟาวัน-แอนติทริปซิน เนื่องจากสารดังกล่าวสามารถสกัดได้จากแอลฟาวัน-กลอบูลินและมีความสามารถในการยับยั้งการทำงานของทริปซิน[12] ในปี ค.ศ. 1965 Axelsson และ Laurell ได้ค้นพบว่า ความผันแปรทางพันธุกรรมของอัลลีลที่สร้าง A1AT อาจเกี่ยวข้องกับโรคที่เกิดจากความผิดปกติทางพันธุกรรมบางอย่าง[13]
ในปี ค.ศ. 1985 ได้มีการคิดค้นระบบการตั้งชื่อของโปรตีนในกลุ่มสารที่ออกฤทธิ์ยับยั้งซีรีสโปรตีเอส (serine proteinase inhibitor) หรือเซอร์ปิน มาใช้ จึงได้มีการกำหนดชื่อให้แอลฟาวัน-แอนติทริปซิน ซึ่งเป็นโปรตีนชนิดแรกที่ถูกค้นพบในกลุ่มนี้ให้อยู่ในเคลดเอ ลำดับที่ 1 ใช้ชื่อสัญลักษณ์แทนว่า SERPINA1[14]
โปรตีนในกลุ่มเซอร์ปินส่วนใหญ่จะเข้าจับและยับยั้งการทำงานของเอนไซม์เป้าหมายโดยการสร้างพันธะโคเวเลนต์ ซึ่งในสภาวะปกติเอนไซม์เหล่านี้จะถูกหลั่งออกมาในระดับความเข้มข้นที่ต่ำมากและจะถูกกำจัดออกไปจากระบบโดยโปรตีนที่ต้านการทำงานของเอนไซม์เหล่านั้นได้ภายในระยะเวลาอันรวดเร็ว ซึ่ง A1AT ก็เป็นโปรตีนอีกชนิดหนึ่งที่มีการทำงานในรูปแบบดังกล่าว ในแต่สภาวะที่เกิดการอักเสบขึ้นเฉียบพลัน จะทำให้เกิดการกระตุ้นให้นิวโตรฟิลหลั่งเอนไซม์เหล่านี้มากขึ้น โดยเฉพาะเอนไซม์อีลาสเตส ทั้งเพื่อลดความเสียหายที่อาจเกิดกับเนื้อเยื่อที่เป็นผลมาจากสิ่งแปลกปลอมหรือการอักเสบนั้นๆ
นอกจากจะยับยั้งการทำงานของอีลาสเตสเพื่อไม่ให้เกิดความเสียหายกับเนื้อเยื่อมาเกินเกินไป A1AT ยังสามารถเหนี่ยวนำให้เกิดการเคลื่อนที่ของลิมโฟไซต์ผ่านเนื้อเยื่อต่างๆ ซึ่งรวมไปถึงการกระตุ้นให้ทีเซลล์ที่ยังไม่เจริญหรือไทโมไซต์ ซึ่งถูกสร้างขึ้นในไขกระดูกให้เคลื่อนที่ผ่านกระแสเลือดเพื่อไปยังต่อมไทมัส ที่ซึ่งไทโมไซต์จะถูกเปลี่ยนเป็นทีเซลล์จะถูกเปลี่ยนให้อยู่ในรูปที่เจริญเต็มที่และทำงานได้ ซึ่งจะถูกหลั่งเข้าสู่กระแสเลือดเพื่อตอบสนองปัจจัยกระตุ้นต่อไป[15]

ความผิดปกติที่เกี่ยวเนื่องกับ A1AT รวมถึงภาวะพร่องแอลฟาวัน-แอนติทริปซิน จัดเป็นความผิดปกติทางพันธุกรรมที่ถ่ายทอดแบบยีนเด่นอีกชนิดหนึ่ง (autosomal dominant hereditary disorders) ซึ่งจะการเกิดการทำลายเนื้อเยื่อต่างๆ อย่างต่อเนื่องโดยปราศจากการยับยั้งจากสารต้านเอนไซม์ โดยเฉพาะเนื้อเยื่อปอด ซึ่งอาจทำให้เกิดโรคถุงลมโป่งพองได้ในที่สุด[16] นอกจากนี้ยังมีหลักฐานเชิงประจักษ์ที่แสดงให้เห็นว่า การสูบบุหรี่จะทำให้เกิดการออกซิเดชันของกรดอะมิโนมีไธโอนีนตำแหน่งที่ 358 ของ A1AT ซึ่งเป็นส่วนสำคัญที่ใช้ในการเข้าจับกับเอนไซม์อีลาสเตส[17] ด้วยเหตุผลดังข้างต้น จึงอาจคาดการณ์ได้ว่า กระบวนการดังกล่าวเป็นอีกสาเหตุหนึ่งที่ทำให้ผู้สูบบุหรี่หรือผู้สูบบุหรี่มือสองสามารถเกิดภาวะถุงลมโป่งพองได้ นอกจากนี้ เนื่องด้วย A1AT ถูกพบได้มากที่ตับ การกลายพันธุ์ของยีน SERPINA1 ที่ควบคุมการถอดรหัสการสร้าง A1AT จะทำให้เกิดการม้วนพับของสายโปรตีนและการหลั่ง A1AT ออกสู่กระแสเลือดผิดปกติ จนนำไปสู่การเกิดโรคตับแข็งในที่สุด ซึ่งความผิดปกติดังกล่าวสามารถตรวจสอบได้ด้วยการเจาะชื้นเนื้อตับเพื่อนำมาย้อมสีชนิด Periodic acid–Schiff stain (PAS) ซึ่งจะพบกลุ่มก้อนที่เกิดจากสีย้อมมากมายภายในบริเวณ periportal ของเซลล์ตับ.
นอกจากนี้ยังมีรายงานการเกิดการกลายพันธุ์ของยีน SERPINA1 โดยเกิดการแทนที่กรดอะมิโนมีไธโอนีนที่ตำแหน่ง 358 ด้วยอาร์จินีน ซึ่งทำให้ A1AT ที่เกิดการกลายพันธุ์นี้ (α1-Antitrypsin Pittsburgh; PiPittsburgh) มีฤทธิ์คล้ายแอนติทรอมบิน III คือ ต้านการทำงานของทรอมบิน เป็นผลให้เกิดภาวะเลือดออกง่าย และเสียชีวิตได้ในที่สุด[18]
ในผู้ป่วยโรคข้ออักเสบรูมาตอยด์พบว่ามีการสร้างภูมิต้านเนื้อเยื่อตนเองขึ้นมาในน้ำไขข้อเพื่อต้าน A1AT ที่ผ่านการเกิดปฏิกิริยาคาร์บามิเลชั่นแล้ว (carbamylated A1AT) ซึ่งบ่งชี้ได้ว่า A1AT อาจมีบทบาทในการต้านการอักเสบหรือปกป้องเนื้อเยื่ออื่นๆ อีกนอกเหนือจากเนื้อเยื่อปอด โดยภูมิต้านทานดังกล่าวมีความสัมพันธ์กันกับอาการของโรคที่รุนแรงขึ้น ซึ่งจะสามารถติดตามวัดค่าได้หลายปีก่อนที่จะเริ่มมีการแสดงอาการของโรค และอาจใช้ทำนายการพัฒนาของโรคในผู้ป่วยกลุ่มดังกล่าวได้ ดังนั้น ในปัจจุบันจึงมีการพัฒนาวิธีการตรวจวัด carbamylated A1AT เพื่อใช้เป็นตัวบ่งชี้ทางชีวภาพ (antigenic biomaker) ในกลุ่มผู้ป่วยดังกล่าว[19]
A1AT มีน้ำหนักโมเลกุลประมาณ 52-กิโลดัลตัน ทั้งชนิดที่เป็นเซอร์ปินในร่างกายและชนิดที่จัดเป็นยา จัดเป็นเซอร์ปินที่มีความโดดเด่นและเป็นที่สนใจในการศึกษาทางการแพทย์ปัจจุบันมากที่สุด ถูกถอดรหัสได้จากยีน SERPINA1 ที่อยู่บนแขนข้างยาวของโครโมโซมคู่ที่ 14 (14q32.1) ความผันแปรทางพันธุกรรมของยีนในตำแหน่งดังกล่าวถูกค้นพบแล้วมากกว่า 100 รูปแบบ โดยกลุ่มประชากรในยุโรปตะวันตกเฉียงเหนือถือเป็นกลุ่มประชากรที่มีความเสี่ยงต่อการได้รีบยีนกลายพันธุ์ชนิด Z ของ SERPINA1 (Glu342Lys บน M1A, rs28929474) ซึ่งเป็นรูปแบบการกลายพันธุ์ที่พบได้มากที่สุดของยีนในตำแหน่งดังกล่าว
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.