Loading AI tools
จากวิกิพีเดีย สารานุกรมเสรี
โรคเกาต์ (หรือที่รู้จักกันในนาม โพดากรา เมื่อเกิดกับนิ้วหัวแม่เท้า)[1] เป็นภาวะความเจ็บป่วยที่มักสังเกตได้จากอาการไขข้ออักเสบกำเริบเฉียบพลันซ้ำ ๆ—มีอาการแดง ตึง แสบร้อน บวมที่ข้อต่อ ข้อต่อกระดูกฝ่าเท้า-นิ้วเท้าที่โคนนิ้วหัวแม่เท้ามักได้รับผลกระทบบ่อยที่สุด (ประมาณ 50% ของผู้ป่วย) นอกจากนี้ ยังอาจพบได้ในรูปแบบของก้อนโทไฟ นิ่วในไต หรือ โรคไตจากกรดยูริก โรคนี้เกิดจากการมีระดับกรดยูริกในเลือดสูง กรดยูริกตกผลึกแล้วมาจับที่ข้อต่อ เส้นเอ็น และ เนื้อเยื่อโดยรอบ
การวินิจฉัยทางคลินิกทำได้โดยการตรวจผลึกที่มีลักษณะเฉพาะในน้ำไขข้อ รักษาได้โดยยาแก้อักเสบชนิดไม่ใช่สเตอรอยด์ (NSAIDs) สเตอรอยด์ หรือ โคลชิซีน ซึ่งทำให้ผู้ป่วยมีอาการดีขึ้นได้ หลังจากอาการข้ออักเสบกำเริบเฉียบพลันผ่านไปแล้ว ระดับของกรดยูริกในเลือดมักจะลดลงได้โดยการปรับเปลี่ยนวิถีชีวิต และในผู้ที่มีอาการกำเริบบ่อยอาจใช้อัลโลพูรินอลหรือโพรเบเนซิดเพื่อให้การป้องกันในระยะยาว
จำนวนผู้ป่วยโรคเกาต์เพิ่มสูงขึ้นในช่วงหลายสิบปีนี้ โดยมีผลกระทบกับ 1-2% ของชาวตะวันตกในช่วงใดช่วงหนึ่งของชีวิต จำนวนที่เพิ่มขึ้นนี้เชื่อว่าเป็นผลมาจากปัจจัยเสี่ยงที่พบมากขึ้นในประชากร ยกตัวอย่างเช่น กลุ่มอาการเมตาบอลิก อายุขัยที่ยืนยาวขึ้น และ พฤติกรรมการกินอาหารที่เปลี่ยนแปลงไป แต่เดิมนั้นโรคเกาต์เคยได้ชื่อว่าเป็น "โรคของราชา" หรือ "โรคของคนรวย"

โรคเกาต์สามารถพบได้หลายรูปแบบ ที่พบมากที่สุดคืออาการไขข้ออักเสบกำเริบแบบเฉียบพลัน (ข้อต่อแดง ตึง แสบร้อน บวม)[2] ข้อต่อกระดูกฝ่าเท้า-นิ้วเท้าที่โคนนิ้วหัวแม่เท้ามักได้รับผลกระทบมากที่สุด โดยคิดเป็นจำนวนครึ่งหนึ่งของผู้ป่วยทั้งหมด[3] ข้อต่ออื่น ๆ เช่น ส้นเท้า หัวเข่า ข้อมือ และ นิ้วมือก็อาจได้รับผลกระทบได้เช่นกัน[3] ความเจ็บปวดที่ข้อต่อมักเริ่มขึ้นประมาณ 2–4 ชั่วโมงในเวลากลางคืน[3] เหตุผลที่เกิดอาการกำเริบในเวลากลางคืนเนื่องจากอุณหภูมิของร่างกายลดลงในช่วงเวลานั้น[1] อาจมีอาการอื่น ๆ เกิดขึ้นพร้อมกับอาการปวดข้อบ้าง เช่น ความล้าและมีไข้สูง[1][3]
ระดับของกรดยูริกที่สูงอย่างต่อเนื่องเป็นเวลานาน (ภาวะกรดยูริกในเลือดสูง) อาจส่งผลให้เกิดอาการอื่น ๆ รวมถึงการจับตัวของผลึกกรดยูริกที่แข็งแต่ไม่แสดงอาการเจ็บปวดที่รู้จักกันในนามของ ก้อนโทไฟ การขยายตัวของก้อนโทไฟอาจนำไปสู่โรคไขข้ออักเสบเรื้อรังเนื่องจากการผุกร่อนของกระดูก[4] นอกจากนี้ ระดับที่สูงของกรดยูริกยังอาจนำไปสู่การเกิดผลึกในไต ก่อให้เกิดนิ่วตามด้วยโรคไตจากกรดยูริก[5]
ภาวะกรดยูริกในเลือดสูง เป็นสาเหตุพื้นฐานของโรคเกาต์ ภาวะนี้อาจเกิดขึ้นได้ด้วยสาเหตุมากมาย ไม่ว่าจะเป็นอาหาร พันธุกรรม หรือ การขับเกลือยูเรทซึ่งเป็นเกลือของกรดยูริกที่ไม่เพียงพอ[2] การขับกรดยูริกไม่เพียงพอของไตเป็นสาเหตุหลักของภาวะกรดยูริกในเลือดสูงในผู้ป่วยประมาณ 90% ในขณะที่การผลิตกรดมากเกินไปเป็นสาเหตุของผู้ป่วยน้อยกว่า 10%[6] ประมาณ 10% ของผู้ป่วยที่มีภาวะกรดยูริกในเลือดสูงจะกลายเป็นโรคเกาต์ในช่วงใดช่วงหนึ่งของชีวิต[7] อย่างไรก็ตาม อัตราความเสี่ยงจะแตกต่างกันไปขึ้นอยู่กับระดับของภาวะกรดยูริกในเลือดสูง หากระดับนี้อยู่ระหว่าง 415 ถึง 530 μmol/l (7 ถึง 8.9 mg/dl) อัตราความเสี่ยงจะอยู่ที่ 0.5% ต่อปี ในขณะที่ผู้ป่วยที่มีระดับกรดยูริกในเลือดสูงกว่า 535 μmol/l (9 mg/dL) อัตราความเสี่ยงจะอยู่ที่ 4.5% ต่อปี[1]
พฤติกรรมการบริโภคอาหารเป็นสาเหตุของการเกิดโรคเกาต์ประมาณ 12%[2] ทั้งนี้รวมถึงการบริโภคเครื่องดื่มแอลกอฮอล์ เครื่องดื่มน้ำหวานที่ผสมฟรักโทส เนื้อสัตว์ และ อาหารทะเล[4][8] ปัจจัยอื่น ๆ ได้แก่ การบาดเจ็บทางร่างกาย และ การผ่าตัด[6] การวิจัยล่าสุดพบว่าปัจจัยเกี่ยวกับพฤติกรรมการบริโภคอาหารที่เคยเชื่อว่าเกี่ยวข้องนั้น ในความเป็นจริงไม่ได้เกี่ยวเลย ไม่ว่าจะเป็นการบริโภคผักที่มีพิวรีนสูง (ตัวอย่างเช่นถั่ว ถั่วลันเตา ถั่วเลนทิล และ ผักโขม) และ โปรตีนทุกชนิด[9][10] การบริโภคกาแฟ วิตามินซี และ ผลิตภัณฑ์นม ตลอดจนการออกกำลังกายดูเหมือนจะช่วยลดความเสี่ยง[11][12][13] ที่เชื่อเช่นนั้นส่วนหนึ่งเนื่องมาจากผลของอาหารเหล่านี้ในการลดภาวะดื้อต่ออินซูลิน[13]
การเกิดโรคเกาต์ส่วนหนึ่งมาจากสาเหตุทางพันธุกรรมซึ่งเอื้อต่อประมาณ 60% ของความแปรปรวนในระดับของกรดยูริก[6] ยีนสามตัวคือSLC2A9 SLC22A12 และ ABCG2 ถูกพบว่ามักจะเกี่ยวข้องกับโรคเกาต์และความแปรปรวนของยีนเหล่านี้สามารถเพิ่มความเสี่ยงได้ประมาณสองเท่า[14][15] การกลายพันธุ์ที่ก่อให้เกิดการสูญเสียฟังก์ชันของโปรตีนใน SLC2A9 และ SLC22A12 ก่อให้เกิดภาวะกรดยูริกในเลือดสูงทางพันธุกรรมโดยการลดการดูดซึมและไม่มีการต่อต้านการหลั่งเกลือยูเรท[15] ความผิดปกติทางพันธุกรรมที่หายากบางอย่าง เช่น โรคไตในเด็กที่ถ่ายทอดทางพันธุกรรมจากภาวะกรดยูริกในเลือดสูง โรคถุงน้ำในไตชั้นกลาง การสังเคราะห์ฟอสโฟไรโบซิลไพโรฟอสเฟตมากเกินไป การขาดไฮโปแทนซีน – กวานีนฟอสโฟไรโบซิลทรานสเฟอเรส เช่นที่พบใน กลุ่มอาการ Lesch-Nyhan เกิดความซับซ้อนเพราะโรคเกาต์[6]
โรคเกาต์มักเกิดขึ้นพร้อมกับปัญหาทางการแพทย์อื่น ๆ กลุ่มอาการเมตาบอลิกซึ่งรวมโรคอ้วนลงพุง ความดันโลหิตสูง ภาวะดื้อต่ออินซูลิน และ ระดับไขมันในเลือดผิดปกติ เกิดขึ้นในเกือบ 75% ของผู้ป่วย[3] ภาวะอื่น ๆ ที่มักเกิดความซับซ้อนเพราะโรคเกาต์รวมถึง: ภาวะเม็ดเลือดแดงมาก โรคพิษตะกั่ว ไตวาย โรคโลหิตจาง โรคสะเก็ดเงิน และ การปลูกถ่ายอวัยวะ[6][16] ค่าดัชนีมวลกายที่มากกว่าหรือเท่ากับ 35 เพิ่มความเสี่ยงของการเป็นโรคเกาต์ขึ้นเป็นสามเท่าในเพศชาย[10] การสัมผัสสารตะกั่วเป็นเวลาติดต่อกันและเครื่องดื่มแอลกอฮอล์ที่มีสารตะกั่วปนเปื้อนเป็นปัจจัยเสี่ยงต่อการเกิดโรคเกาต์ เนื่องจากผลกระทบที่เป็นอันตรายของสารตะกั่วต่อการทำงานของไต[17] กลุ่มอาการ Lesch-Nyhan มักจะเกี่ยวข้องกับโรคข้ออักเสบเพราะโรคเกาต์
ยาขับปัสสาวะถูกเชื่อมโยงกับสาเหตุการกำเริบของโรคเกาต์ตลอดมา อย่างไรก็ตาม การใช้ไฮโดรคลอโรไทอาไซด์ในปริมาณน้อยดูเหมือนจะไม่ได้เพิ่มความเสี่ยง[18] ยาอื่น ๆ ที่เกี่ยวข้องรวมถึงไนอาซิน และ แอสไพริน (กรดอะซิทิลซาลิไซลิก)[4] สารกดภูมิคุ้มกันต่าง ๆ ไซโคลสปอริน และ ทาโครลิมุส ก็เกี่ยวข้องกับการเกิดโรคเกาต์ด้วยเช่นกัน[6] โดยเฉพาะอย่างยิ่งยาตัวแรกเมื่อใช้ร่วมกับไฮโดรคลอโรไทอาไซด์[19]
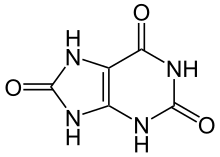
โรคเกาต์เป็นความผิดปกติของการเผาผลาญพิวรีน[6]และเกิดขึ้นเมื่อสารสังเคราะห์สุดท้าย กรดยูริก ตกผลึกในรูปแบบของโมโนโซเดียมยูเรทที่ตกตะกอนในข้อต่อ บนเส้นเอ็น และ เนื้อเยื่อรอบ ๆ[4] จากนั้น ผลึกเหล่านี้จะก่อให้เกิดปฏิกิริยาการอักเสบเนื่องจากภูมิคุ้มกัน [4] โดยหนึ่งในโปรตีนที่สำคัญในชั้นการอักเสบได้แก่ อินเตอร์ลูคิน 1β[6] การสูญเสียยูริเคสซึ่งย่อยสลายกรดยูริกทีละน้อยในมนุษย์และไพรเมตชั้นสูงต่าง ๆ ทำให้ภาวะนี้กลายเป็นเรื่องที่พบบ่อย[6]
สารที่มากระตุ้นการตกตะกอนของกรดยูริกนั้นไม่เป็นที่ทราบแน่ชัด แม้ว่ากรดยูริกจะสามารถตกผลึกได้เมื่อปริมาณของมันอยู่ในระดับปกติ แต่ก็มีแนวโน้มที่จะตกผลึกมากขึ้นเมื่อปริมาณเพิ่มขึ้น[4][20] ปัจจัยอื่น ๆ ที่เชื่อว่ามีความสำคัญในการกระตุ้นการอักเสบเฉียบพลันของอาการข้ออักเสบได้แก่อุณหภูมิที่เย็น การเปลี่ยนแปลงอย่างรวดเร็วของระดับกรดยูริก ภาวะกรด[21][22] ความชุ่มชื้นของข้อต่อ และ โปรตีนเคลือบเซลล์ เช่น โปรตีโอไกลแคน คอลลาเจน และ คอนดรอยตินซัลเฟต[6] การตกตะกอนที่เพิ่มขึ้นที่อุณหภูมิต่ำอธิบายได้ส่วนหนึ่งว่าเหตุใดข้อต่อบริเวณเท้าจึงได้รับผลกระทบมากที่สุด[2] การเปลี่ยนแปลงอย่างรวดเร็วของปริมาณกรดยูริกอาจเกิดขึ้นเนื่องจากหลายปัจจัย ไม่ว่าจะเป็นการบาดเจ็บ การผ่าตัด เคมีบำบัด ยาขับปัสสาวะ และ การหยุดหรือการเริ่มใช้อัลโลพูรินอล[1] ในขณะเดียวกัน แคลเซียมแชนแนลบล็อกเกอร์ และ โลซาร์แทน ถูกเชื่อมโยงกับการลดความเสี่ยงจากโรคเกาต์เมื่อเทียบกับยาอื่น ๆ สำหรับโรคความดันโลหิตสูง [23]


โรคเกาต์อาจจะได้รับการวินิจฉัยและรับการรักษาโดยไม่ต้องสืบหาสาเหตุต่อไปในผู้ป่วยที่มีภาวะกรดยูริกในเลือดสูงและเป็นโรคโพดากราทั่วไปอยู่แล้ว อย่างไรก็ตาม ควรจะทำการวิเคราะห์น้ำไขข้อหากไม่แน่ใจในการวินิจฉัย[1] รังสีเอกซ์นั้นแม้ว่าจะมีประโยชน์ในการระบุโรคเกาต์เรื้อรังแต่ก็ใช้ได้เพียงเล็กน้อยกับการกำเริบเฉียบพลัน[6]
การวินิจฉัยโรคเกาต์ให้ได้แน่นอนขึ้นอยู่กับการระบุผลึกของเกลือโมโนโซเดียมยูเรทในน้ำไขข้อหรือก้อนโทไฟ[3] ทุกตัวอย่างน้ำไขข้อที่ได้รับจากข้อต่ออักเสบที่ยังไม่ได้รับการวินิจฉัยควรได้รับการตรวจสอบหาผลึกเหล่านี้[6] ภายใต้กล้องจุลทรรศน์แสงโพลาไรซ์ ผลึกเหล่านี้มีรูปร่างเหมือนเข็ม มีความแข็งแรงและมีค่าไบรีฟริงเจนซ์เป็นลบ การทดสอบนี้ทำได้ยากและมักจะต้องใช้ผู้สังเกตการณ์ที่ผ่านการฝึกอบรม[24] นอกจากนี้ ของเหลวยังต้องได้รับการตรวจสอบอย่างรวดเร็วหลังจากการเจาะ เพราะอุณหภูมิและค่าพีเอชมีผลต่อการละลายของผลึก[6]
ภาวะกรดยูริกในเลือดสูงเป็นลักษณะพื้นฐานของโรคเกาต์ แต่โรคเกาต์เกือบครึ่งหนึ่งของทั้งหมดเกิดได้โดยไม่ต้องมีภาวะนี้ และคนส่วนใหญ่ที่มีระดับกรดยูริกสูงไม่เคยเป็นโรคเกาต์[3][25] ดังนั้น ประโยชน์ของการวินิจฉัยโดยการวัดระดับกรดยูริกจึงถูกจำกัด[3] ภาวะกรดยูริกในเลือดสูง หมายถึง การมีระดับของกรดยูริกในพลาสมาสูงกว่า 420 μmol/l (7.0 mg/dl)ในเพศชาย และสูงกว่า 360 μmol/l (6.0 mg/dl)ในเพศหญิง[26] การตรวจเลือดอื่น ๆ ที่ดำเนินการกันทั่วไปได้แก่ การตรวจนับเม็ดเลือดขาว อิเล็กโทรไลต์ การตรวจการทำงานของไต และ การตรวจอัตราการตกตะกอนของเม็ดเลือดแดง (ESR) อย่างไรก็ตาม ทั้งอัตราเซลล์เม็ดเลือดขาวและ ESR อาจจะสูงเนื่องจากโรคเกาต์ในกรณีที่ไม่มีการติดเชื้อ[27][28] เคยมีการบันทึกจำนวนเซลล์เม็ดเลือดขาวที่นับได้สูงถึง 40.0×109/l (40,000/mm3)[1]
การวินิจฉัยแยกโรคที่สำคัญที่สุดของโรคเกาต์คือโรคไขข้ออักเสบจากการติดเชื้อ[3][6]ซึ่งควรได้รับการพิจารณาในผู้ที่มีอาการของการติดเชื้อหรือผู้ที่อาการไม่ดีขึ้นหลังได้รับการรักษา[3] เทคนิคที่ช่วยในการวินิจฉัยโรครวมถึงการย้อมแกรมและการปลูกน้ำไขข้อ[3] ภาวะอื่น ๆ ที่มีลักษณะคล้ายคลึงกันรวมถึงโรคเกาต์เทียมและโรคข้ออักเสบรูมาตอยด์[3] ก้อนโทไฟจากโรคเกาต์ โดยเฉพาะอย่างยิ่งเมื่อไม่ได้อยู่ในข้อต่อสามารถทำให้สับสนกับโรคมะเร็งผิวหนัง[29] หรือ เนื้องอกอื่น ๆ[30]
ทั้งการเปลี่ยนแปลงวิถีชีวิตและการรักษาทางยาสามารถลดระดับของกรดยูริกได้ การเลือกพฤติกรรมการบริโภคอาหารและการดำเนินชีวิตที่มีประสิทธิภาพรวมถึงการลดการบริโภคอาหารจำพวกเนื้อและอาหารทะเล การบริโภควิตามินซีอย่างเพียงพอ การจำกัดการบริโภคแอลกอฮอล์และฟรักโทสตลอดจนการหลีกเลี่ยงโรคอ้วน[2] พฤติกรรมการบริโภคอาหารที่มีแคลอรี่ต่ำในผู้ชายที่เป็นโรคอ้วนสามารถลดระดับกรดยูริกได้ถึง 100 µmol/l (1.7 mg/dl)[18] การบริโภควิตามิน ซีในปริมาณ 1,500 mg ต่อวันลดความเสี่ยงของโรคเกาต์ได้ถึง 45%[31] การบริโภคกาแฟ (แต่ไม่รวมชา) ช่วยลดความเสี่ยงของโรคเกาต์[32] โรคเกาต์อาจเป็นอาการข้างเคียงของภาวะหยุดหายใจขณะหลับเนื่องจากการปล่อยสารพิวรีนของเซลล์ที่ขาดแคลนออกซิเจน การรักษาภาวะหยุดหายใจสามารถช่วยลดการกำเริบของโรคเกาต์ได้[33]
จุดมุ่งหมายเบื้องต้นของการรักษาคือการระงับอาการกำเริบแบบเฉียบพลัน[34] การกำเริบซ้ำ ๆ สามารถป้องกันได้โดยยาชนิดต่าง ๆ ที่ใช้เพื่อลดระดับของกรดยูริก[34] การประคบน้ำแข็งเป็นเวลา 20 ถึง 30 นาทีวันละหลาย ๆ ครั้งจะช่วยลดความเจ็บปวด[2][35] ทางเลือกสำหรับการรักษาแบบเฉียบพลันได้แก่ยาแก้อักเสบชนิดไม่ใช่สเตอรอยด์ (NSAIDs) โคลชิซีน และ สเตอรอยด์[2] ส่วนทางเลือกสำหรับการป้องกันได้แก่อัลโลพูรินอล ฟีบัคโซสตัต และ โพรเบเนซิด การลดระดับกรดยูริกสามารถรักษาโรคนี้ให้หายได้[6] นอกจากนี้ การรักษาแบบการวินิจฉัยร่วมก็มีความสำคัญ[6]
ยาแก้อักเสบชนิดไม่ใช่สเตอรอยด์ หรือ NSAIDs เป็นการรักษาขั้นพื้นฐานสำหรับโรคเกาต์และไม่มีสารตัวใดโดยเฉพาะที่มีประสิทธิภาพมากหรือน้อยกว่าตัวอื่น ๆ อย่างเห็นได้ชัด[2] ยาเหล่านี้อาจช่วยให้อาการดีขึ้นภายในสี่ชั่วโมงและมักได้รับการแนะนำให้ใช้เป็นเวลาหนึ่งถึงสองสัปดาห์[2][6] อย่างไรก็ตาม ตัวยาเหล่านี้ไม่เป็นที่แนะนำสำหรับผู้ที่มีปัญหาสุขภาพอื่น ๆ บางอย่าง เช่น ภาวะเลือดออกในทางเดินอาหาร ไตวาย หรือ ภาวะหัวใจล้มเหลว[36] แม้ว่าอินโดเมตทาซินจะเป็น NSAID ที่ใช้กันมากที่สุดมาเป็นเวลานาน ทางเลือกอื่น เช่น ไอบูโปรเฟน อาจเป็นที่ชื่นชอบมากกว่าเนื่องจากประวัติด้านผลข้างเคียงน้อยกว่าแม้ว่าจะไม่ได้มีประสิทธิภาพเหนือกว่า[18] สำหรับผู้ที่มีความเสี่ยงจากผลข้างเคียงจาก NSAIDs ในกระเพาะอาหาร อาจมีการให้ยายับยั้งการหลั่งกรดเพิ่มเติม[37]
โคลชิซีนเป็นอีกทางเลือกหนึ่งสำหรับผู้ที่ไม่สามารถใช้ NSAIDs ได้[2] ผลข้างเคียงของยานี้ (ส่วนใหญ่เป็นความแปรปรวนในระบบทางเดินอาหาร) เป็นตัวจำกัดการใช้งาน[38] อย่างไรก็ตาม ความแปรปรวนในระบบทางเดินอาหารจะขึ้นอยู่กับปริมาณของยาที่ใช้ เราจึงสามารถลดความเสี่ยงได้โดยการลดปริมาณยาลงโดยยังคงให้มีประสิทธิภาพเพียงพอ[18] โคลชิซีนอาจเกิดปฏิกิริยากับยาที่แพทย์มักสั่งอื่น ๆ เช่น อะโทวาสแตติน อีริโทรมัยซิน และอื่น ๆ[38]
จากการวิจัยพบว่ากลูโคคอร์ติคอยด์มีประสิทธิภาพพอ ๆ กับ NSAIDs[39] และสามารถใช้ในกรณีที่ NSAIDs ถูกห้ามใช้[2] นอกจากนี้ ยานี้ยังทำให้อาการดีขึ้นเมื่อฉีดเข้าไปในข้อต่อ; อย่างไรก็ตามไม่ควรใช้ยานี้ในกรณีที่มีการติดเชื้อที่ข้อต่อเพราะสเตอรอยด์จะทำให้อาการแย่ลง[2]
เพลโกลติเคส (Krystexxa) ได้รับการอนุมัติในประเทศสหรัฐอเมริกาให้ใช้รักษาโรคเกาต์ในปีค.ศ. 2010 (พ.ศ. 2553) [40] ยานี้เป็นทางเลือกสำหรับ 3% ของผู้ป่วยที่ไม่สามารถต้านยาอื่น ๆ ได้[40] เพลโกลติเคสเป็นยาที่ใช้ฉีดเข้าเส้นเลือดดำทุกสองสัปดาห์[40]และได้รับการค้นพบว่าช่วยลดระดับกรดยูริกในผู้ป่วยกลุ่มนี้[41]
มียาหลายชนิดที่มีประโยชน์ต่อการป้องกันการกำเริบครั้งต่อไปของโรคเกาต์ ไม่ว่าจะเป็นตัวยับยั้งแซนทีนออกซิเดส (จำพวกอัลโลพูรินอลและ ฟีบัคโซสตัต) และ ยาเร่งการขับกรดยูริกออกทางไต (จำพวกโพรเบเนซิดและซัลฟินพัยราโซน) ยาเหล่านี้มักไม่เริ่มใช้จนกว่าเวลาจะผ่านไปหนึ่งถึงสองสัปดาห์หลังจากอาการกำเริบเฉียบพลันหายไป เนื่องจากความกังวลทางทฤษฎีว่าอาจทำให้อาการกำเริบหนักขึ้น[2] ยาเหล่านี้มักใช้ร่วมกันกับ NSAIDs หรือโคลชิซีนในช่วงสามถึงหกเดือนแรก[6] ไม่แนะนำให้ใช้จนกว่าจะมีการกำเริบของโรคเกาต์สองครั้ง[2] ยกเว้นในกรณีที่มีการเปลี่ยนแปลงของข้อต่อ ก้อนโทไฟ หรือ โรคไตจากกรดยูริกที่อาจเป็นอันตราย[5] เพราะพบว่ายาเหล่านี้ยังมีประสิทธิภาพไม่คุ้มราคาในปัจจุบัน[2] ควรเพิ่มมาตรการลดกรดยูริกจนกว่าระดับของกรดยูริกจะลดต่ำกว่า 300–360 µmol/l (5.0-6.0 mg/dl) และลดลงเรื่อย ๆ แบบไม่จำกัด[2][6] หากมีการใช้ยาเหล่านี้อย่างต่อเนื่องเมื่ออาการกำเริบ ขอแนะนำให้หยุดใช้[3] หากไม่สามารถลดระดับของกรดยูริกลงมาให้ต่ำกว่า 6.0 mg/dl และมีการกำเริบเกิดขึ้นให้ถือว่าเป็นความล้มเหลวของการรักษาหรือโรคเกาต์ดื้อยา[42] โดยรวมแล้ว โพรเบเนซิดดูเหมือนจะมีประสิทธิภาพน้อยกว่าอัลโลพูรินอล[2]
ยาเร่งการขับกรดยูริกออกทางไต เป็นการรักษาที่ได้รับความนิยมเมื่อมีการหลั่งกรดยูริกน้อยเกินไป เช่น ตามที่แสดงในผลการตรวจปัสสาวะในช่วงเวลา 24 ชั่วโมงที่พบปริมาณของกรดยูริกน้อยกว่า 800 mg[43] อย่างไรก็ตาม ยานี้ไม่แนะนำในผู้ป่วยที่มีประวัติเป็นโรคนิ่วในไต[43] หากพบว่ามีการขับถ่ายกรดยูริกทางปัสสาวะในเวลา 24 ชั่วโมงมากกว่า 800 mg ซึ่งบ่งชี้การผลิตมากเกินไป การใช้ตัวยับยั้งแซนทีนออกซิเดสจะได้รับความนิยมมากกว่า[43]
ตัวยับยั้งแซนทีนออกซิเดส (จำพวกอัลโลพูรินอลและ ฟีบัคโซสตัต) ยับยั้งการผลิตกรดยูริก การรักษาในระยะยาวมีความปลอดภัย ผู้ป่วยมักต้านทานยาได้ดีและสามารถนำมาใช้ในผู้ที่เป็นโรคไตหรือนิ่วเกลือยูเรทได้ แม้ว่อัลโลพูรินอลมีประวัติก่อโรคภูมิแพ้ในผู้ป่วยจำนวนหนึ่ง[2] ในกรณีเช่นนี้ ยาทางเลือกฟีบัคโซสตัตได้รับการแนะนำ[44]
หากไม่ได้รับการรักษา อาการกำเริบเฉียบพลันของโรคเกาต์มักจะหายไปเองภายในห้าถึงเจ็ดวัน อย่างไรก็ตาม 60% ของผู้ป่วยเหล่านี้มีอาการกำเริบอีกครั้งภายในหนึ่งปี[1] ผู้ป่วยโรคเกาต์มีความเสี่ยงที่เพิ่มขึ้นของโรคความดันโลหิตสูง โรคเบาหวาน กลุ่มอาการเมตาบอลิก โรคไต และ โรคระบบหัวใจและหลอดเลือด จึงมีความเสี่ยงที่เพิ่มขึ้นของการเสียชีวิต[6][45]ส่วนหนึ่งอาจเป็นเพราะความเกี่ยวข้องกับภาวะดื้อต่ออินซูลินและโรคอ้วน แต่ความเสี่ยงที่เพิ่มขึ้นมาบางอย่างก็ปรากฏว่าเกิดขึ้นเอง[45]
หากไม่ได้รับการรักษา การกำเริบของโรคเกาต์แบบเฉียบพลันอาจพัฒนาเป็นโรคเกาต์เรื้อรังที่มีการทำลายพื้นผิวข้อต่อ รูปร่างข้อต่อผิดปกติ และ ก้อนโทไฟที่ไม่สร้างความเจ็บปวด[6] ก้อนโทไฟเหล่านี้เกิดขึ้นใน 30% ของผู้ที่ไม่ได้รับการรักษาเป็นเวลาห้าปี โดยส่วนมากเกิดที่วงใบหู เหนือปุ่มปลายศอก หรือบนเอ็นร้อยหวาย[6] ซึ่งหากใช้การรักษาที่รุนแรงก็อาจทำให้สลายไปได้ นอกจากนี้ โรคนิ่วในไตก็มักก่อความซับซ้อนแก่ผู้ป่วยโรคเกาต์โดยมีผลกระทบต่อระหว่าง 10 ถึง 40% ของผู้ป่วย อาการนี้เกิดจากค่าพีเอชปัสสาวะต่ำซึ่งส่งเสริมการตกตะกอนของกรดยูริก[6] รูปแบบอื่น ๆ ของความผิดปกติเรื้อรังของการทำงานของไตอาจเกิดขึ้นได้[6]
โรคเกาต์เกิดกับประมาณ 1-2% ของประชากรชาวตะวันตก ณ ช่วงใดช่วงหนึ่งของชีวิตและกำลังพบมากขึ้นเรื่อย ๆ[2][6] อัตราการเกิดโรคเกาต์ได้เพิ่มขึ้นประมาณสองเท่าระหว่างปีค.ศ. 1990 และ 2010 (พ.ศ. 2533-2553) [4] การเพิ่มขึ้นนี้เชื่อว่าเกิดจากอายุขัยที่เพิ่มขึ้น การเปลี่ยนแปลงพฤติกรรมการบริโภคอาหาร และ การเพิ่มขึ้นของโรคที่เกี่ยวข้องกับโรคเกาต์ เช่น กลุ่มอาการเมตาบอลิกและภาวะความดันโลหิตสูง[10] มีหลายปัจจัยที่พบว่ามีอิทธิพลต่ออัตราการเกิดโรคเกาต์ ไม่ว่าจะเป็นอายุ เชื้อชาติ และฤดูกาล ในผู้ชายที่มีอายุเกินกว่า 30 และผู้หญิงที่มีอายุเกินกว่า 50 อัตราการเกิดอยู่ที่ 2%[36]
ในประเทศสหรัฐอเมริกา โรคเกาต์มีแนวโน้มการเกิดในชายชาวอเมริกันเชื้อชาติอาฟริกันมากกว่าชายอเมริกันเชื้อชาติยุโรปถึงสองเท่า[46] มีอัตราการเกิดสูงในประชาชนของหมู่เกาะแปซิฟิกและชาวมาวรีในประเทศนิวซีแลนด์ แต่ไม่ค่อยพบในชาวพื้นเมืองออสเตรเลียแม้ว่ากลุ่มหลังจะมีความเข้มข้นของกรดยูริกในเลือดโดยเฉลี่ยสูงกว่า[47] ต่อมามีการพบมากในประเทศจีน โพลีนีเซียและประเทศในอาฟริกาแถบทะเลทรายซาฮารา[6] การวิจัยบางส่วนพบว่าโรคเกาต์มีการกำเริบบ่อยในฤดูใบไม้ผลิ โดยสันนิษฐานว่าเกิดจากการเปลี่ยนแปลงพฤติกรรมการบริโภคอาหารตามฤดูกาล การบริโภคเครื่องดื่มแอลกอฮอล์ กิจกรรมทางกายภาพ และ อุณหภูมิ[48]

คำว่า "เกาต์" ถูกใช้ครั้งแรกโดยแรนดอลฟัส แห่ง บ็อกกิง เมื่อประมาณปีค.ศ. 1200 (พ.ศ. 1743) คำนี้รับมาจากคำในภาษาลาติน gutta แปลว่า "หยด" (ของเหลว)[49] ตามพจนานุกรมภาษาอังกฤษฉบับออกซฟอร์ด (Oxford English Dictionary) คำนี้มาจากธาตุ และ "แนวคิดของ 'การหยด' ของสิ่งแปลกปลอมจากเลือดในข้อต่อและบริเวณรอบ ๆ"[50]
อย่างไรก็ตาม โรคเกาต์เป็นที่รู้จักกันมาตั้งแต่สมัยโบราณ ในอดีตจะถูกเรียกว่า "ราชาของโรคและโรคของราชา"[6][51] หรือ "โรคของคนรวย"[52] หลักฐานชิ้นแรกเกี่ยวกับโรคนี้มาจากประเทศอียิปต์เมื่อ 2,600 ปีก่อนคริสตกาล ในคำอธิบายของโรคข้ออักเสบของนิ้วหัวแม่เท้า แพทย์ชาวกรีกชื่อฮิปพอคราทีสได้ให้ความคิดเห็นเมื่อประมาณ 400 ปีก่อนคริสตกาลในแง่คิด ของเขาโดยตั้งข้อสังเกตว่าโรคเกาต์จะไม่เกิดกับขันทีและสตรีวัยเจริญพันธุ์[49][53] ออร์ลุส คอร์เนลุส เคลซุส (ค.ศ. 30) อธิบายความเกี่ยวข้องกับเครื่องดื่มแอลกอฮอล์ การเริ่มตรวจพบในเพศหญิง และ ปัญหาไตที่เกี่ยวข้อง:
นอกจากนี้ ปัสสาวะข้นที่ตกตะกอนสีขาวแสดงให้เห็นว่าความเจ็บปวดและโรคต้องได้รับการรักษาบริเวณข้อต่อหรืออวัยวะภายใน... ปัญหาข้อต่อมือและเท้าเกิดขึ้นบ่อยมากและกินเวลานานเช่นที่เกิดขึ้นในกรณีของโพดากราและเชอิรากรา อาการเหล่านี้แทบจะไม่เกิดขึ้นกับขันทีหรือเด็กผู้ชายก่อนการมีเพศสัมพันธ์กับผู้หญิงและไม่เกิดกับผู้หญิงยกเว้นผู้ที่อยู่ในวัยหมดประจำเดือน... บางคนมีภูมิคุ้มกันตลอดชีวิตโดยการละเว้นจากไวน์ สุราและ การมีเพศสัมพันธ์[54]
ในปีค.ศ. 1683 (พ.ศ. 2226) โทมัส ซิดเดนแฮม แพทย์ชาวอังกฤษ ได้อธิบายการกำเริบของโรคเกาต์ในช่วงเช้ามืดและการที่เพศชายที่มีอายุมากมักพบปัญหามากกว่า:
ผู้ป่วยที่เป็นโรคเกาต์โดยทั่วไปจะเป็นชายชรา หรือ ชายที่บั่นทอนสุขภาพของตนในวัยเยาว์จนกระทั่งนำมาซึ่งความชราก่อนวัยอันควร ในบรรดาพฤติกรรมเสเพลต่าง ๆ ไม่มีสิ่งใดที่พบบ่อยไปกว่าความหลงระเริงก่อนวัยอันควรและมากเกินไปในกามารมย์ และ ความชอบที่สร้างความเหน็ดเหนื่อยในทำนองเดียวกัน ผู้ป่วยสามารถเข้านอนและหลับเหมือนมีสุขภาพดี ก่อนที่จะถูกปลุกให้ตื่นประมาณตีสองด้วยอาการปวดอย่างรุนแรงที่นิ้วหัวแม่เท้า; บางครั้งที่ส้นเท้า ข้อเท้า หรือ หลังเท้า ความเจ็บปวดเหมือนกับว่าอวัยวะเหล่านั้นเคลื่อน นอกจากนี้บางส่วนยังรู้สึกเหมือนกับถูกราดด้วยน้ำเย็น จากนั้นตามด้วยอาการหนาวสั่น ตัวสั่นและมีไข้เล็กน้อย... ค่ำคืนผ่านไปด้วยความทรมาน การนอนไม่หลับ การพลิกอวัยวะส่วนที่เจ็บและการเปลี่ยนท่านอนตลอดเวลา; ตัวโยนไปมาไม่หยุดหย่อนเพราะความเจ็บปวดของข้อต่อที่ได้รับความทรมาน และยิ่งเลวร้ายเมื่ออาการต่าง ๆ เกิดขึ้นพร้อมกัน[55]
นักวิทยาศาสตร์ชาวเนเธอร์แลนด์ อังตวน แวน เลเวนฮุค ได้อธิบายลักษณะโมเลกุลของผลึกเกลือยูเรทเป็นครั้งแรกในปีค.ศ. 1679 (พ.ศ. 2222)[49] ต่อมาในปีค.ศ. 1848 (พ.ศ. 2391) แพทย์ชาวอังกฤษ อัลเฟรด แบริง แกร์รอด ได้ค้นพบว่ากรดยูริกส่วนเกินในเลือดเป็นสาเหตุของโรคเกาต์[56]
โรคเกาต์ไม่ค่อยเกิดในสัตว์อื่น ๆ สาเหตุส่วนใหญ่เนื่องจากพวกมันสามารถผลิตยูริเคสซึ่งย่อยสลายกรดยูริกได้เอง[57] มนุษย์และวงศ์ลิงใหญ่อื่น ๆ ไม่มีความสามารถนี้ จึงประสบปัญหาโรคเกาต์ได้บ่อย[1][57] อย่างไรก็ตาม เชื่อกันว่าตัวอย่างไทแรนโนซอรัส ที่รู้จักกันดีในชื่อของ "ซู" เคยมีอาการโรคเกาต์[58]
ปัจจุบันมีการศึกษาวิจัยยาใหม่หลายชนิดสำหรับรักษาโรคเกาต์ไม่ว่าจะเป็น อนาคินรา คานาคินูมับ และริโลนาเซ็ปต์[59] การตัดต่อเอนไซม์ยูริเคส (ราสบูริเคส) สามารถใช้ได้; แต่การใช้นั้นถูกจำกัด เพราะอาจก่อให้เกิดภาวะภูมิต้านตนเองได้ รุ่นที่กระตุ้นการสร้างภูมิคุ้มกันน้อยกว่ากำลังได้รับการพัฒนา[1]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.