Loading AI tools
Från Wikipedia, den fria encyklopedin
Propranolol är en antihypertensiv medicin som agerar på kroppens noradrenerga system. Den minskar aktiviteten hos kroppens sympatiska nervsystem genom att blockera adrenerga beta-receptorer, vilket bland annat leder till sänkt blodtryck.
| Den här artikeln har källhänvisningar, men eftersom det saknas fotnoter är det svårt att avgöra vilken uppgift som är hämtad var. (2019-09) Hjälp gärna till med att redigera artikeln, eller diskutera saken på diskussionssidan. |
| Propranolol | |
 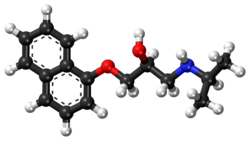 | |
| Systematiskt namn | 1-naftalen-1-yloxy-3-(propan-2-ylamino)propan-2-o |
|---|---|
| Kemisk formel | C16H21NO2 |
| Molmassa | 259.34 g/mol |
| CAS-nummer | 525-66-6 |
| SMILES | CC(NCC(O)COC1=C(C=CC=C2)C2=CC=C1)C |
| Egenskaper | |
| Löslighet (vatten) | 0.0617 (25 °C) g/l |
| Smältpunkt | 96 °C |
| Faror | |
| LD50 | 565 mg/kg |
| SI-enheter & STP används om ej annat angivits | |
Propranolol skrivs framförallt ut för att behandla sjukdomar i kardiovaskulära systemet, till exempel hjärtinfarkt, högt blodtryck, angina pectoris, men även för giftstruma, migrän, tumörer i binjuremärgen och tremor. Den har även använts experimentellt mot posttraumatiskt stressyndrom, där den verkar minska symptomen på tillståndet.
Eftersom betablockerare sänker blodsockret, kan propranolol ge hypoglykemi. Det kan också förvärra obstruktiva lungsjukdomar och sänka pH-värdet i blodet. Ökad drömaktivitet och mardrömmar förekommer vid behandling med propranolol. Dess påverkan på blodkärlen kan leda till vita fingrar. Agranulocytos är en allvarlig biverkning som kan uppkomma.


Propranolol används för att behandla olika medicinska tillstånd, såsom:
Tidigare var propanolol en av de bästa behandlingar för hypertoni. Eftersom de inte kunde ge lika bra effekt som andra mediciner, särskilt bland de äldre, blev beta-blockeraren nedgraderad till fjärde-klass i juni 2006 i Storbritannien. Fler och fler bevis hos de mest frekvent använda beta-blockerare vid normal dosering har även påvisat att öka risken för Typ 2-diabetes.[1]
Propranolol används ibland till för att behandla scenskräck. Dock finns inte lika bra bevis på att behandla andra ångeststörningar.[2] De utförda experiment i andra psykiatriska områden: [3]
Propranolol framställs ur 1-naftol och epiklorhydrin. I första steget öppnas epoxid-ringen upp av nukleofil-attack från OH-gruppen i 1-naftol, samtidigt sker 2 stegs protonöverföring. Vätet som sitter på -OH hamnar nu på epoxidsyret. I det andra steget sker en SN2-reaktion, i det här fallet, en nukleofil substitution av isopropylamin på det kolet som binder till den hyfsat bra lämnande grupp -Cl. Därav bildas den önskade slutprodukten - propranolol.
Man kan även använda sig av en stark bas som NaOH i det undre steget. Den starka basen NaOH hjälper till att deprotonera vätet som är bunden till OH-gruppen i 1-naftol, samtidigt hjälper den till att stabilisera den bildande alkoxid. Den nya natrium-1-naftolat intermediat som har bildats är en bra nukleofil. På samma sätt kommer den att attackera kolet som binder till -Cl på epiklorhydrin och en ny mellanprodukt bildas. Därefter görs en nukleofil-attack av isopropylamin på det elektrofila kolet som sitter på epoxidsyret. Vilket resulterar i en ringöppning och syret protoneras till en alkohol, därav fås slutprodukten - propranolol.
Propranolol är en racematisk blandning – det vill säga, två enantiomerer, R(+) och S(-). S(-)-enantiomeren är ungefär 100 gånger bättre än R(+)-enantiomeren på att blockera adrenerga beta-receptorer.
Syntesen ovan (1) visar ett generellt och billigt sätt att syntetisera propranolol. Men för att undvika racemat har forskare behövt hitta andra sätt. Som till exempel syntesen nedan (2) som är steoreoselektiv, vilket betyder att det mesta av produkten blir S(-)-propranolol. [8]
(I) K2CO3, CH2=CHCH2Br, acetone, reflux, 12 h; 97-99%; (II) cat-OsO4, (DHQD)2-PHAL, K3Fe(CN)6, K2CO3, t -BuOH:H2O, 0 °C, 12 h, 94-98%; 73-90% ee; (III) SOCl2, Et3N, CH2Cl2, 0 °C, 40 min.; 96-99%; (IV) cat. RuCl3.3H2O, NaIO4, CH3CN:H2O, 0 °C, 30 min., 94-98%; (V) LiBr, THF 25 °C, 2-3 h; (VI) 20% H2SO4, Et2O, 25 °C, 10 h; (VII) K2CO3, MeOH, 0 °C, 2 h, 80-85%; (VIII) iPr-NH2, H2O (cat.), reflux, 2 h, 99%.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.