
Nitrometan
From Wikipedia, the free encyclopedia
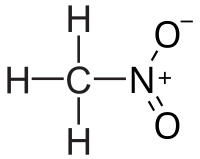
Nitrometan, eller CH3NO2, är en organisk molekyl. Det används bland annat som industriellt lösningsmedel och reaktant, men också som bränsle bland annat inom motorsport, till exempel dragracing. I detta sammanhang kallas nitrometan ofta bara för nitro.
Snabbfakta Systematiskt namn, Kemisk formel ...
| Nitrometan | |
  | |
| Systematiskt namn | Nitrometan |
|---|---|
| Kemisk formel | CH3NO2 |
| Molmassa | 61,04 g/mol |
| Utseende | Färglös vätska |
| CAS-nummer | 75-52-5 |
| SMILES | C[N+]([O-])=O |
| Egenskaper | |
| Densitet | 1,138 g/cm³ |
| Löslighet (vatten) | 100 g/l |
| Smältpunkt | -29 °C |
| Kokpunkt | 101,2 °C |
| Faror | |
| Huvudfara | |
| NFPA 704 | |
| LD50 | 940 |
| SI-enheter & STP används om ej annat angivits | |
Stäng
Snabbfakta Ångbildningsvärme, Smältvärme ...
| Fysikaliska data | |
| Ångbildningsvärme | 38,4 kJ/mol |
|---|---|
| Smältvärme | 9,71 kJ/mol |
| Kritisk temperatur | 315 °C |
| Kritiskt tryck | 6310 kPa |
| Förbränningsvärme | -711 kJ/mol |
Stäng
Eftersom nitrometan innehåller sitt 'eget' syre krävs mycket mindre syre för att uppnå full förbränning än vid förbränning av till exempel bensin:
Det krävs 14,6 kg luft för att förbränna 1 kg bensin, men bara 1,7 kg luft för att förbränna 1 kg nitrometan.
Nitrometan är explosivt vid kraftig upphettning.

