
Хидроксид
Класа једињења / From Wikipedia, the free encyclopedia
Хидроксиди су једињења типа која дисоцијацијом дају хидроксидне јоне.[3] Хидроксиди могу да буду базни или амфотерни.[4] Хидроксид је исто тако диатомски анјон са хемијском формулом −. Хидроксид се састоји од атома кисеоника и водоника које држи заједно ковалентна веза, и носи негативан електрични набој. Овај јон је важан, али обично незнатно застуљени састојак воде. Он функционише као база, лиганд, нуклеофил и катализатор. Хидроксидни јон формира соли, од којих неке дисоцирају у воденом раствору, ослобађајући солватиране хидроксидне јоне. Натријум хидроксид је хемијска супстанца која се производи у количинама од више милиона тона годишње. Хидроксид везан за снажно електропозитивни центар може и сам да се јонизује, ослобађајући водонични катјон (+), чинећи матично једињење киселином.
 | |
| Називи | |
|---|---|
| Системски IUPAC назив
Хидроксид | |
| Идентификација | |
3Д модел () |
|
| UNII | |
| Својства | |
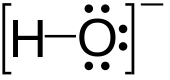
| OH− | |
| Моларна маса | 17,01 g·mol−1 |
| Конјугована киселина | Вода |
| Конјугована база | Оксидни анјон |
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°C [77°F], 100 kPa). | |
| Референце инфокутије | |
Кореспондирајуће електрично неутрално једињење HO• је хидроксилни радикал. Кореспондирајућа ковалентно везана група – атома је хидроксилна група. Хидроксидни јони и хидрокси група су нуклеофили и могу деловати као катализатори у органској хемији.
Многе неорганске материје које у свом називу носе реч „хидроксид” нису јонска једињења хидроксидног јона, већ ковалентна једињења која садрже хидрокси групе.