
Алфа распад
From Wikipedia, the free encyclopedia
Алфа распад је облик радиоактивног распада у којем се атомско језгро избацивањем алфа честице (атомског језгра хелијума) преобраћа у језгро са масеним бројем, , мањим за 4 јединице и наелектрисањем, мањим за 2 јединице. Распад може бити приказан следећом схемом: 




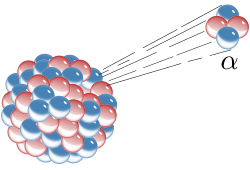
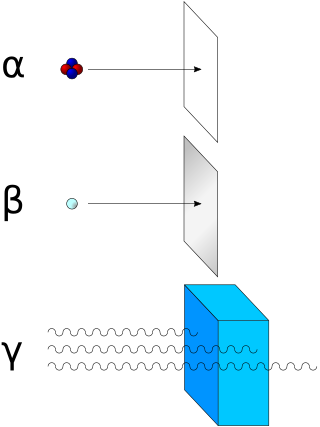



Алфа распад се у суштини може сматрати цепањем атомског језгра (нуклеарна фисија), где се језгро родитељ цепа на два потомка од којих је један хелијум. Алфа распад се одвија помоћу тунел ефекта. За разлику од бета распада, алфа распад се одвија под утицајем јаке силе. Алфа честице имају кинетичку енергију реда 5 (тј. ≈0,13% њихове тоталне енергије која износи 110 ) и брзину од 15.000 (што одговара брзини приближно 0,05c). Упркос томе, алфа честице се у ваздуху заустављају на путањи од неколико сантиметара. Због постојања алфа распада, скоро целокупна количина хелијума насталог на Земљи потиче из наслага минерала који садрже уранијум и торијум, а на површину излази као нуспроизвод у производњи природног (земног) гаса. Алфа распад честица је природан вид зрачења честица. Анализа је показала да је α-зрачење састављено од два протона и два неутрона (конфигурација хелијума). α-распад се јавља код елемената великог редног броја ( > 82). Настаје емисијом α-честица из језгра искључиво тунел ефектом. Енергије алфа честица имају дискретан спектар и тачно одређен спектар вредности енергија. Вредности енергија α-честица су реда величине неколико -а. Приликом емисије α-честице, језгро радиоактивног елемента (родитеља) је трансформисано у језгро другог елемента (потомка) чији је редни број мањи за два, а масени за четири.
До распада долази због нестабилности атомског језгра односно неуравнотеженог броја протона и неутрона у њему. Нека су атомска језгра природно нестабилна и распадају се у дужем или краћем временском интервалу (време полураспада), а нека стабилна атомска језгра могу постати нестабилна након што на њих делују честице велике енергије. Алфа распад се догађа најчешће код масивних језгара која имају превелик однос протона у односу на неутроне. Алфа честица с два протона и два неутрона је врло стабилна конфигурација нуклеона. Многа се језгра масивнија од олова (> 106 у или више од 106 атомских јединица масе) распадају овим распадом. Најмања атомска језгра која могу зрачити алфа-честице је телуријум (З = 52), који има атомску масу од 106 до 110. Код алфа распада атомска маса и редни бројеви језгра се мењају, што значи да атомско језгро која се распада и језгро настало тим распадом припадају различитим хемијским елементима, те стога, имају различита хемијска својства.[1]
Кад је однос неутрона и протона у атомском језгру одређених атома пренизак, они емитирају алфа-честицу како би успоставили равнотежу. На пример: полонијум-210 има 126 неутрона и 84 протона, што је однос од 1,50 према 1. Након радиоактивног распада емитовањем алфа честице, однос постаје 124 неутрона напрема 82 протона или 1,51 напрема 1. Будући да број протона у језгру одређује елемент, полонијум-210 након емисије алфа честице постаје олово-206 који је стабилан елемент.[2][3] Атоми који емитују алфа честице углавном су врло велики атоми, тј. имају високе атомске бројеве. Много је природних и вештачких радиоактивних елемената који емитују алфа честице. Природни извори алфа-честица имају атомски број најмање 82, уз неке изузетке. Најважнији алфа емитери су: америцијум-241 ( = 95), плутонијум-236 ( = 94), уранијум-238 ( = 92), торијум-232 ( = 90), радијум-226 ( = 88), радон-222 ( = 86). Алфа емитери су присутни у различитим количинама у готово свим стенама, тлу и води. Након емисије, алфа честице се због велике масе и електричног набоја крећу се релативно споро (отприлике 1/20 брзине светлости) и у ваздуху потроше сву енергију након неколико центиметара и тада вежу слободне електроне и постају хелијум.[4]