Изотоп водоника са 2 неутрона. From Wikipedia, the free encyclopedia
Трицијум (грч. »трећи«) је поред протијума и деутеријума природни изотоп водоника. Његово атомско језгро се понекад назива и тритон.[1][2]
 | |
| Опште | |
|---|---|
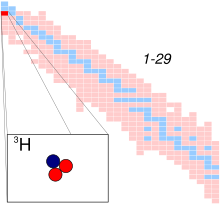
| Симбол | 3H |
| Име | трицијум, H-3, тритијум, тритон |
| Број протона | 1 |
| Број неутрона | 2 |
| Подаци о нуклидима | |
| Распрострањеност у природи | trace |
| Полураспад | 12.32 године |
| Продукти распада | 3He |
| Маса изотопа | 3.0160492 |
| Спин | 1⁄2 |
| Вишак енергије | 14,949.794± 0.001 |
| Eнергија везања | 8,481.821± 0.004 |
| Мод распада | |
| Мод распада | Енергија распада () |
| Бета распад | 0.018590 |
| Изотопи водоник Потпуна таблеа нуклида | |
Хемијски симбол трицијума је 3, а поједностављено се може обележити са T. У поређењу са деутеријумом, поред тога што има протон у атомском језгру, не поседује један, већ два неутрона. Међутим ово атомско језгро је нестабилно и распада се са једним временом полураспада од 12,32 година по емисији једног електрона у 3He (бета распад). Такође трицијум је радиоактиван.[3]
Иако изотопи истог хемијског елемента имају једнаке физичке и хемијске особине, код водоника се због значајне разлике у тежини атомског језгра појављују различите физичке особине између обичне, тешке и претешке воде. Трицијум оксид (претешка вода) има тачку кључања од 101,51 °C, а температуру топљења износи 4,48 °C.
Док трицијум има неколико различитих експериментално одређених вредности свог времена полураспада, Национални институт за стандарде и технологију наводи 4.500 ± 8 дана (12,32 ± 0,02 година).[4] Трицијум се распада у хелијум-3 путем бета распада према следећој нуклеарној реакцији:
и при томе се ослобађа 18,6 енергије. Електронска кинетичка енергија варира, са просеком од 5,7 , док преосталу енергију односи електронски антинеутрино који је скоро немогуће детектовати. Бета честице из трицијума могу да пенетрирају само око 6,0 дебео слој ваздуха, и оне немају способност пролаза кроз мртви спољашњи слој људске коже.[5] Необично ниска енергија ослобођена при бета распаду трицијума чини тај распад (заједно са ренијумом-187) подесним за мерења апсолутне масе неутрина у лабораторији (један од недавних експеримената је ).
Ниско енергетска трицијумска радијација отежава детектовање трицијумом обележених једињења изузев при примени ликвидног сцинтилационог бројања.
Природним путем трицијум настаје неутронским бомбардовањем језгара атома азота из космичког зрачења у горњим слојевима атмосфере.
Конвекционалним струјањима трицијум доспева до земљине површине као трицијумводоник. У читавој природи постоји можда око 2 – 3,5 kg трицијума. Вештачки трицијум се добија у језгро-реактору. Ово се одвија: бомбардовањем 6-мете са неутронима из реакторског језгра и екстракцијом из хладне воде из реактора тешке воде, гдје настаје као нус продукт.
Трицијум се производи у нуклеарним реакторима путем неутронске активације литијума-6. То се може остварити са неутронима било које енергије, и одвија се као егзотермна реакција којом се ослобађа 4,8 . У поређењу с тим фузија деутеријума и трицијума ослобађа око 17,6 енергије. За примену у предложеним реакторима на фузијску енергију, као што је , грумени који се састоје од литијумске керамике укључујући и , се развијају за трицијумско формирање у хелијумом хлађеним слојевима.
Неутрони високе енергије исто тако могу да произведу трицијум из литијума-7 у ендотермним реакцијама (уз нето конзумацију топлоте), при чему се троши 2,466 . То је откривено кад је Касл Браво нуклеарни тест из 1954. године произвео неочекивано велики принос.[6]
Озрачивање бора-10 високо енергетским неутронима исто тако може да доведе до формирања трицијума:[7]
Чешћи исход хватања неутрона у бору-10 је 7Li и једна алфа честица.[8]
Трицијум се исто тако производи у реакторима који су модулисани тешком водом у којима деутеријумска језгра хватају неутроне. При овој реакцији долази у веома малој мери до апсорпције, те је тешка вода добар модератор неутрона, и релативно мало трицијума се формира. Независно од тога, чишћење трицијума из модератора је пожељно након неколико година да би се смањио ризик од његовог испуштања у околину. Постројење за уклањање трицијума предузећа обрађује око 2500 тешке воде годишње, и при томе се издваја око 2,5 kg (5,5 lb) трицијума, који је доступан корисницима.[9]
Попречни пресек деутеријумске апсорпције термалних неутрона је око 0,52 милибарна, док је за кисеоник-16 (168O) око 0,19 милибарна, а за кисеоник-17 (178O) је око 240 милибарна.
Трицијум није уобичајени продукат нуклеарне фисије уранијума-235, плутонијума-239, и уранијума-233, при којима се формира око један атом на сваких 10.000 фисија.[1][10] Ослобађање или опоравак трицијума мора се разматрити при раду нуклеарних реактора, посебно при поновној обради нуклеарних горива и складиштењу потрошеног нуклеарног горива. Продукција трицијума није наменска, већ је нуспродукат. Неке нуклеарне електране испуштају трицијум у атмосферу у малим количинама.[11]
У јуну 2016. године Оперативна група за триционирану воду је објавила извештај[12] о статусу трицијума у триционираној води у нуклеарном реактору Фукушима Даичи, у оквиру разматрања за финално одлагање ове воде. Тим извештајем је идентификовано да је марта 2016. количина садржаног трицијума била 760 TBq (што је еквивалентно са 2,1 трицијума или 14 трициониране воде) укупно 860000 3 ускладиштене воде. Овај извештај је исто тако идентификовао редукујући концентрацију трицијума у води екстрахованој из објеката итд. за чување, што одговара десетоструком смањењу током разматраног петогодишњег периода (2011—2016), 3,3 до 0,3 (након корекције за годишње распадање трицијума).
Према извештају стручног панела који је разматрао најбољи приступ решавања овог проблема, „Трицијум би се теоријски могао раздвојити, али не постоји практична технологија одвајања у индустријским размерима. Сходно томе, сматра се да је контролисано испуштање у околину најбољи начин за третирање воде са ниском концентрацијом трицијума.”[13]
Трицијумски производ распадања хелијум-3 има веома велики попречни пресек у реакцији са термалним неутронима, при чему долази до избацивања протона, стога се он брзо конвертује назад у трицијум у нуклеарним реакторима.[14]
Између осталог користи се у биологији, хемији и медицини. Користи се као маркер (трејсер) за маркирање појединих супстанци.
Као средство за осветљавање користи се мешавина гасовитог Трицијума и флуоресцентног средства у запечаћеним боросиликат-ампулама. Трицијумово бета зрачење активира унутрашњи слој којим је премазана унутрашња страна ампуле и на тај начин производи слабо, флуоресцентно светло. Ово „хладно осветљење“ има теоретски животни век од више деценија, а на тржишту га је могуће наћи у више боја, под називом Трејсер ().
Трицијум се такође користи као средство за осветљавање, на пример на казаљкама сатова, на бројевима сатова. Код производње и складиштења већих количина трицијума, не смеју се искључити ризици по здравље.
Трицијум је такође саставни део појединог атомског оружја У будућим атомским електранама требало би да се користи мешавина деутеријума и трицијума као погонско гориво.
Доказивање постојања трицијума се врши помоћу течних цинтилатора и отворених јонизаторских комора.
Трицијум је први пут био произведен 1934. године из деутеријума, још једног изотопа водоника заслугом Ернеста Радерфорда, Марка Олифанта, и Пола Хартека.[15][16] Међутим, у њихоховом експерименту није било могуће да се изолује трицијум. То су касније остварили Луис Алварез и Роберт Корног, који су исто тако утврдили његову радиоактивност.[17][18] Вилард Либи је утврдио да трицијум може да се користи за радиометричко датирање воде и вина.[19]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.