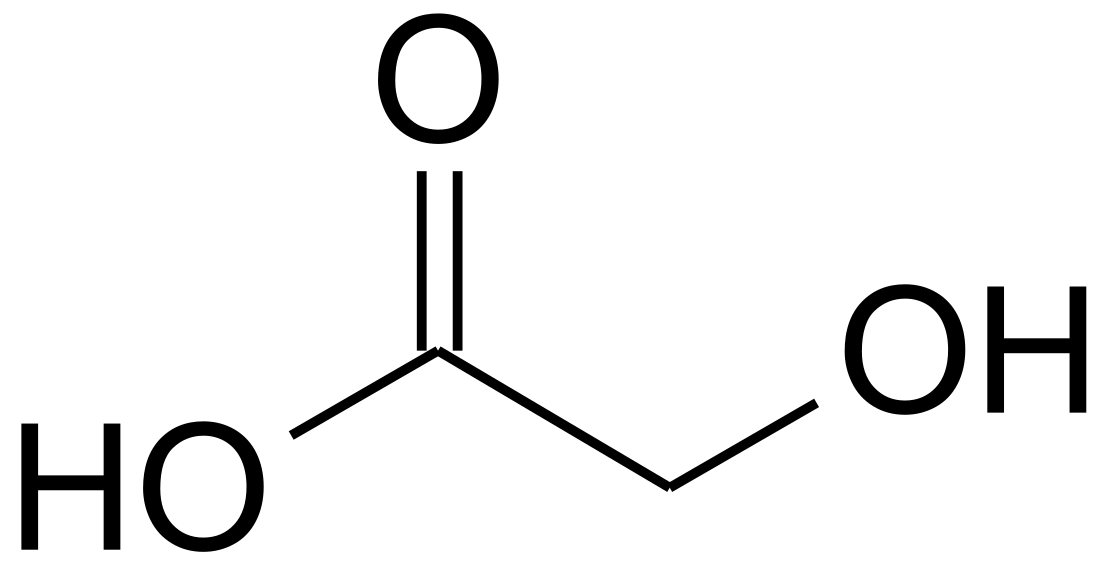
Glikolna kiselina
From Wikipedia, the free encyclopedia
Glikolna kiselina (ili hidroksisirćetna kiselina) je najmanja α-hidroksi kiselina (AHA). Ova bezbojna, bezmirisna, i higroskopna kristalna materija je visoko rastvorna u vodi. Ona se koristi u raznim produktima za kožu. Glikolna kiselina je prisutna u pojedinim šećernim usevima.
| |||
| Nazivi | |||
|---|---|---|---|
| naziv
| |||
| Drugi nazivi
Dikarbonska kiselina glikolinska kiselina, hidroksiacetatna kiselina | |||
| Identifikacija | |||
3D model () |
|||
| 100.001.073 | |||
| KEGG[1] | |||
| MC5250000 | |||
| UNII | |||
| Svojstva | |||
| Molarna masa | |||
| Agregatno stanje | beli prah | ||
| Gustina | |||
| Tačka topljenja | |||
| Tačka ključanja | |||
| 70% rastvor | |||
| Rastvorljivost u drugi rastvarači | alkoholi, aceton, sirćetna kiselina and etil acetat[2] | ||
| Kiselost (pKa) | 3,83 | ||
| Opasnosti | |||
| Opasnost u toku rada | Korozivna je (C) | ||
| R-oznake | R22-R34 | ||
| S-oznake | S26-S36/37/39-S45 | ||
| NFPA 704 | |||
| Tačka paljenja | 129 °[3] | ||
| Srodna jedinjenja | |||
Srodne α-hidroksi kiseline |
mlečna kiselina | ||
Srodna jedinjenja |
sirćetna kiselina, glicerol | ||
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 ° [77 °], 100 ). | |||
| verifikuj (šta je ?) | |||
| Reference infokutije | |||
Priprema
Postoji više načina za sintezu glikolne kiseline. Najveći deo svetske proizvodnje se formira putem katalizovane reakcije iz formaldehida (karbonilacijom formaldehida). To je posebno efektivan postupak pripreme.[4]
Ona se takođe priprema reakcijom hlorsirćetne kiseline sa natrijum hidroksidom čemu sledi reacidifikacija. Neto reakcija je:
Na ovaj način se proizvede nekoliko miliona kilograma godišnje.[5]
Glikolna kiselina se takođe može pripremiti koristeći enzimatski biohemijski proces kojim se formiraju manje količine nečistoća u poređenju sa tradicionalnim hemijskim sintezama, za koji su potrebne manje količine energije i koji proizvodi manje količine koprodukta.[6]
Bezbednost
Glikolna kiselina je jak iritant u zavisnosti od pH nivoa.[7] Poput etilen glikola, ona se metaboliše do oksalne kiseline, zbog čega može da bude štetna ako se proguta.
Reference
Spoljašnje veze
Wikiwand - on
Seamless Wikipedia browsing. On steroids.