From Wikipedia, the free encyclopedia
Натријум-тиосулфат је хемијско неорганско једињење хемијске формуле .
 | |
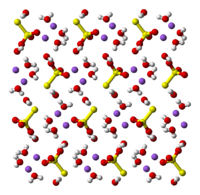 | |
| Називи | |
|---|---|
| назив
Натријум-тиосулфат | |
| Други називи
Натријум-хипосулфат (чест назив у фотографији) Хипосулфат соде | |
| Идентификација | |
| 100.028.970 | |
| Е-бројеви | E539 (регулатор киселости, ...) |
| MeSH | Sodium+thiosulfate |
| Својства | |
| Моларна маса | |
| Агрегатно стање | бели кристали |
| Густина | |
| Тачка топљења | 48.3 ° |
| Тачка кључања | Разлаже се |
| веома растворан | |
| Базност (pKb) | |
| Структура | |
| Геометрија молекула | тетраедар-анион |
| Опасности | |
| Није токсичан | |
| R-ознаке | R35 |
| S-ознаке | (S1/2) S26 S37/39 S45 |
| NFPA 704 | |
| Тачка паљења | Није запаљив |
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°C [77°F], 100 kPa). | |
| Референце инфокутије | |
У лабораторији се добија загревањем раствора натријум-сулфата са елементарним сумпором:
Уколико се ова реакција изводи са радиоактивним изотопом сумпора, па се онда делује киселином на добијени радиоактивни натријум-тиосулфат, сав елементарни сумпор који се добије ће бити радиоактиван, док сумпор-диоксид који се ослобађа то неће бити. Ово наводи на закључак да два сумпорова атома у натријум-тиосулфату нису еквивалентна.[1]
Некада су се веће количине ове соли добијале из калцијум-сулфида који би остајао као отпадак при Леблановом процесу. Након оксидације калцијум-сулфида на ваздуху, производ би се испирао са раствором натријум-карбоната, а потом се након испаравања вршила кристализација натријум-тиосулфата[1]:
У новије време се натријум-тиосулфат производи из течности које представљају отпатке при производњи натријум-сулфида. Таква течност садржи сулфид, сулфат, сулфит и карбонат. При концентровању, ове соли се таложе, да би се онда процедиле, раствориле у води и напокон се третирају гасовима из пећи који садрже сумпор-диоксид[1]:
Гради крупне кристале у облику пентахидрата који се у води лако растварају. При загревању се распада на натријум-сулфат и натријум-пентасулфид[1]:
Време настанка сумпора зависи од концентрације раствора. Ова реакција се користи за квалитативно доказивање тиосулфата.
Ова реакција се много примењује у волуметријској анализи, не само за одређивање јода, већ и ма којег оксидационог средства које ослобађа јод из јодида, што значи за одређивање хлора, брома, бакарних соли, хипохлорита и хлорног креча.[1]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.