
Стехиометрија
прорачун релативних количина реактаната и продуката у хемијским реакцијама / From Wikipedia, the free encyclopedia
Стехиометријски односи су квантитативни односи који следе из хемијских формула или хемијских једначина. У складу са тим сва израчунавања у вези са хемијским формулама или једначинама називају се стехиометријски односи (стехиометрија).[1] Стехиометрија је утемељена на закону одржања масе, где је укупна маса реагенаса једнака укупној маси производа. То значи да се односи између количине реагенаса и производа обично понашају као односи позитивних целих бројева. То истовремено говори да ако су познати износи одвојених реагенаса, онда се може израчунати и износ производа. Сагласно томе, ако је позната количина једног реагенса и количина производа, емпиријски се може одредити један од реагенаса, а затим се може израчунати и износ других реагенаса.[2][3][4][5]
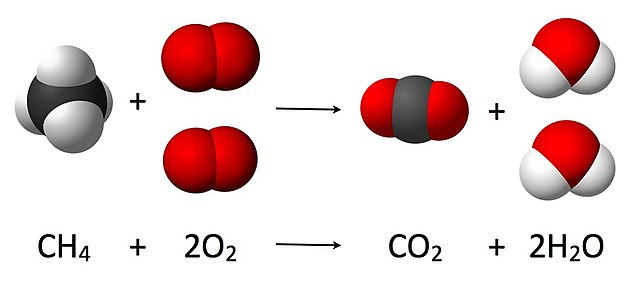
Ови односи се могу приказати уравнотеженом једначином:
- CH
4 + 2 O
2 → CO
2 + 2 H
2O.
Овде један молекул метана реагује са два молекула гасовитог кисеоника, па настају један молекул угљен диоксида и два молекула воде. Стехиометрија мери ове количинске односе, а користи се за одређивање количине производа/реагенаса који су производени/потребни у датој реакцији. Описани количински односи међу супстанцама у хемијској реакцији познати су као реакцијска стехиометрија. У горњем примеру, реакцијска стехиометрија мери однос између метана и кисеоника који у међусобној реакцији стварају угљен диоксид и воду.
Због познатог односа молске и атомске тежине, добијени стехиометријски коефицијенти могу се користити за одређивање тежине у реакцији која је описана у уравнотеженој једначини. То се зове композицијска стехиометрија.
Гасна стехиометрија бави се реакцијама које укључују гасове, а на основу познате температуре, притиска и запремине може се претпоставити да ли је дати узорак идеалан гас. За гасове, однос запремина је идеално исти као и онај по закону о идеалном гасу, али се однос масе једне реакције мора израчунати из молекулских маса реагенаса и производа. У пракси, због постојања изотопа, користе се моларне масе, уместо да се израчунава однос маса.