From Wikipedia, the free encyclopedia
U hemiji, boran je hemijsko jedinjenje bora i vodonika. Borani obuhvataju veliku grupu jedinjenja sa opštom formulom .[3][4] Ta jedinjenja se ne javljaju u prirodi. Mnogi borani se lako oksiduju u kontaktu sa vazduhom, neki burno. Osnovni član 3 se zove boran. On je poznat samo u gasovitom stanju. On se dimerizuje da formira diboran, . Veći borani se sastoje od klastera bora koji su poliedarski, neki od njih postoje kao izomeri. Na primer, izomeri su bazirani na fuziji dva desetoatomna klustera.
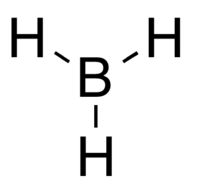 | |||
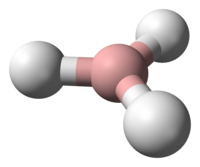 Model borana, 3, koji je visoko reaktivan. | |||
| |||
 3 formira dimeri diboran, . | |||
| Identifikacija | |||
|---|---|---|---|
3D model () |
|||
| Svojstva | |||
| Molarna masa | |||
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 ° [77 °], 100 ). | |||
| Reference infokutije | |||
Najvažniji borani su diboran , pentaboran , i dekaboran . Razvoj hemije bor hidrida je omogućio razvoj novih eksperimentalnih tehnika i teoretskih koncepta. Bor hidridi su studirani kao potencijalna goriva za raketa i za automobilsku primenu.
Tokom zadnjih nekoliko dekada, doseg hemije bor hidrida je porastao da obuhvati atome osom bora, kao što je ugljenik u karboranima i metali u metalboranima, gde je jedan ili više atoma bora zamenjen metalnim atomima.
Borani koje je koristio i pravio Alfred Štok imali su opstu formulu BnHn+4 i BnHn+6, ali danas su poznata i kompleksnija jedinjenja, kako neutralna tako i negativna (anjonska). Hidridi bora brojniji su od hidrida svih ostalih elemenata sem ugljenika. Najjednostavniji boran koji se može izolovati je B2H6, diboran(6). On se najviše koristi i istražuje. Komercijalno je dostupan, i dug niz godina borani i njihovi derivati sintetisani su upravo od njega, direktno ili indirektno. Slobodni molekuli BH3 (i B3H7) su veoma nestabilni, ali mogu biti izolovani kao stabilni produkti adicije sa Luisovim bazama, na primer BH3·N(CH3)3. Borani mogu biti u sva tri agregatna stanja, i njihove tačke topljenja i ključanja rastu sa relativnom atomskom masom i kompleksnošću.
| tačka topljenja (°C) | tačka ključanja (°C) | |
|---|---|---|
| B2H6, diboran(6) | -165 | -93 |
| B4H10, tetraboran(10) | -122 | 16 |
| B5H9, pentaboran(9) | -47 | 60 |
| B5H11, pentaboran(11) | -123 | 65 |
| B6H10, heksaboran(10) | -62 | 108 |
| B10H14, dekaboran(14) | 100 | 213 |
| Osobina | Vrednost |
|---|---|
| Particioni koeficijent[5] ( | 3,2 |
| Rastvorljivost[6] ()) | 1,4 |
| Polarna površina[7] (, Å2) | 0,0 |
Hidrate borana je prvi put sistematično sintetisao i okarakterisao između 1912. i 1937. godine Alfred Štok. Hidridi ugljenika (nalazi se do bora u PSE) su alkani (zasićeni ugljovodonici), pa je Štok analogno nazvao hidride bora boranima. Posto lakši borani burno reaguju, toksični su i osetljivi na vazduh i vlažnost, Štok je razvio metode i aparaturu za proučavanje borana koja je koristila vakuum. Americki rad na boranima počeli su 1931. godine Herman I. Slesinger i Anton B. Burg. Borani su bili samo u akademskim interesima sve do Drugog svetskog rata, kada je američka vlada podržala istraživanje da se nadju eksplozivna jedinjenja uranijuma zbog izdvajanja izotopa, i 1950-ih godina kada je američka vlada podržala programe da se pronadju visoko-energetska goriva za rakete i mlaznjake (borani i njihovi derivati imaju mnogo veće toplote sagorevanja od ugljovodonika). Vilijam Lipskomb Junior je 1976. godine dobio Nobelovu nagradu iz hemije za "njegova istraživanja strukture borana, osvetljujuci probleme hemijskih veza". Herbert Braun, njegov učenik, je 1979. godine delio Nobelovu nagradu za reakciju hidroborovanja (1956), veoma jednostavnu reakciju adicije BH3 nezasićenim organskim jedinjenjima (npr. alkeni i alkini) u etarskim rastvaracima na sobnoj temperaturi da bi nastali organoborani kvantitativno (visok prinos, skoro potpuna reakcija). Reakcija hidroboracije je otvorila nove perspektive u oblasti nekih organskih sinteza.[8].
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.