From Wikipedia, the free encyclopedia
Aktomiozin je aktinsko-miozinski kompleks koji se formira unutar citoskeleta. Aktomiozin je sam po sebi kontraktilni protein, s tim da se motorni protein miozina mogu povući na aktinske filamente. Ovo svojstvo omogućavaju kontraktilnost vlaknima koja je osnova funkcija skeletnih mišića, pa čak i u nemišićnim ćelijama, jer omogućava pokretljivost ćelija i stvaranje sile na subćelijskom nivou.

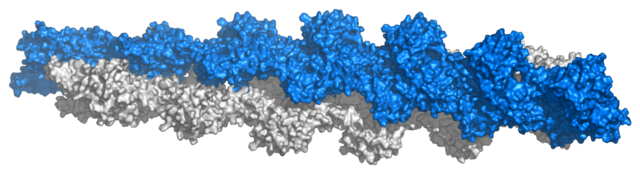
Aktin (filamentozni ili F-aktin) je polimer građen od dva proteinska lanca, koja se spiralno uvijaju jedan oko drugog. Ti lanci su izgrađeni od monomera (globularnog ili G-aktina), a na svakom monomeru se nalazi po jedno aktivno mesto za vezivanje miozina, što je značajno za proces mišićne kontrakcije. F-aktin čini okosnicu tankog filamenta.
Aktini čine filamentsku mrežu, kako unutar filopodija tako i kod lamelipodijaa. Oni su veoma dinamične strukture, čija karakteristika se najbolje uoćavaju u retrogradnom pokretu koji je svojstven mehanizmu stvaranja niti. Uz to kretanje, niza ćelijskih procesa poput filopodijalnog uvlačenja i lamelipodijalnih/lamelalnih kontrakcija oslanja se na kretanje unazad cele mreže niti ili velikih snopova filamenata.
Kako retrogradno pomeranje ili „hodanje” pomoću aktina može imati malu ulogu u pomaganju tim procesima, neophodni su dodatni faktori.

Jedna klasa proteina koja je umešana u translokaciju F-aktina je porodica proteina je miozin, koga čine polimerizovani proteinski molekuli koji učestvuju u izgradnji miofibrila. Imaju dijametar 15 nm i dužinu oko 1,6 µm. Sastoje se od 200—300 molekula miozina.
Miozin čine dva teška i četiri laka polipeptidna lanca. Teški lanci se spiralno uvijaju i formiraju dvostruki heliks. Međutim, na jednom kraju, oni se nabiraju i grade tzv. miozinske glave, a u njihov sastav ulaze i laki lanci (po dva za svaku glavicu).
Ostaje nejasno koji izoformi doprinose ovom procesu u specifičnim situacijama i u kojoj meri.[1][2][3][4] Svaki član porodice miozina poseduje jedinstvena strukturna i funkcionalna svojstva, poput veličine koraka, koja određuje njihovu sposobnost da se uključe u translokaciju F-aktina.[5] Utvrđeno je da su miozini veoma potrebni za ovaj proces da bi se olakšala filopodijska retrakcija.[2]
Miozin II, posebno je povezan je s povlačenjem F-aktina u nekoliko tipova ćelija, uključujući neurone,[1] fibroblaste,[6] i keratocite,[7] s posebnim naglaskom na njegovu ulogu u lameli i lamelipodiji. U početku se verovalo da miozin II utiče nana dinamiku i pokretljivost F-aktina unutar lamele, jer nije primiećen na vodećoj ivici, ali je nedavno primiećen unutar lamelipodije kao izbočina koja dostiže svoj vrhunac, neposredno pre povlačenja.[8] Ovo istraživanje smatraju da je miozin II odgovoran za nastanak i retrogradno kretanje aktinskih lukova - snopova koji se formiraju paralelno s vodećom ivicom i eventualno dodiruju više žarišnih adhezija. Ovaj pokret nastaje na lamelipidijumu i kreće se natrag u lameli, proizvodeći jedinstvenu kontinuirano tekuću aktinsku mrežu u obliku lukova.[8] Shodno tome, predloženo je da se brzina retrogradnog kretanja smanji kada su lučni kontaktni žarišni spojevi u blizini i unutar lamele.[8]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.