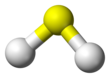
Vodikov sulfid
From Wikipedia, the free encyclopedia
Vodikov sulfid je kemijska spojina s formulo H2S. Je brezbarven plin z neprijetnim vonjem po gnilih jajcih. Je težji od zraka, zelo strupen, jedek, vnetljiv in eksploziven.
 | |||
| |||
| Imena | |||
|---|---|---|---|
| Sistematično ime
sulfan[1] | |||
| Druga imena
vodikov sulfid žveplovodik | |||
| Identifikatorji | |||
3D model (JSmol) |
|||
| 3DMet | |||
Beilstein |
3535004 | ||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.029.070 | ||
| EC število |
| ||
| Gmelin | 303 | ||
| KEGG | |||
| MeSH | Hydrogen+sulfide | ||
PubChem CID |
|||
| RTECS število |
| ||
| UNII | |||
| UN število | 1053 | ||
CompTox Dashboard (EPA) |
|||
| |||
| |||
| Lastnosti | |||
| H2S | |||
| Molska masa | 34,08 g·mol−1 | ||
| Videz | brezbarven plin | ||
| Vonj | po gnilih jajcih | ||
| Gostota | 1,363 g dm−3 | ||
| Tališče | −82 °C (−116 °F; 191 K) | ||
| Vrelišče | −60 °C (−76 °F; 213 K) | ||
| 4 g/L (pri 20 °C) | |||
| Parni tlak | 1740 kPa (pri 21 °C) | ||
| Kislost (pKa) | 7,0[2][3] | ||
| Bazičnost (pKb) | 6,95 | ||
| Lomni količnik (nD) | 1,000644 (0 °C)[4] | ||
| Struktura | |||
Točkovna grupa |
C2v | ||
| Oblika molekule | upognjena | ||
| Dipolni moment | 0,97 D | ||
| Termokemija | |||
| Specifična toplota, C | 1,003 J K−1 g−1 | ||
| Standardna molarna entropija S |
206 J·mol−1·K−1[5] | ||
Std tvorbena entalpija (ΔfH⦵298) |
−21 kJ·mol−1[5] | ||
| Nevarnosti | |||
EU klasifikacija (DSD) (zastarelo) |
|||
| R-stavki (zastarelo) | R12, R26, R50 | ||
| S-stavki (zastarelo) | (S1/2), (S9), S16, S36, S38, (S45), (S61) | ||
| NFPA 704 (diamant ognja) | |||
| Plamenišče | −82,4 °C (−116,3 °F; 190,8 K) | ||
| 232 °C (450 °F; 505 K) | |||
| Meje eksplozivnosti |
4,3–46 % | ||
| Sorodne snovi | |||
| Sorodno vodikovi halogenidi | vodikov selenid vodikov telurid vodikov polonid vodikov disulfid sulfanil | ||
| Sorodne snovi | fosfin | ||
| Sklici infopolja | |||
Plin pogosto nastaja kot produkt bakterijske razgradnje organskih snovi v odsotnosti kisika, na primer v močvirjih in kanalizaciji. Nahaja se tudi v vulkanskih plinih, naravnem plinu, nekaterih vodnih vrelcih, nekaterih kamenih soleh (halit), predvsem v črni himalajski soli, ki se koplje predvsem v goratih predelov Pakistana. Majhne količine H2S proizvede tudi človeški organizem in služi za celično signaliziranje.
Vodna raztopina vodikovega sulfida je šibka žveplovodikova kislina.
Odkritje H2S se pripisuje švedskemu kemiku Carlu Wilhelmu Scheeleju (1777).
Nedavno so ugotovili, da postane pod velikim tlakom pri temperaturi 190 K superprevoden. To pomeni, da ima najvišjo do sedaj znano temperaturo superprevodnega prehoda.[6]