Natrijev oksid
From Wikipedia, the free encyclopedia
Natrijev oksid ali dinatrijev oksid je kemijska spojina s formulo Na2O. Uporablja se v industriji stekla in keramike, vendar ne kot tak. Spojina je bazični anhidrid natrijevega hidroksida, zato pri raztapljanju v vodi tvori natrijev hidroksid:
- Na2O + H2O → 2 NaOH
Podatki na hitro Imena, Identifikatorji ...
| |||
| Imena | |||
|---|---|---|---|
| IUPAC ime
natrijev oksid | |||
| Druga imena
dinatrijev oksid | |||
| Identifikatorji | |||
3D model (JSmol) |
|||
| ECHA InfoCard | 100.013.827 | ||
| EC število |
| ||
PubChem CID |
|||
| UN število | 1825 | ||
CompTox Dashboard (EPA) |
|||
| |||
| |||
| Lastnosti | |||
| Na2O | |||
| Molska masa | 61,98 g·mol−1 | ||
| Videz | bela trdnina | ||
| Gostota | 2,27 g/cm3 | ||
| Tališče | 1.132 °C (2.070 °F; 1.405 K) | ||
| Vrelišče | 1.950 °C (3.540 °F; 2.220 K) | ||
| Sublimacijske okoliščine | sublimira pri 1275 °C | ||
| burno reagira in tvori NaOH | |||
| Topnost | reagira z etanolom | ||
| Struktura | |||
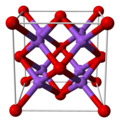
| Kristalna struktura | kubična (antifluoritna), ploskovno centrirana kocka, Pearsonov simbol: cF12 | ||
| Prostorska skupina | Fm3m, No. 225 | ||
| Koordinacijska geometrija |
tetraedrična (Na+); kubična (O2−) | ||
| Termokemija | |||
| Specifična toplota, C | 72,95 J/mol·K | ||
| Standardna molarna entropija S |
73 J/mol·K[1] | ||
Std tvorbena entalpija (ΔfH⦵298) |
-416 kJ/mol[1] | ||
Gibbsova prosta energija (ΔfG˚) |
-377,1 kJ/mol | ||
| Nevarnosti | |||
| Glavne nevarnosti | jedek, burno reagira z vodo | ||
| GHS piktogrami |  [2] [2] | ||
GHS stavki za nevarnost |
H314[2] | ||
GHS stavki za previdnost |
P280[2] | ||
| NFPA 704 (diamant ognja) | |||
| Plamenišče | ni vnetljiv | ||
| Sorodne snovi | |||
| Drugi anioni | natrijev sulfid natrijev selenid natrijev telurid | ||
| Drugi kationi | litijev oksid kalijev oksid rubidijev oksid cezijev oksid | ||
| Sorodno natrijevi oksidi | natrijev peroksid natrijev superoksid | ||
| Sorodne snovi | natrijev hidroksid | ||
| Sklici infopolja | |||
Zapri
Alkalni kovinski oksidi s splošno formulo M2O, v katerih je M lahko litij, natrij, kalij ali rubidij, imajo antifluoritno kristalno strukturo. To pomeni, da so položaji anionov in kationov v primerjavi s CaF2 (fluorit) zamenjani: natrijev kation je tetraedrično koordiniran s štirimi kisikovimi anioni, kisik pa kubično koordiniran z osmimi natrijevimi ioni.[3][4]