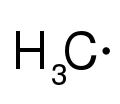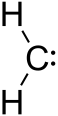Ako reaktívny intermediát sa v chémii označuje zlúčenina alebo molekula, ktorá má vysokú energiu, krátky polčas života a je veľmi reaktívna. Keď vznikne v chemickej reakcii, rýchlo sa premení na stabilnejšiu molekulu. Tieto molekuly je možné izolovať a skladovať iba v výnimočných prípadoch, napríklad pri nízkych teplotách alebo uväznením v matrici. Keď je indikovaná prítomnosť reaktívneho intermediátu, môže pomôcť vysvetliť priebeh chemickej reakcie.[1][2][3][4]
- Nezamieňať s heslom Reakčný intermediát.
Väčšina chemických reakcií prebieha vo viac než jednom elementárnom kroku a reaktívne intermediáty sú vysokoenergetické, ale stabilné produkty, ktoré existujú len v medzikrokoch. Sled jednotlivých krokov tvorí reakčný mechanizmus. Reaktívne intermediáty sa líšia od reaktantu, produktu alebo i reakčného intermediátu iba tým, že ich zvyčajne nie je možné izolovať, ale niekedy sú pozorovateľné rýchlymi spektroskopickými metódami. Reaktívny intermediát je stabilný v tom zmysle, že vzniká v elementárnej reakcii a je nutná ďalšia elementárna reakcia na jeho ďalšiu premenu.
Keď reaktívne intermediátu nie sú pozorovateľné, ich existencia sa musí usudzovať pomocou experimentálnych výsledkov. To väčšinou spočíva v zmene reakčných podmienok, (napríklad teploty alebo koncentrácie), aplikáciou techník chemickej kinetiky či chemickej termodynamiky alebo využitím spektroskopických metód. Reaktívne intermediáty založeé na uhlíku môžu byť radikály, karbény, karbokatióny, karbanióny, aríny a karbíny.
Reaktívne intermediáty majú niekoľko spoločných vlastností:
- nízka koncentrácia v porovnaní s reaktantom alebo produktom
- reaktívne intermediáty zvyčajne nespĺňajú oktetové pravidlo, čo vysvetľuje ich vysokú reaktivitu (s výnimkou karbaniónov)
- často vznikajú pri chemickom rozklade zlúčenín
- ich existenciu je často možné dokázať pomocou spektroskopie
- je nutné uvážiť klietkový efekt
- často dochádza k stabilizácii pomocou konjugácie alebo rezonancie
- často je náročné ich rozlíšiť od tranzitného stavu
- dôkaz existencie často vyžaduje uväznenie v matrici
- Radikál (nespárovaný elektrón)
- Karbén (voľný elektrónový pár na uhlíku)
- Karbokatión (kladný náboj)
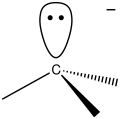
- Karbanión (záporný náboj)
- Karbín
- Benzín (typ arínu)
- Karbenoid
- Ión-neutrálny komplex
- Ketoanióny
- Nitrény
- Oxokarbéniové ióny
- Fosfinidény
- Fosforylnitridy
- Tetrahedrálne intermediáty v karbonylových adičných reakciách
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.