
Hloroamin
From Wikipedia, the free encyclopedia
Hloroamin (NH2Cl) je toksičan gas koji nastaje u reakciji amonijaka i natrijum-hlorida.
Kratke činjenice Hloramin, Identifikacija ...
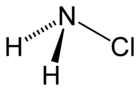
| Hloramin | |
|---|---|
 | |
 | |
| Drugi nazivi | monohloroamin hloramid |
| Identifikacija | |
| CAS registarski broj | 10599-90-3 |
| PubChem[1][2] | 25423 |
| ChemSpider[3] | 23735 |
| EINECS broj | 234-217-9 |
| KEGG[4] | C19359 |
| MeSH | chloramine |
| ChEMBL[5] | CHEMBL1162370 |
| Jmol-3D slike | Slika 1 |
| Svojstva | |
| Molekulska formula | NH2Cl |
| Molarna masa | 51.48 g/mol |
| Agregatno stanje | bezbojan gas |
| Tačka topljenja |
−66 °C |
| Tačka ključanja |
°C |
| Rastvorljivost u drugim rastvaračima | rastvorljiv |
| Srodna jedinjenja | |
| Сродна једињења | dihloroamin nitrogen-trihlorid |
|
| |
| Infobox references | |
Zatvori
Hloroamin je popularno sredstvo za dezinfekciju koje se koristi u vodenim rastvorima. Ima bolje dezinfekciono dejstvo od samog rastvora hlora, jer je hloroamin postojaniji u rastvorima, a sa organskim jedinjenjima ne gradi po zdravlje štetne halometane (kao na primer tetrahlorid ugljenika).[6][7]