Aktivno mjesto katalizatora ili enzima je dio molekule koji direktno sudjeluje u stvaranju veze enzima sa supstratom i u samom katalitičkom procesu.
Aktivno mjesto kod katalizatora predstavlja određeni dio u strukturi katalizatora koji je direktno odgovoran u katalizi kemijske reakcije u krutoj fazi. Kod povećanja broja aktivnih mjesta, kao na primjer pri povećanju površine katalizatora povećava se i sama katalitička aktivnost. Primjeri aktivnih mjesta kod anorganskih katalizatora su hidroksilne grupe (-OH) prisutne na siliki (SiO2) ili šupljine unutar kristala.
Veza enzim supstrat
Kod proteinskih enzima, aktivno mjesto predstavlja mali broj aminokiselina smještenih u unutrašnjosti u hidrofobnom dijelu proteinske molekule, čije prostorno uređenje omogućava vezu specifično s molekulom supstrata. Taj trodimenzijski prostor koji se formira u hidrofobnoj unutrašnjosti enzima je odgovoran za njegovu katalitičku moć. Aminokiseline koje izgrađuju aktivno mjesto ne moraju biti susjedne aminokiseline u peptidnom lancu. Ribozimi su dijelovi ribonukleinske kiseline (RNK) koji su sposobni za katalitičke reakcije. U tom slučaju, aktivno mjesto čine nukleotidi. U trenutku katalitičke reakcije u aktivnom se mjestu supstrat veže s enzimom slabim nekovalentnim vezama (vodikove veze, hidrofobne i Van der Waalsove veze) što omogućava brzu izmjenu molekula supstrata na enzimu. Pošto je veza supstrata na nivou aktivnog mjesta uglavnom vrlo specifična, predložena su dva modela vezivanja molekula na aktivno mjesto.
- Model ključ-brava: svaki supstrat koji se veže za enzim ima točno određeni oblik. Aktivno mjesto enzima je modelirano tako da se supstrat savršeno prostorno uklopi u njega, onemogućivši vezivanje drugih molekula neodgovarajućeg oblika.
- Model pobuđene prilagodbe: Pošto su enzimi fleksibilne strukture, u trenutku vezanja supstrata, aktivno se mjesto prostorno modificira kako bi se prilagodilo obliku vezane molekule.
Kod mnogih enzima na aktivno se mjesto često vežu i kofaktori koji sudjeluju u enzimskoj reakciji kao i inhibitori koji je usporavaju ili onemogućavaju.
Katalitičke reakcije
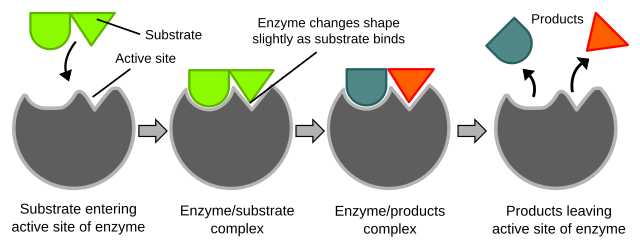
Supstrati vežu aktivno mjesto enzima preko slabih nekovalentnih veza, kako bi stvorili kompleks enzim-supstrat. Bočni lanci aminokiselina koje ulaze u sastav aktivnog mjesta služe kao donori ili akceptori protona ili drugih skupina prema supstratu kako bi olakšali reakciju. Aminokiseline u sastavu aktivnog mjesta nikad ne mijenjaju kemijsku reakciju u kojoj sudjeluju, nego samo povećavaju njenu brzinu (smanjuju energiju aktivacije). Produkt kemijske reakcije je najčešće vrlo nestabilno povezan s aktivnim mjestom zbog steričkih smetnji, pa se brzo odvaja od samog enzima, koji postaje spreman za slijedeću reakciju.
- () Catalytic Site Atlas (CSA) Arhivirano 2013-08-03 na Wayback Machine-u — hosted by EMBL-EBI
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.